
 为测定NaOH、Na2C03混合物中Na2C03的质量分数,甲同学拟采用图(1)所示装置来测定.乙同学拟采用图(2)所示装置来测定.请回答下列问题:
为测定NaOH、Na2C03混合物中Na2C03的质量分数,甲同学拟采用图(1)所示装置来测定.乙同学拟采用图(2)所示装置来测定.请回答下列问题:分析 (1)根据在密封条件容器中气体体积不变判断;碳酸钠与硫酸反应产生的二氧化碳的体积为(c-b+a)mL,根据二氧化碳的体积可计算出碳酸钠的质量,进而确定样品中Na2C03的质量分数;
(2)稀硫酸不易挥发,稀盐酸易挥发出,挥发出来的氯化氢对实验有影响;
(3)根据减少二氧化碳的溶解判断,例如可以用饱和碳酸氢钠溶液,或水面上加一层植物油等;
(4)根据反应前后整个装置的质量差可知产生的二氧化碳的质量,根据二氧化碳的质量再计算出碳酸钠的质量,进而确定样品中Na2C03的质量分数;
(5)测定NaOH、Na2C03混合物中Na2C03的质量分数,可以用氯化钡或氯化钙将碳酸根离子沉淀,根据沉淀的质量可计算出碳酸钠的质量,进而确定样品中Na2C03的质量分数.
解答 解:(1)根据在密封条件容器中气体体积不变判断可知,当注射器增大的体积与加入水的体积相等时,则可以说明此装量不漏气,碳酸钠与硫酸反应产生的二氧化碳的体积为(c-b+a)mL,则二氧化碳的物质的量为$\frac{(c-b+a)×10{\;}^{-3}}{22.4}$mol,根据碳元素守恒可知,样品中Na2C03的质量为$\frac{(c-b+a)×10{\;}^{-3}}{22.4}$mol×106g/mol=$\frac{106(c-b+a)×10{\;}^{-3}}{22.4}$g,所以Na2C03的质量分数为$\frac{\frac{106(c-b+a)×10{\;}^{-3}}{22.4}}{m}$=$\frac{53(c-b+a)}{11200m}$,
故答案为:注射器增大的体积与加入水的体积相等;$\frac{53(c-b+a)}{11200m}$;
(2)稀硫酸不易挥发,稀盐酸易挥发出,挥发出来的氯化氢对实验有影响,所以不能用稀盐酸而要用稀硫酸,
故答案为:稀硫酸不易挥发,稀盐酸易挥发出氯化氢气体,产生误差;
(3)减少二氧化碳的溶解就在就可减小误差,所以可以用饱和碳酸氢钠溶液,或水面上加一层植物油等,
故答案为:将水换成饱和NaHCO3溶液,或在贮水瓶中的水面上加一层植物油都可防止CO2溶于水;
(4)根据反应前后整个装置的质量差可知产生的二氧化碳的质量,根据二氧化碳的质量再计算出碳酸钠的质量,进而确定样品中Na2C03的质量分数,所以除了测定样品的质量,还需测定的另两个数据是反应前装有药品的整个装置的质量,反应后整个装置的质量,
故答案为:反应前装有药品的整个装置的质量;反应后整个装置的质量;
(5)测定NaOH、Na2C03混合物中Na2C03的质量分数,可以用氯化钡或氯化钙将碳酸根离子沉淀,根据沉淀的质量可计算出碳酸钠的质量,进而确定样品中Na2C03的质量分数,所以实验方法为称量一定质量的样品配成溶液,加入足量的BaCl2溶液后得到沉淀,将沉淀进行过滤、洗涤、干燥、冷却、称量.由沉淀(BaCO3)质量计算出Na2CO3的质量,最后计算出Na2CO3的质量分数,
故答案为:称量一定质量的样品配成溶液,加入足量的BaCl2溶液后得到沉淀,将沉淀进行过滤、洗涤、干燥、冷却、称量.由沉淀(BaCO3)质量计算出Na2CO3的质量,最后计算出Na2CO3的质量分数.
点评 本题以NaOH、Na2C03混合物中Na2C03的质量分数的测定载体,考查了实验方案的设计、质量分数的计算等知识,内容较多,难度中等.


 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源: 题型:选择题
| A. | 符合条件的X元素有2种 | |
| B. | Y的最高价氧化物的水化物不可能是强酸 | |
| C. | Y的氢化物中可能存在离子键 | |
| D. | Y的单质在常温下可能是气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 HS-+H+
HS-+H+查看答案和解析>>
科目:高中化学 来源: 题型:解答题
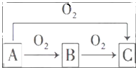 A、B、C是中学化学中常见的三种物质,它们之间的相互转化关系如图(部分反应条件及产物略去):
A、B、C是中学化学中常见的三种物质,它们之间的相互转化关系如图(部分反应条件及产物略去):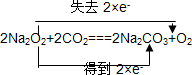 ,并用双线桥法表示上述反应中电子转移的方向和数目,如此反应转移0.5mol电子时,生成物中气体在标准状况下的体积为5.6L.如在AlCl3溶液中投入足量的(1)中的C物质,则反应的离子方程式为2Na2O2+Al3+═AlO2-+O2↑+4Na+.
,并用双线桥法表示上述反应中电子转移的方向和数目,如此反应转移0.5mol电子时,生成物中气体在标准状况下的体积为5.6L.如在AlCl3溶液中投入足量的(1)中的C物质,则反应的离子方程式为2Na2O2+Al3+═AlO2-+O2↑+4Na+.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气是一种无色、密度比空气大的有毒气体 | |
| B. | 红热的铁丝在Cl2中剧烈燃烧生成FeCl2 | |
| C. | 新制氯水能杀菌消毒是因为Cl2有毒,能毒杀细菌 | |
| D. | 氯水放置数天后酸性增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
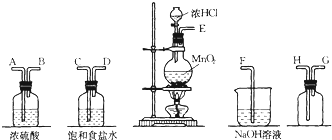
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | R表示非处方药,OTC表示处方药 | |
| B. | 使用青霉素时,直接静脉注射可以不用进行皮肤敏感试验 | |
| C. | 长期大量使用阿司匹林可以预防某些疾病,没有任何副作用 | |
| D. | 阿司匹林属于解热镇痛药 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴加甲基橙显黄色的溶液:Na+、NO3-、SO32-、Fe3+ | |
| B. | 加入Al粉能放出H2的溶液:Al3+、NO3-、HCO3-、Ba2+ | |
| C. | c(OH -)水=1×10-12的溶液:K+、NH4+、Cl -、SO42- | |
| D. | 能使pH试纸显深红色的溶液:Fe 2+、Cl -、Ba 2+、ClO - |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com