
【题目】如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为离子交换膜。

请按要求回答相关问题:
(1)甲烷燃料电池负极电极反应式是:____________________________________。
(2)向乙中加入几滴酚酞溶液,工作一段时间后铁电极附近溶液变红,请用化学用语解释相关原因__________________________________
(3)若在标准状况下,有4.48 L氧气参加反应,则乙装置中C电极上生成的气体的物质的量为__________。
(4)欲用丙装置给铜镀银,b应是____________(填化学式)。
【答案】CH4-8e-+10OH-=CO32-+7H2O 2H2O+2e-= H2+2OH-,使溶液呈碱性 0.4mol Ag
【解析】
(1)甲烷燃料电池中,负极上甲烷失电子和氢氧根离子反应生成碳酸根离子和水;
(2)根据装置可知,甲池中通入甲烷的一极为负极,则乙池中连接负极的铁电极为阴极;
(3)串联电池中转移电子数相等;
(4)欲用丙装置给铜镀银,b连接燃料电池的正极,为阳极,应是镀层金属Ag。
(1)甲烷燃料电池中,负极上甲烷失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为:CH4-8e-+10OH-=CO32-+7H2O;
(2)根据装置可知,甲池中通入甲烷的一极为负极,则乙池中连接负极的铁电极为阴极,向乙中加入几滴酚酞溶液,工作一段时间后铁电极上水电离出的氢离子得电子产生氢气,电极反应为2H2O+2e-= H2+2OH-,附近溶液中氢氧根离子浓度增大,使溶液呈碱性,溶液变红;
(3)串联电池中转移电子数相等,若在标准状况下,有4.48 L氧气参加反应,则转移电子的物质的量=![]() ×4=0.8mol,乙装置中C电极上氯离子放电生成氯气,设生成氯气的物质的量为x;
×4=0.8mol,乙装置中C电极上氯离子放电生成氯气,设生成氯气的物质的量为x;
2Cl-+2e-=Cl2↑
2mol 1mol
0.8mol x
x=0.4mol;
(4)欲用丙装置给铜镀银,b连接燃料电池的正极,为阳极,应是镀层金属Ag。


 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:高中化学 来源: 题型:
【题目】室温下两种金属硫化物MS、QS的沉淀溶解平衡曲线分别为图中的I、II (X2+代表 M2+或Q2+),下列有关说法中正确的是
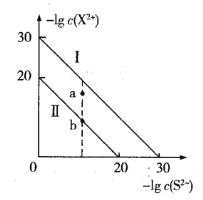
A.MS易与可溶性Q(N03)2的溶液作用转化为QS
B.与a点对应的由MS形成的分散系很稳定
C.向c(M2+)>c(Q2+)的混合溶液中滴加Na2S溶液,首先析出MS沉淀
D.蒸发a点的QS溶液可得到b点状态的QS溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作对应的现象不符合事实的是
选项 | 实验操作 | 现象 |
A | 向盛有 | 溶液逐渐变为黄色,滴加KSCN后溶液变血红色 |
B | 向盛有 | 溶液逐渐褪色,静置后观察到溶液有分层现象 |
C | 向 | 先产生白色沉淀,后沉淀消失 |
D | 向盛有 | 有刺激性气味气体产生,溶液变浑浊 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常用药品柳胺酚的合成路线如图。

已知:①![]() ;
;
②![]() (R代表烷基)
(R代表烷基)![]() ;
;
③当苯环上连有羧基,在苯环上引进的新取代基易进入羧基的间位。
回答下列问题:
(1)柳胺酚的分子式为__,F含有的官能团名称是__。
(2)A的名称为____。
(3)A→B所需试剂为___;D→E的反应类型为___。
(4)B→C的化学方程式为___。
(5)F的同分异构体中既能与FeCl3溶液发生显色反应,又能发生银镜反应的共有__种,其中能发生水解反应,核磁共振氢谱显示4组峰,其峰面积之比为1∶2∶2∶1的同分异构体的结构简式是___。
(6)写出以甲苯为原料(其他无机试剂任选)制备高聚物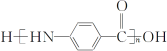 的合成路线。__。
的合成路线。__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,2.24L四氯化碳中含有共价键总数为0.4NA
B.46g NO2和N2O4的混合气体中,含有的氮原子数为1NA
C.1L1.0mol/L的盐酸中含有HCl分子数为NA
D.一定条件下,将2molSO2与1molO2充分反应,得到SO3的分子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯碳酸锰在电子工业中有着重要的应用,湿法浸出软锰矿(主要成分为MnO2,含有少量Fe、Al、Mg等杂质元素)制备高纯碳酸锰的流程如下:其中除杂过程包括:①向浸出液中加入一定量的试剂X,调节浸出液的pH为3.5~5.5;②再加入一定量的软锰矿和双氧水,过滤;③…下列说法正确的是(已知室温下:Kap[Mg(OH)2]=1.8×10-11,Kap[Al(OH)3]=3.0×10-34,Kap[Fe(OH)3]=4.0×10-38。)
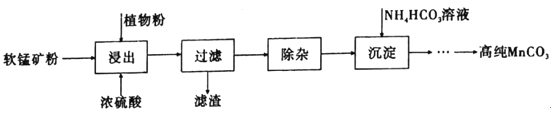
A.浸出时加入植物粉的作用是作为还原剂
B.除杂过程中调节浸出液的pH为3.5~5.5可完全除去Fe、Al、Mg等杂质
C.试剂X可以是MnO、MnO2、MnCO3等物质
D.为提高沉淀MnCO3步骤的速率可以持续升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年是“国际化学元素周期表年”。1869年门捷列夫把当时已知的元素根据物理、化学性质进行排列,准确预留了甲、乙两种未知元素的位置,并预测了二者的相对原子质量,部分原始记录如下。下列说法不正确的是( )

A.元素甲的原子结构示意图为
B.原子半径比较:甲>乙>Si
C.元素乙的简单气态氢化物的稳定性比CH4弱
D.推测乙可以用作半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MgCO3和CaCO3的能量关系如图所示(M=Ca、Mg):
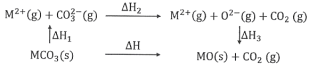
下列说法正确的是
A.△H1(CaCO3)>△H1(MgCO3)>0
B.△H2(MgCO3)>△H2(CaCO3)>0
C.△H1(CaCO3)-△H1(MgCO3)=△H3(CaO)-△H3(MgO)
D.对于MgCO3和CaCO3,△H1+△H2>△H3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以二氧化锰为原料制取高锰酸钾晶体的实验流程如下:

下列说法正确的是
A. “灼烧”可在石英坩埚中进行
B. 母液中的溶质是K2CO3、KHCO3、KCl
C. “结晶”环节采用加热蒸发结晶的方法
D. “转化”反应中,生成的KMnO4和MnO2的物质的量之比为2︰1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com