
关于氢键下列说法正确的是( )
A.每个水分子内含有两个氢键
B.在水蒸气、水和冰中都含有氢键
C.氢键是化学键
D.氨水中,水分子和氨分子间存在氢键
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.目前加碘食盐中主要添加的是KIO3
B.浓硝酸在光照下颜色变黄,说明浓硝酸易挥发
C.绿色食品是不含任何化学物质的食品
D.在空气质量日报中CO2含量属于空气污染指数
查看答案和解析>>
科目:高中化学 来源: 题型:
不具有放射性的同位素称之为稳定同位素,稳定同位素分析法近20年来在植物生理学、生态学和环境科学研究中获得广泛应用。如在陆地生态系统研究中,2H、13C、15N、18O、34S等常用作环境分析指示物。下列有关说法正确的是( )
A.34S原子核内中子数为16
B.1H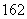 O和1H
O和1H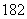 O的相对分子质量不同
O的相对分子质量不同
C.13C和15N原子核内的质子数相差2
D.2H+结合OH-的能力比1H+的更强
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.金属元素与非金属元素能形成共价化合物
B.只有在原子中,质子数才与核外电子数相等
C.目前使用的元素周期表中,最长的周期含有36种元素
D.非金属元素形成的共价化合物中,原子的最外层电子数只能是2或8
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D是元素周期表中的四种短周期元素。
| 元素 | 性质或结构信息 |
| A | 单质制成的高压灯,发出的黄光透雾力强、射程远、且其单质燃烧后生成淡黄色固体 |
| B | 工业上通过分离液态空气获得其单质。原子的最外层电子数是其内层电子总数的2.5倍 |
| C | 单质是双原子分子,常温、常压下是淡黄绿色气体,原子的L层再增加1个电子即达到8电子稳定结构 |
| D | +2价阳离子的核外电子排布与氖原子相同 |
请根据表中信息回答下列问题:
(1)表中与元素A属于同一周期的元素是________(填字母),写出其离子的结构示意图________。
(2)已知C单质能与H2O发生置换反应生成O2,写出C单质与水反应的化学方程式__________________。
(3)对元素B的单质或化合物描述正确的是________。
a.元素B的最高正化合价为+6
b.常温常压下,其单质难溶于水
c.单质分子中含有18个电子
d.在一定条件下,氢气能与B单质反应
(4)A和D两种元素中活动性较强的是________(填元素符号),判断依据是________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数,下列叙述正确的是( )
A.46 g乙醇中含有的化学键数为7NA
B.1 mol氯气和足量NaOH溶液反应转移电子数为2NA
C.1 mol OH-和1 mol —OH(羟基)中含有的质子数均为9NA
D.10 L 0.1 mol·L-1的Na2CO3溶液中,Na+、CO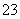 总数为3NA
总数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若它们的温 度和密度均相同,试根据甲、乙的摩尔质量(M)关系,判断下列说法正确的是
度和密度均相同,试根据甲、乙的摩尔质量(M)关系,判断下列说法正确的是
A.若M(甲)>M(乙),则气体体积:甲<乙
B.若M(甲)<M(乙),则气体的压强:甲>乙
C.若M(甲)>M(乙),则气 体的摩尔体积:甲<乙
体的摩尔体积:甲<乙
D.若M(甲)<M(乙),则的分子数:甲<乙
查看答案和解析>>
科目:高中化学 来源: 题型:
电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。
|
图1 |
图2 |
(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择 (填字母序号)。
a.碳棒 b.锌板 c.铜板
用电化学原理解释材料B需定期拆换的原因: 。
(2)图2中,钢闸门C做 极。用氯化钠溶液模拟海水进行实验,D为石墨块,则D上的电极反应式为 ,检测该电极反应产物的方法是 。
| | |
图3 图4
(3)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图3为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
① E为该燃料电池的 极(填“正”或“负”)。F电极上的电极反应式为 。
② 镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语解释其原因 。
(4)乙醛酸(HOOC-CHO)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图4所示,该装置中阴、阳两极为惰性电极,两级室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。
① N电极上的电极反应式为 。
② 若有2 mol H+通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为
mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com