
| A. | 烧红的木炭和热的浓硫酸 | B. | 铜和浓硫酸共热 | ||
| C. | 食盐和浓硫酸共热 | D. | 蔗糖中滴入浓硫酸 |
分析 在反应中浓硫酸体现酸性,说明和物质反应生成硫酸盐,又体现强氧化性,说明在反应中S元素得电子化合价降低,据此分析解答.
解答 解:A.发生的反应为C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,该反应硫酸中S元素化合价由+6价变为+4价,所以浓硫酸作氧化剂,体现氧化性,故A不选;
B.发生的反应为Cu+2H2SO4 (浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,该反应中部分S元素化合价不变、部分S元素化合价由+6价变为+4价,所以浓硫酸体现酸性、强氧化性,故B选;
C.发生的反应为 2NaCl+H2SO4 (浓)$\frac{\underline{\;\;△\;\;}}{\;}$2HCl↑+Na2SO4,该反应中各元素化合价不变,属于复分解反应,浓硫酸体现酸性,故C不选;
D.浓硫酸将有机物中的H、O元素以2:1水的形式脱去而体现脱水性,还能将C氧化为二氧化碳而强氧化性,故D不选;
故选B.
点评 本题考查浓硫酸的性质,浓硫酸具有吸水性、脱水性、强氧化性和酸性,知道吸水性和脱水性区别,注意C反应原理是利用高沸点酸制取易挥发性酸,题目难度不大.


 特高级教师点拨系列答案
特高级教师点拨系列答案 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:填空题
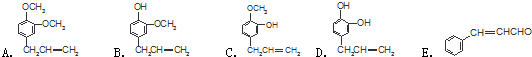
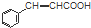 $\stackrel{反应②}{→}$X,
$\stackrel{反应②}{→}$X,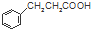 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
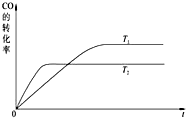 甲醇燃料电池被认为是21世纪电动汽车最佳候选动力源.
甲醇燃料电池被认为是21世纪电动汽车最佳候选动力源.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 112mL | B. | 1008mL | C. | 224mL | D. | 448mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 植物从土壤中吸收含氮养料 | |
| B. | 豆科植物把含氮化合物转变为蛋白质 | |
| C. | 将空气中的氮气转化为含氮化合物 | |
| D. | NH3经催化氧化生成NO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③⑥⑧ | B. | ②③④⑦ | C. | ④⑤⑥⑧ | D. | ①④⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 78gNa2O2晶体中所含阴、阳离子个数均为2NA | |
| B. | PCl3和H2O分子中所有原子的最外层都达到8电子稳定结构 | |
| C. | 1.8gD2O含有NA个中子 | |
| D. | 3.4g氨气中含有0.6NA个N-H键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
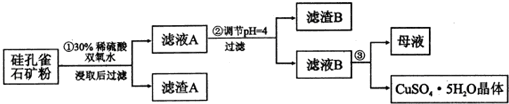
| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com