
氢气(H2)、一氧化碳(CO)、辛烷(C8H18)、甲烷(CH4)的热化学方程式分别为:
H2 (g) + 1/2O2(g) == H2O (l); △H = -285.8 KJ/mol
CO(g) + 1/2O2(g) == CO2(g); △H = -283.0 KJ/mol
C8H18 (l) +(25/2)O2(g) == 8CO2(g) + 9H2O (l); △H = -5518 KJ/mol
CH4 (g) + 2O2(g) == CO2(g) + 2H2O  (l); △H = -890.3 KJ/mol
(l); △H = -890.3 KJ/mol
相同质量的H2、CO、C8H18、CH4完全燃烧时,放出热量最少的是
A.H2 (g) B.CO(g)
C.C8H18 (l) D.CH4 (g)
科目:高中化学 来源: 题型:
始祖鸟烯(Pterodactyladiene),形状宛如一只展翅飞
翔的鸟,其键线式如右图,其中R1、R2为烷烃基。则下
 列有关始祖鸟烯的说法中正确的是
列有关始祖鸟烯的说法中正确的是
A.始祖鸟烯与乙烯互为同系物
B.若Rl=R2=—CH3,则其化学式为C12H16
C.若R1=R2,一定条件下烯烃双键碳原子上的氢也能取代,则始祖鸟烯环上
的二氯代物有10种
D.始祖鸟烯既能使酸性高锰酸钾褪色也能使溴水褪色,其褪色原理是一样
查看答案和解析>>
科目:高中化学 来源: 题型:
设阿伏加德罗常数为NA,下列说法正确的是( )
A.4.4 g乙醛分子中含有的共用电子对数为0.6NA
B.标准状况下,11.2 L二氯甲烷所含分子数为0.5 NA
C.18.8 g苯酚中含有碳碳双键的个数为0.6 NA
D.现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
将V1mL1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50mL)。下列叙述正确的是
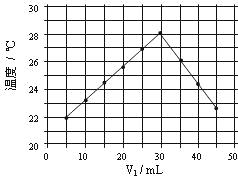
A 做该实验时环境温度为22℃
B 该实验表明化学能可能转化为热能
C NaOH溶液的浓度约为1.0mol/L
D 该实验表明有水生成的反应都是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
白磷与氧可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P-P akJ·mol-1、P-O bkJ·mol-1、P=O ckJ·mol-1、O=O dkJ·mol-1

根据图示的分子结构和有关数据估算该反应的 H,其中正确的是
H,其中正确的是
A.(6a+5d-4c-12b) kJ·mol-1
B.(4c+12b-6a-5d) kJ·mol-1
C.(4c+12b-4a-5d) kJ·mol-1
D.(4a+5d-4c-12b) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1

请回答下列问题:
(1)图中A、C分别表示_________、_________,E的大小对该反应的反应热有无影响?_________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?_________,理由是__________________;
(2)图中ΔH=_________kJ·mol-1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式_____________________________;
(4)如果反应速率v(SO2)为0.05 mol·L-1·min-1,则v(O2)=_______mol·L-1·min-1、v(SO3)=_______mol·L-1·min-1;
(5)已知单质硫的燃烧热为296 kJ·mol-1,计算由S(s)生成3 mol SO3(g)的ΔH_______(要求计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验操作的叙述正确的是
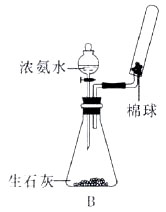
A.实验室利用右图所示装置制取并收集氨气
B.用洁净的玻璃棒蘸取溶液,点在湿润的pH试纸上测定溶液pH
C.用铂丝蘸取某溶液于无色火焰灼烧,透过蓝色钴玻璃观察,火焰呈浅紫色,证明其中含K+
D.在苯和苯酚的混合液中加入足量的浓溴水,振荡、过滤分离出苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用大理石等原料制取安全无毒的杀菌剂过氧化钙。大理石的主要杂质是氧化铁,以下是提纯大理石的实验步骤:

(1)溶解大理石时,用硝酸而不用硫酸的原因是___________________。
(2)操作Ⅱ的目的是__________________,溶液A(溶质是共价化合物)是___________________。
(3)写出检验滤液中是否含铁离子的方法:___________________。
(4)写出加入碳酸铵所发生反应的离子方程式:___________________,写出滤液B的一种用途:___________________。
(5)CaO2中一般含CaO。试按下列提示完成CaO2含量分析的实验设计。
试剂:氢氧化钠标准溶液、盐酸标准溶液、酚酞 仪器:电子天平、锥形瓶、滴定管
实验步骤:
①___________________;②加入___________________;③加入酚酞,用氢氧化钠标准溶液滴定。
(6)若理论上滴定时耗用标准溶液20.00 mL恰好完全反应,实际操作中过量半滴(1 mL溶液为25滴),则相对误差为___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com