
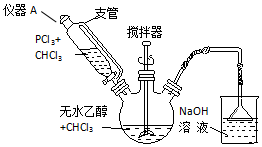
分析 (1)恒压滴液漏斗通过液体上方的气体压强使溶液能顺利滴下;氢氧化钠吸收酸性气体,倒置漏斗防止发生倒吸;分离提纯互不相溶的液体采用分液方法分离;
(2)制得的亚磷酸二乙酯中有PCl3、HCl等酸性物质,可以用碳酸钠除去,而去离子水可以除去NaCl、Na2CO3及部分C2H5OH,据此答题;
(3)反应后的混合溶液中有CHCl3、C2H5Cl、C2H5OH等,都可以用减压蒸馏得到;
(4)根据产率=$\frac{实际产量}{理论产量}×100%$计算.
解答 解:(1)三颈瓶中的蒸汽进入恒压滴液漏斗上方而产生压强,能使恒压滴液漏斗上下压强相等,从而使溶液能顺利滴下(或能使恒压滴液漏斗上下压强相等);氢氧化钠吸收生成酸性HCl气体,倒置漏斗防止发生倒吸;分离提纯互不相溶的液体采用分液方法分离,所用的仪器是分液漏斗;
故答案为:平衡压强,便于液体顺利滴下; 防倒吸;分液漏斗;
(2)制得的亚磷酸二乙酯中有PCl3、HCl等酸性物质,可以用碳酸钠除去,而去离子水可以除去NaCl、Na2CO3及部分C2H5OH;
故答案为:HCl;Na2CO3(NaCl);
(3)反应后的混合溶液中有CHCl3、CH3CH2Cl、CH3CH2OH等,都可以用减压蒸馏得到;
故答案为:CHCl3、C2H5Cl、C2H5OH;
(4)(4)根据PCl3+4C2H5OH→HPO(OC2H5)2+HCl↑+2C2H5Cl+H2O可知,0.3molPCl3和1mol无水乙醇反应,乙醇充分反应,则生成亚磷酸二乙酯为0.25mol,其质量为0.25mol×138g/mol=34.5g,所以其产率为(29.6g÷34.5g)×100%=85.70%;
故答案为:85.80%.
点评 本题考查有机物制备,侧重考查学生对实验基本能力、实验操作、计算能力的掌握和应用,明确仪器用途、物质性质及实验原理是解本题关键,注意碳酸钠、去离子水的作用,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由Al、Cu、稀H2SO4组成原电池,放电时SO42-向Al电极移动 | |
| B. | 由Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3e-+3OH-═Al(OH)3 | |
| C. | 由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:Fe-3e-═Fe3+ | |
| D. | 由Al、Cu、浓硝酸组成原电池作电源,用石墨电极来电解500mL硝酸银溶液,当消耗铜电极32 g时,电解池溶液中pH=2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 目前我国流通的硬币是由合金材料制造的 | |
| B. | 明矾和漂白粉常用于自来水的处理,两者的作用原理不同 | |
| C. | 目前人类使用最广泛的金属材料是铝合金 | |
| D. | 机动车实行限行措施是减少雾霾的途径之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 27g Al3+所含电子数为NA | |
| B. | 11.2L氯气所含的原子数目为NA | |
| C. | 常温常压下32g氧气所含的原子数目为2NA | |
| D. | 标准状况下,22.4 L水中含有的水分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10 mL18.4mol•L-1浓硫酸与足量锌反应,转移电子数为0.184NA | |
| B. | 0.1 mol24Mg18O晶体中所含中子总数为2.0 NA | |
| C. | 在标准状况下,2.8g N2和2.24L CO所含电子数均为1.4NA | |
| D. | 1 L 1 mol•L-1的NaClO溶液中含有ClO-的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com