
【题目】物质的分类是学习化学的一种重要方法,科学合理的分类对于提高学习效率、解决问题都有着重要的意义。请回答下列问题:
I. 纯净物根据其组成和性质有如图分类形式
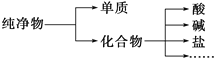
图中所示所属的分类方法为__________________。
II. 有以下13种物质①石墨 ②氧化钠 ③酒精 ④氨水 ⑤二氧化碳 ⑥碳酸氢钠 ⑦氢氧化钠溶液 ⑧纯醋酸 ⑨氯化氢 ⑩硫酸铝 稀硫酸 氯化银 硫酸氢钠
(1)能导电的是 _________;属于非电解质的是 _________。
(2)写出下列物质溶于水的电离方程式:⑥__________;⑧ _________;
(3)写出物质⑥和⑦反应的离子方程式:_________。
(4)写出物质⑥和在水中发生反应的离子方程式:_____________。
【答案】树状分类法 ① ④⑦ ③⑤ NaHCO3=Na++HCO3- CH3COOH ![]() CH3COO-+H+ HCO3-+OH-=CO32-+H2O HCO3-+H+=CO2↑+H2O
CH3COO-+H+ HCO3-+OH-=CO32-+H2O HCO3-+H+=CO2↑+H2O
【解析】
I. 这种分类没有交叉关系,是从属关系或包含关系,图中所示所属的分类方法为树状分类法。
II. 有以下13种物质①石墨 ②氧化钠 ③酒精 ④氨水 ⑤二氧化碳 ⑥碳酸氢钠 ⑦氢氧化钠溶液 ⑧纯醋酸 ⑨氯化氢 ⑩硫酸铝 稀硫酸 氯化银 硫酸氢钠
(1)在设条件下,有能自由移动的离子或自由电子,就能导电,①石墨含有自由电子④氨水含有铵根离子、氢氧根离子⑦氢氧化钠溶液中有钠离子和氢氧根离子 稀硫酸电离出氢离子和硫酸根离子,能导电的是① ④⑦ ;
非电解质是在水溶液中或熔融状态下都不能能够导电的化合物,③酒精和⑤二氧化碳符合,属于非电解质的是③⑤。
(2)溶于水的电离方程式:⑥都为强电解质,可完全电离,⑥NaHCO3=Na++HCO3;醋酸是弱电解质,在水中部分电离:⑧ CH3COOH ![]() CH3COO-+H+ ;
CH3COO-+H+ ;
(3)碳酸氢钠和氢氧化钠反应生碳酸钠和水,反应的离子方程式为HCO3-+OH-=CO32-+H2O。
(4)碳酸氢钠与硫酸氢钠反应生成二氧化碳、水和硫酸钠,反应的离子方程式为HCO3-+H+=CO2↑+H2O。


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
【题目】某研究小组为了探究一种无机矿物质X(仅含四种元素)的组成和性质,设计并完成如下实验:
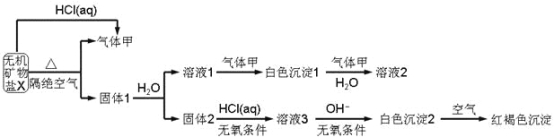
另取10.80gX在惰性气流中加热至完全分解,得到6.40g固体1.请回答如下问题:
(1)画出白色沉淀1中金属元素的原子结构示意图_______,写出气体甲的电子式_______。
(2)X的化学式是______,在惰性气流中加热X至完全分解的化学反应方程式为_______。
(3)白色沉淀2在空气中变成红褐色沉淀的原因是_______(用化学反应方程式表示)。
(4)一定条件下,气体甲鱼固体1中的某种成分可能发生氧化还原反应,写出一个可能的化学反应方程式_______,并设计实验方案验证该反应的产物_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在一定条件可发生如下两个化学反应:①Fe+H2SO4(稀)=FeSO4+H2↑,②2Fe+6H2SO4(浓) ![]() Fe2(SO4)3+3SO2↑+6H2O,试回答下列问题:
Fe2(SO4)3+3SO2↑+6H2O,试回答下列问题:
(1)反应①中__元素(填元素名称)被还原,氧化产物为____;
(2)反应②中还原产物为__;该反应中,氧化剂与还原剂之比为___;
(3)标况下,当反应②中生成33.6LSO2气体时,被氧化的Fe有___mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应:![]() ,
,![]() ,向
,向![]() 、
、![]() 混合溶液中通入适量
混合溶液中通入适量![]() ,溶液中某些离子的物质的量变化如图所示。下列说法不正确的( )
,溶液中某些离子的物质的量变化如图所示。下列说法不正确的( )
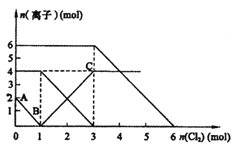
A.通过上述反应,比较还原性强弱![]()
B.原混合液中![]()
C.原混合液中![]()
D.通入![]() 时,溶液中发生的离子反应方程式为
时,溶液中发生的离子反应方程式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A 是石油裂解气的主要产物之一,其产量常用于衡量一个国家石油化工发展水平的标志。下列是有机物 A~G 之间的转化关系:
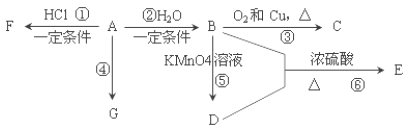
请回答下列问题:
(1)A 的官能团的名称是___________; C 的结构简式是________;
(2)E 是一种具有香味的液体, 由 B+D→E 的反应方程式为___________, 该反应类型是______________;
(3)G 是一种高分子化合物,其结构简式是______________;
(4)比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射物质 F(沸点 12.27°C)进行应急处理.写出由A 制 F 的化学反应方程式______________。
(5)E 的同分异构体能与 NaHCO3溶液反应,写出该同分异构体的结构简式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用NaI溶液中通入少量Cl2得到含碘废液,再利用含碘废液获取NaI固体,实验流程如下:

已知反应②:2I﹣+2Cu2++![]() +H2O
+H2O![]() 2CuI↓+
2CuI↓+![]() +2H+。
+2H+。
回答下列问题:
(1)过滤实验所需要的玻璃仪器有普通漏斗、烧杯、_____________。
(2)反应③中CuI被氧化,还原产物只有NO2,该反应的化学方程式为_________________。当有95.5 g CuI参与反应,则需要标况下______________L的O2才能将生成的NO2在水中完全转化为硝酸。
(3)化合物B中含两种元素,铁原子与另一种元素原子的物质的量之比为3∶8,则化合物B的化学式为_____________。
(4)反应⑤中生成黑色固体和无色气体,黑色固体的俗称为磁性氧化铁,则反应⑤的化学方程式为______。
(5)将足量的Cl2通入含12 g NaI的溶液中,一段时间后把溶液蒸干得到固体的质量为_________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工业对国民经济和社会发展具有重要意义。对于密闭容器中的反应:N2(g)+3H2(g)![]() 2NH3(g),在673 K、30 MPa下,n(NH3)和n(H2)随时间变化的关系如图所示。下列叙述正确的是
2NH3(g),在673 K、30 MPa下,n(NH3)和n(H2)随时间变化的关系如图所示。下列叙述正确的是

A. 点a的正反应速率比点b的小
B. 点c处反应达到平衡
C. 点d(t1时刻)和点e(t2时刻)处n(N2)不一样
D. 点e处反应达到平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示的是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质和反应条件被略去。化合物A是家庭生活中常用的一种调味品,反应①称之为“氯碱工业”。D是黄绿色气体,H的水溶液具有漂白、杀菌性,J为红褐色沉淀。
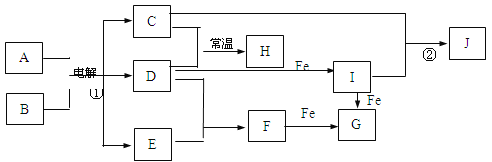
(1)H的化学式为____________。
(2)写出I与Fe反应生成G的离子方程式为_____________________________。
(3)反应①的化学方程式为____________________________________________。
(4)反应②的离子方程式为____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ksp(AgCl)=1.56×10-10,Ksp(AgBr)=7.7×10-13 ,Ksp(Ag2CrO4)=9×10-11。某溶液中含有Cl-、Br-和CrO42-,浓度均为0.010mol/L,向该溶液中逐滴加入0.010mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为( )
A. Cl-、Br-、CrO42-B. Br-、Cl-、CrO42-
C. CrO42-、Br-、Cl-D. Br-、CrO42-、Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com