
【题目】某溶液X中可能含有下列离子中的若干种:Cl-、SO42-、CO32-、Na+、Mg2+,为了确定溶液的组成,取100mL该溶液进行如下实验:
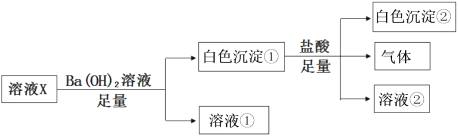
(1)溶液X中一定存在的离子有__________;一定不存在的离子有________。
(2)写出白色沉淀①与足量盐酸反应的离子方程式_____________。
【答案】SO42-、CO32-、Na+ Mg2+ BaCO3 + 2H+ = Ba2+ + H2O + CO2↑
【解析】
某溶液X中可能含有下列离子中的若干种:Cl-、SO42-、CO32-、Na+、Mg2+,加入足量氢氧化钡溶液,产生白色沉淀①和溶液①,白色沉淀①中加入足量盐酸,产生气体,则可判断溶液X中含有CO32-,沉淀①中含有BaCO3,因Mg2+与CO32-不能大量共存则溶液X中不含Mg2+,反应后还有白色沉淀②,则为不溶于盐酸的BaSO4,可判断溶液X中含有SO42-;根据溶液为电中性可判断还含有阳离子Na+;不能确定溶液中是否含有Cl-,据此分析。
某溶液X中可能含有下列离子中的若干种:Cl-、SO42-、CO32-、Na+、Mg2+,加入足量氢氧化钡溶液,产生白色沉淀①和溶液①,白色沉淀①中加入足量盐酸,产生气体,则可判断溶液X中含有CO32-,沉淀①中含有BaCO3,因Mg2+与CO32-不能大量共存则溶液X中不含Mg2+,反应后还有白色沉淀②,则为不溶于盐酸的BaSO4,可判断溶液X中含有SO42-;根据溶液为电中性可判断还含有阳离子Na+;不能确定溶液中是否含有Cl-。
根据分析可知:(1)溶液X中一定存在的离子有SO42-、CO32-、Na+;一定不存在的离子有Mg2+;
(2)写出白色沉淀①与足量盐酸反应的离子方程式为BaCO3 + 2H+ = Ba2+ + H2O + CO2↑。


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源: 题型:
【题目】钴元素是三元锂离子电池阳极材料的重要成分。请回答下列问题:
(1)钴元素在周期表中的位置是___________,其外围电子排布式为___________。
(2)已知第四电离能大小:I4(Fe)> I4 (Co),从原子结构的角度分析可能的原因是___________。
(3)配位化学创始人维尔纳发现,取1mol配合物CoCl3·6NH3(黄色)溶于水,加人足量硝酸银溶液,产生3mol白色沉淀,沉淀不溶于稀硝酸。原配合物中络离子形状为正八面体。
①根据上述事实推测原配合物中络离子化学式为___________。
②该配合物在热NaOH溶液中发生反应,并释放出气体,该反应的化学方程式___________;生成气体分子的中心原子杂化方式为___________。
(4)经X射线衍射测定发现,晶体钴在417℃以上堆积方式的剖面图如图所示,则该堆积方式属于___________,若该堆积方式下的晶胞参数为acm,则钴原子的半径为___________pm。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列指定溶液中微粒的物质的量浓度关系一定正确的是![]()
A.某溶液中由水电离出的![]() ,若
,若![]() 时,该溶液pH一定为
时,该溶液pH一定为![]()
B.向澄清石灰水中通入![]() 至
至![]() 恰好完全反应:
恰好完全反应:![]()
C.![]() 溶液与
溶液与![]() 溶液等体积混合
溶液等体积混合![]() 无气体逸出
无气体逸出![]() :
:![]()
D.![]() 溶液与
溶液与![]() 溶液等体积混合
溶液等体积混合![]() :
:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向![]() 氨水中滴加盐酸,溶液中水电离出的氢离子浓度随加入盐酸体积的变化如图所示.下列说法错误的是
氨水中滴加盐酸,溶液中水电离出的氢离子浓度随加入盐酸体积的变化如图所示.下列说法错误的是 ![]()
![]()
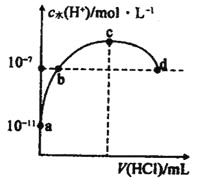
A.c点表示氨水与盐酸恰好完全反应
B.b点溶液呈中性,d点溶液呈酸性
C.常温下,![]() 的数量级为
的数量级为![]()
D.a、b之间的任意一点(不包括a、b点)溶液中:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应:2SO2(g)+O2(g)![]() 2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
A. 增大压强 B. 升高温度 C. 使用催化剂 D. 多充O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳樟醇和橙花叔醇是决定茶叶花甜香的关键物质。芳樟醇和橙花叔醇的结构如图所示,下列有关叙述正确的是
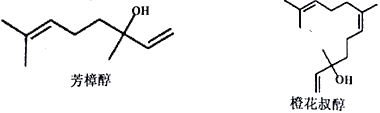
A. 橙花叔醇的分子式为C15H28O
B. 芳樟醇和橙花叔醇互为同分异构体
C. 芳樟醇和橙花叔醇与H2完全加成后的产物互为同系物
D. 二者均能发生取代反应、加成反应、还原反应,但不能发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
①干冰晶体气化时需破坏分子间作用力
②HClO 分子的结构式:H—Cl—O
③NH4Cl 的电子式 ![]()
④H2O2分子中既含极性共价键,又含非极性共价键
⑤由于 H—F 键比 H—Cl 键强,所以 HF 的沸点比 HCl 的沸点高
⑥NaHSO4 在溶于水时发生电离,破坏了离子键和共价键
⑦用电子式表示溴化氢的形成过程为:![]()
A.①②⑤B.②④⑥C.③⑤⑦D.①④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国工业废水中几种污染物即其最高允许排放浓度如下表。下列说法不正确的是
污染物 | 汞 | 镉 | 铬 | 铅 | 砷 | 氰化物 |
主要存在形式 |
|
|
|
|
|
|
最高允许排放浓度
|
|
|
|
|
|
|
注:我国规定酸、碱废水pH的最大允许排放标准是大于6、小于![]()
A.![]() 、
、![]() 、
、![]() 是重金属离子
是重金属离子
B.对于![]() 的废水可用中和法处理
的废水可用中和法处理
C.将![]() 转化为
转化为![]() 是用氧化还原的方法
是用氧化还原的方法
D.在含有![]() 的废水中加入
的废水中加入![]() ,可使转变为沉淀而除去
,可使转变为沉淀而除去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
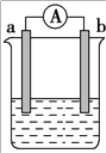
(1)当电极 a 为 Al,电极 b 为 Cu,电解质溶液为浓硝酸时,该电池的 负极为_________(填“Al”或“Cu”),正极的电极反应式为___________。
(2)当电极 a 为 Al,电极 b 为 Mg,电解质溶液为氢氧化钠溶液时,该 电池负极的电极反应式为_____,当反应中收集到标准状况下 224 mL 气体时,消耗的电极质量为_____g。
(3)燃料电池的工作原理是将燃料和氧化剂(如 O2)反应所产生的能量直接转化为电能。现设计一种燃料电池,以对气体吸附能力很强的 Pt 作为两个电极,甲烷为燃料,采用氢氧化钠溶液 为电解质溶液,则通甲烷的电极为_____极(填“正”或“负”),该电池正极的电极反应式 为_____,该电池工作一段时间后,溶液中OH-的浓度将_____(填“增 大”、“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com