
| A、葡萄糖的结构简式:C6H12O6 | ||
| B、NaHCO3的电离:NaHCO3=Na++H++CO32- | ||
C、质子数为53、中子数为78的碘原子:
| ||
D、CO2的电子式: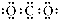 |
131 59 |
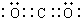 ,故D错误;
,故D错误;

科目:高中化学 来源: 题型:
| A、用洁净铁丝蘸取两种样品在煤气火焰上灼烧,使火焰颜色发生明显变化的是小苏打 |
| B、用两只玻璃杯分别加入少量的两种样品,再加入等量的食醋,产生气泡快的是小苏打 |
| C、分别用炒锅加热两种样品,全部分解挥发,没有残留物质的是小苏打 |
| D、先将两样品配成溶液,分别加入石灰水,无白色沉淀生成的是小苏打 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1s22s22p63s23p2→1s22s22p63s23p1 |
| B、1s22s22p63s23p3→1s22s22p63s23p2 |
| C、1s22s22p63s23p4→1s22s22p63s23p3 |
| D、1s22s22p63s23p1→1s22s22p63s2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由①知:氢气的燃烧热△H=-241.8 kJ/mol |
| B、由①、②知:2H2S(g)+O2(g)=2S(g)+2H2O(g)△H=-443.4 kJ/mol |
C、 反应②中的能量变化能用图表示 |
| D、若反应②中改用固态硫,放热将大于20.1kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、大于50% |
| B、小于50% |
| C、小于或等于50% |
| D、大于或等于50% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,11.2 L NH3溶于1 L水,溶液中含有N原子的微粒总数为0.6NA |
| B、1.00 mol NaCl中,所有Na+的最外层电子总数约为8×6.02×1023 |
| C、欲配制1.00 L 1.00 mol?L-1的NaCl溶液,可将58.5 g NaCl溶于1.00 L水中 |
| D、1mol FeCl3完全转化为Fe(OH)3胶体后形成NA个胶粒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标况下,4.48L SO2中含O原子数为0.4NA |
| B、常温常压下,8.96LCO2中所含分子数为0.4 NA |
| C、500mL 0.1 mol/L的NaOH溶液中含OH-的数目为0.05NA |
| D、常温常压下,1.6g CH4中含H原子数为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.5mol?L-1 28.57% |
| B、2.2mol?L-1 23.07% |
| C、1.5mol?L-1 24.55% |
| D、2.5mol?L-1 18.37% |
查看答案和解析>>
科目:高中化学 来源: 题型:
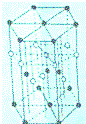 已知:X、Y、Z、W是四种短周期元素,它们的原子序数依次增大.其中X、Y、Z同周期,X与W同主族;X与Z形成的常见化合物之一常被用于高炉炼铁,且X、Z原子的L层都有2个未成对电子;Q+离子M层3d轨道电子为全充满状态.请回答下列问题:
已知:X、Y、Z、W是四种短周期元素,它们的原子序数依次增大.其中X、Y、Z同周期,X与W同主族;X与Z形成的常见化合物之一常被用于高炉炼铁,且X、Z原子的L层都有2个未成对电子;Q+离子M层3d轨道电子为全充满状态.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com