
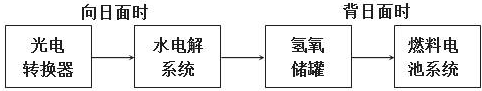
分析 (1)根据盖斯定律,由已知热化学方程式乘以合适的系数进行适当的加减,反应热也乘以相应的系数进行相应的加减;
(2)根据氢氧燃料电池中氢气在负极放电,结合电解质溶液为氢氧化钾溶液来写出负极反应方程式;某段时间内氢氧储罐中共收集到33.6L,为1.5mol气体,则生成氢气1mol,转移电子2mol,据此计算;
(3)阴极发生还原反应,CO2被还原生成CO,总反应式减去阳极反应式得阴极反应式;根据△G=△H-T△S判断.
解答 解:(1)①已知:N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ•mol-1①
N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534.0kJ•mol-1②
NO2(g)=$\frac{1}{2}$N2O4(g)△H=-26.35kJ•mol-1③
根据盖斯定律,②×2-①-③×2得2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) 故△H=2×(-534.0kJ•mol-1)-67.7kJ•mol-1-2×(-26.35kJ•mol-1)=-1083.2kJ•mol-1;故答案为:2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)△H=-1083.0 kJ/mol;
(2)氢氧燃料电池中氢气在负极放电,由于电解质溶液为氢氧化钾溶液,故负极的电极反应式为:H2-2e-+2OH-=2H2O;如果某段时间内氢氧储罐中共收集到33.6L,为1.5mol气体,电解方程式为2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑,则生成1mol氢气和0.5mol氧气,生成1mol氢气转移电子2mol,所以该段时间内水电解系统中转移电子的物质的量为2mol,故答案为:H2-2e-+2OH-=2H2O;2;
(3)总反应式为2CO2=2CO+O2,阳极反应为4OH--4e-=O2↑+2H2O,总反应式减去阳极反应式得阴极反应式,所以阴极反应为:2CO2+4e-+2H2O=2CO+4OH-,由于反应2CO=2C+O2是吸热的△H>0,熵值减小的反应,所以△G=△H-T△S>0,是不能自发进行的;
故答案为:2CO2+4e-+2H2O=2CO+4OH-;不能;△H>0吸热,△S<0.
点评 本题考查了盖斯定律以及电解原理的应用,注意把握电极方程式的书写方法,根据电极反应判断生成的气体的量及转移电子的量,题目难度不大.


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验编号 | NaOH起始读数 | NaOH终点读数 |
| 第一次 | 0.10mL | 18.40mL |
| 第二次 | 3.00mL | 21.10mL |
| 第三次 | 0.20mL | 20.40mL |
| 第四次 | 0.00mL | 18.20mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ•mol-1 | 436 | 391 | 946 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁丝在纯氧中燃烧 | B. | 红热的铁和水蒸气反应 | ||
| C. | 将Fe2(SO4)3 溶液蒸干后灼烧 | D. | 加热氢氧化铁固体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com