
将一定量的Na2O2和NaHCO3混合后,在密闭容器中加热充分反应,排出气
体,冷却后有固体物质剩余,下列选项不正确的是( )。
| Na2O2/mol | NaHCO3/mol | 剩余的固体物质 | |
| A | 1 | 2 | Na2CO3 |
| B | 1.5 | 2 | Na2O2 Na2CO3 |
| C | 2 | 1 | Na2O2 NaOH Na2CO3 |
| D | 2 | 2 | NaOH Na2CO3 |
解析 有关的反应方程式依次为2NaHCO3 Na2CO3+CO2↑+H2O、2CO2+2Na2O2===2Na2CO3+O2、2Na2O2+2H2O===4NaOH+O2↑。当Na2O2与NaHCO3的物质的量之比为1∶2时,二者反应的总方程式为2Na2O2+4NaHCO3
Na2CO3+CO2↑+H2O、2CO2+2Na2O2===2Na2CO3+O2、2Na2O2+2H2O===4NaOH+O2↑。当Na2O2与NaHCO3的物质的量之比为1∶2时,二者反应的总方程式为2Na2O2+4NaHCO3 4Na2CO3+O2↑+2H2O;当Na2O2与NaHCO3的物质的量之比为1∶1时,2Na2O2+2NaHCO3
4Na2CO3+O2↑+2H2O;当Na2O2与NaHCO3的物质的量之比为1∶1时,2Na2O2+2NaHCO3 2Na2CO3+O2↑+2NaOH,即1∶2<n(Na2O2)∶n(NaHCO3)≤1∶1,反应后剩余固体的成分为Na2CO3和NaOH,n(Na2O2)∶n(NaCO3)>1∶1时,反应后剩余固体为Na2O2、NaOH、Na2CO3,由此可以判断A、C、D对,B错。
2Na2CO3+O2↑+2NaOH,即1∶2<n(Na2O2)∶n(NaHCO3)≤1∶1,反应后剩余固体的成分为Na2CO3和NaOH,n(Na2O2)∶n(NaCO3)>1∶1时,反应后剩余固体为Na2O2、NaOH、Na2CO3,由此可以判断A、C、D对,B错。
答案 B


 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
以下非金属氧化物与其引起的环境问题及主要来源对应正确的是( )
| 选项 | 氧化物 | 环境问题 | 主要来源 |
| A | CO | 煤气中毒 | 含碳燃料的不完全燃烧 |
| B | SO2 | 光化学烟雾 | 汽车尾气的排放 |
| C | NO2 | 温室效应 | 工厂废气的排放 |
| D | CO2 | 酸雨 | 化石燃料的燃烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一密闭容器中,反应mM(气) 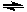 nN(气)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,M的浓度为原来的80%,则( )
nN(气)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,M的浓度为原来的80%,则( )
A、平衡正向移动; B、物质M的转化率增大; C、n > m D、物质N的质量分数减少
查看答案和解析>>
科目:高中化学 来源: 题型:
下列热化学方程式书写正确的是 )。
A.2SO2+O2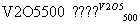 2SO3 ΔH=-196.6 kJ·mol-1
2SO3 ΔH=-196.6 kJ·mol-1
B.H2g)+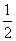 O2g)===H2Ol) ΔH=-285.8 kJ·mol-1
O2g)===H2Ol) ΔH=-285.8 kJ·mol-1
C.2H2g)+O2g)===2H2Ol) ΔH=-571.6 kJ
D.Cs)+O2g)===CO2g) ΔH=+393.5 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,通过下列反应可以制备特种陶瓷的原料MgO:MgSO4s)+COg)MgOs)+CO2g)+SO2g) ΔH>0
该反应在恒容密闭容器中达到平衡后,若仅改变图中横坐标x的值,纵坐标y随x变化趋势合理的是 )。
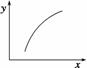
| 选项 | x | y |
| A | 反应时间 | CO2与CO的物质的量之比 |
| B | 反应温度 | 逆反应速率 |
| C | 体系压强 | 平衡常数K |
| D | MgSO4的质量 | CO的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
“心得安”是治疗心脏病的药物,下面是它的一种合成路线(具体反应条件和部分试剂略):
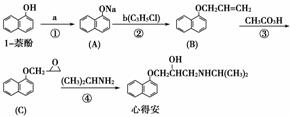
回答下列问题:
(1)试剂a是________,试剂b的结构简式为________,b中官能团的名称是________。
(2)③的反应类型是________。
(3)心得安的分子式为________。
(4)试剂b可由丙烷经三步反应合成:
C3H8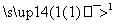 X
X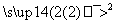 Y
Y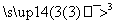 试剂b
试剂b
反应1的试剂与条件为________,反应2的化学方程式为______________, 反应3的反应类型是________。
(5)芳香化合物D是1萘酚的同分异构体,其分子中有两个官能团,能发生银镜反应,D能被 KMnO4酸性溶液氧化成E(C2H4O2)和芳香化合物F(C8H6O4),E和F与碳酸氢钠溶液反应均能放出CO2气体,F芳环上的一硝化产物只有一种。D的结构简式为________;由F生成一硝化产物的化学方程式为________________,该产物的名称是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中含有如下离子组中的若干种:K+、Mg2+、Fe3+、Fe2+、
CO32-、NO3-、SO42-、I-、SiO32-、Cl-且物质的量浓度相同。某同学欲探究该溶液的组成,进行了如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到浅紫色火焰;
Ⅱ.另取原溶液加入足量盐酸有无色气体生成,该气体遇空气变成红棕色,此时溶液颜色加深,但无沉淀生成;
Ⅲ.取Ⅱ反应后的溶液分置于两支试管中加入BaCl2溶液,有白色沉淀生成,再滴加
KSCN溶液上层清液变红;第二支试管中加入CCl4,充分振荡静置后溶液分层,下
层出现紫红色。下列说法正确的是
A.原溶液中肯定不含Mg2+、SiO32-
B.步骤Ⅱ中无色气体可能含有CO2,原溶液中可能含有CO32-
C.原溶液由K+、Fe2+、NO3-、I-、SO42-五种离子组成
D.原溶液中一定含有Mg2+、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
硫元素有多种化合价,可形成多种化合物。
(1)旋转喷雾干燥法是去除燃煤烟气中二氧化硫的方法之一,工艺流程如下图所示,写出雾化器中发生反应的化学方程式:________________________________________________。
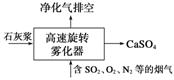
(2)已知NaHSO3溶液显弱酸性,其原因用离子方程式表示为____________。
(3)请按照浓度由大到小的顺序排列0.1 mol·L-1 Na2SO3 溶液中的离子________。Na2SO3溶液放置于空气中一段时间后,溶液的pH________(填“增大”、“减小”或“不变”)。
(4)某同学在常温下设计如下实验流程探究Na2S2O3的化学性质。
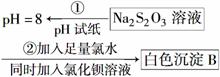
实验①可说明________(填字母)。
A.该Na2S2O3溶液中水电离的c(OH-)=10-8 mol·L-1
B.H2S2O3是一种弱酸
C.Na2S2O3是一种弱电解质
D.Na2S2O3能发生水解,其离子方程式为S2O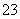 +2H2O===H2S2O3+2OH-
+2H2O===H2S2O3+2OH-
实验②说明Na2S2O3具有________性。写出发生反应的离子方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)Li3N中氮以N3-存在,基态N3-的电子排布式为________。
(2)O=O键的键能为497.3kJ·mol-1,O—O键的键能为142kJ·mol-1,说明O2中的________键更稳定(填“σ”或“π”)。
(3)BF3与F-可形成BF4-离子。BF3与F-形成BF4-离子时,二者形成的化学键为________键。
(4)X+中所有电子正好充满K、L、M三个电子层,则X的元素符号是________,基态X+的电子排布式为_____________________________________________。
(5)与N2互为等电子体的一种分子为 (填化学式),该分子中σ键与π键的个数比为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com