
���� ��A���Է����е��ж������ǡ�H-T��S��0����Ϸ�Ӧ���������ж���Ҫ��������
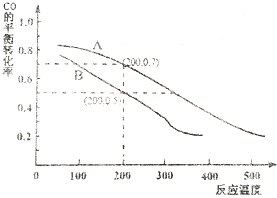
B���Ƚ�ѹǿ��ͳһ�¶ȣ�����ͬ�¶�200��ʱ��A��ת���ʱ�B�ĸߣ�˵��ѹǿ�ı䣬ƽ�������ƶ���
C����G=��H-T��S=0��˵���˷�Ӧ�ﵽƽ��״̬��
D�����ͼ����������ʽ�������⣻
��A�����ӷ�Ӧ���Ũ�ȣ���ѧ��Ӧ���ʼӿ죬��ѧƽ�������ƶ���
B��Ҳ�����ӷ�Ӧ���Ũ�ȣ���ѧƽ�������ƶ���
C��ͨ����Ҫ�ļ���ͷ����жϣ�����ij���£���ӦN2��g��+3H2��g��?2NH3��g����ij��ѹ�������з����ϳɰ��ķ�Ӧ����ƽ��ʱ��������к���1.0molN2��0.4molH2��0.4molNH3����ʱ�ݻ�Ϊ2���������¶Ⱥ�ѹǿ���䣬���֮�ȵ��������ʵ���֮�ȣ����������ͨ��0.36mol N2����ʽ����ƽ��Ũ�ȣ�
D��ͨ����Ҫ�ļ���ͷ����жϣ�����ij���£���ӦN2��g��+3H2��g��?2NH3��g����ij��ѹ�������з����ϳɰ��ķ�Ӧ����ƽ��ʱ��������к���1.0molN2��0.4molH2��0.4molNH3����ʱ�ݻ�Ϊ2���������¶Ⱥ�ѹǿ���䣬���֮�ȵ��������ʵ���֮�ȣ����������ͨ��0.36mol H2����ʽ����ƽ��Ũ�ȣ�
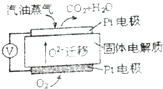
��1����������ڸ������ܴ���O2-����������������Ӧ����C6H14ʧȥ��������CO2�����������غ�͵���غ�д���缫��Ӧʽ��
��2��һ�����ӵĵ�����1.602��10-19C������·��ͨ��1.929��105 C�ĵ���ʱ�����ӵĸ���=$\frac{1.929��1{0}^{5}C}{1.602��1{0}^{-19}C}$=1.204��1024�����ӵ����ʵ���=$\frac{1.204��1{0}^{24}}{6.02��1{0}^{23}mo{l}^{-1}}$=2mol������ת�Ƶ��Ӻ������Ĺ�ϵʽ���㣮
��� �⣺��A����CO2��g��+3H2��g���TCH3OH��l��+H2O��l�����ر��S��0����Ӧ�ʱ��H��0�������������H-T��S��0��
�ʴ�Ϊ�����£�
B���Ƚ�ѹǿ��ͳһ�¶ȣ�����ͬ�¶�200��ʱ��A��ת���ʱ�B�ĸߣ�˵��ѹǿ�ı䣬ƽ�������ƶ�������CO��g��+2H2��g��?CH3OH��g���������������С�ķ�Ӧ����ѹǿ�ĸı�ֻ��������ѹǿ������A���ѹǿ��Ϊ5.0MPa��
�ʴ�Ϊ��A��
C����G=��H-T��S=0��˵����Ӧ�ﵽƽ��״̬�����ʱ��Ӧ��V��=V����
�ʴ�Ϊ��=��
D�������COamol������H22amol
����������������CO��g��+2H2��g��?CH3OH��g����
��Ӧǰ��mol�� ��a ������ 2a ����������0
��Ӧ�ˣ�mol�� 0.5a �� �� a �������� ��0.5a
ƽ��ʱ��mol�� 0.5a���� a �������� ��0.5a
����ã�$\frac{0.5a}{0.5a+a+0.5a}$��100%=25%��
�ʴ�Ϊ��25%��
��A�������¶Ⱥ�������䣬ͨ������N2�����ӷ�Ӧ�ﵪ����Ũ�ȣ���ѧ��Ӧ���ʼӿ죬��ѧƽ�������ƶ�����A��ȷ��
B�������¶Ⱥ�������䣬ͨ������H2��Ҳ�����ӷ�Ӧ���Ũ�ȣ���ѧƽ�������ƶ�����B��ȷ��
C������ij���£���ӦN2��g��+3H2��g��?2NH3��g����ij��ѹ�������з����ϳɰ��ķ�Ӧ����ƽ��ʱ��������к���1.0molN2��0.4molH2��0.4molNH3����ʱ�ݻ�Ϊ2������ʽ����ƽ��Ũ�ȣ�
N2��g��+3H2��g��?2NH3��g��
��ʼ����mol/L�� 0.6 0.5 0
�仯����mol/L�� 0.1 0.3 0.2
ƽ������mol/L�� 0.5 0.2 0.2
��������µ�ƽ�ⳣ��K=$\frac{0��{2}^{2}}{0.5��0��{2}^{3}}$=10��
�����¶Ⱥ�ѹǿ���䣬���֮�ȵ��������ʵ���֮�ȣ����������ͨ��0.36mol N2����ʱ�������Ϊ��1.0mol+0.4mol+0.4mol������1.0mol+0.4mol+0.4mol+0.36mol��=2��V��V=2.4L������Q��c��=$\frac{��\frac{0.4}{2.4}��^{2}}{\frac{1+0.36}{2.4}����\frac{0.4}{2.4}��^{3}}$=10.58��K=10��ƽ��������У���C����
D������ij���£���ӦN2��g��+3H2��g��?2NH3��g����ij��ѹ�������з����ϳɰ��ķ�Ӧ����ƽ��ʱ��������к���1.0molN2��0.4molH2��0.4molNH3����ʱ�ݻ�Ϊ2������ʽ����ƽ��Ũ�ȣ�
N2��g��+3H2��g��?2NH3��g��
��ʼ����mol/L�� 0.6 0.5 0
�仯����mol/L�� 0.1 0.3 0.2
ƽ������mol/L�� 0.5 0.2 0.2
��������µ�ƽ�ⳣ��K=$\frac{0��{2}^{2}}{0.5��0��{2}^{3}}$=10��
�����¶Ⱥ�ѹǿ���䣬���֮�ȵ��������ʵ���֮�ȣ����������ͨ��0.36mol H2����ʱ�������Ϊ��1.0mol+0.4mol+0.4mol������1.0mol+0.4mol+0.4mol+0.36mol��=2��V��V=2.4L������Q��c��=$\frac{��\frac{0.4}{2.4}��^{2}}{\frac{1}{2.4}����\frac{0.4+0.36}{2.4}��^{3}}$=2.1��K=10��ƽ��������У���D��ȷ��
��ѡABD��
��1����������ڸ������ܴ���O2-����������������Ӧ����1molC6H14ʧȥ��������CO2����ʧȥ38mole-���缫��ӦΪ��C6H14-38e-+19O2-=6CO2+7H2O��
�ʴ�Ϊ��C6H14-38e-+19O2-=6CO2+7H2O��
��2��һ�����ӵĵ�����1.602��10-19C������·��ͨ��1.929��105 C�ĵ���ʱ�����ӵĸ���=$\frac{1.929��1{0}^{5}C}{1.602��1{0}^{-19}C}$=1.204��1024�����ӵ����ʵ���=$\frac{1.204��1{0}^{24}}{6.02��1{0}^{23}mo{l}^{-1}}$=2mol������ת�Ƶ��Ӻ������Ĺ�ϵʽ�����������ʵ���Ϊ1mol�������Ϊ22.4L��
�ʴ�Ϊ��22.4��
���� ���⿼�鷴Ӧ�Է��Ե��жϡ���ѧƽ��״̬�жϣ��漰Ӱ�컯ѧƽ��ļ��㡢�Ȼ�ѧ����ʽ�Լ�����֪ʶ���ѶȽϴ���ƽ�⽨����;�����бȽ��ǹؼ�����Ͽ����˻�ѧ��Ӧ���ʺͶ�ͼ������������������ۺ�����Ҫ��ϸߣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| �� | �� | �� | �� | ||
| �ܱ��������/L | 2 | 2 | 2 | 1 | |
| ��ʼ���ʵ��� | n��SO2��/mol | 0.4 | 0.8 | 0.8 | 0.4 |
| n��O2��/mol | 0.24 | 0.24 | 0.48 | 0.24 | |
| SO2��ƽ��ת����/% | 80 | ��1 | ��2 | ��3 | |
| A�� | SO2��ƽ��ת���ʣ���1����2=��3 | B�� | SO3�����ʵ���Ũ�ȣ�c���ף�=c��������c������ | ||
| C�� | �ס����е�ƽ�ⳣ����K���ף�=K���ң�=400 | D�� | �������е�ƽ�ⳣ����K��������K������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʱ�� | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| c��X��/mol•L-1 | 0.2 | c | 0.6 | 0.6 | 1.0 | c1 | c1 |
| c��Y��/mol•L-1 | 0.6 | c | 0.4 | 0.4 | 0.4 | c2 | c2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | CH3OH | CH3OCH3 | H2O |
| c/��mol•L-1�� | 0.8 | 1.24 | 1.24 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �÷�Ӧ����������ԭ��Ӧ | B�� | ����ֻ���������� | ||
| C�� | N2O4�ǻ�ԭ�� | D�� | N2O4�������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com