
”¾ĢāÄæ”æNH4HSO4 ŌŚ·ÖĪöŹŌ¼Į”¢Ņ½Ņ©”¢µē×Ó¹¤ŅµÖŠÓĆĶ¾¹ć·ŗ”£ŹŅĪĀŹ±£¬Ļņ100mL0.lmol”¤L-1 NH4HSO4 ČÜŅŗÖŠµĪ¼Ó0.1mol”¤L-1NaOHČÜŅŗ£¬µĆµ½µÄČÜŅŗpH ÓėNaOH ČÜŅŗĢå»żµÄ¹ŲĻµĒśĻßČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
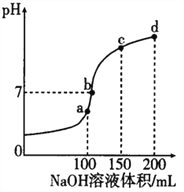
A. aµćČÜŅŗÖŠ£ŗc(NH4+)+c(H+)=c(Na+) +c(OH-)
B. CµćČÜŅŗÖŠ£ŗc(SO42-)>c(NH3”¤H2O)>c(NH4+)
C. dµćČÜŅŗÖŠ£ŗc(SO42-) >c(OH-)>c(NH4+)
D. a”¢b”¢c”¢d ĖÄøöµćÖŠ£¬bµćĖ®µÄµēĄė³Ģ¶Č×ī“ó
”¾“š°ø”æAC
”¾½āĪö”æ
A.aµćČÜŅŗĻŌĖįŠŌNH4HSO4+NaOH= NaNH4 SO4+H2O 100mL0.lmol”¤L-1 NH4HSO4 ČÜŅŗÖŠµĪ¼Ó0.1mol”¤L-1NaOHČÜŅŗ100mL£¬Ē”ŗĆĶźČ«·“Ó¦£¬NH4+·¢ÉśĖ®½ā£¬ĖłŅŌĻŌĖįŠŌc(NH4+)+c(H+)+c(Na+) =c(OH-)+2 c(SO42-)£¬øł¾ŻĪļĮĻŹŲŗćc(Na+)= c(SO42-)£¬ĖłŅŌÉĻŹöŹ½×ÓæÉŅŌŠ“³Éc(NH4+)+c(H+)=c(Na+) +c(OH-) ¹ŹA¶Ō£»B. CµćČÜŅŗÖŠŗ¬ÓŠĮņĖįÄĘ£¬ĮņĖįļ§ŗĶ°±Ė®£¬ŅņĪŖ°±Ė®µÄµēĄė³Ģ¶Č“óÓŚļ§øłĄė×ÓµÄĖ®½ā³Ģ¶Č£¬c(SO42-)> c(NH4+)> c(NH3”¤H2O)£¬¹ŹB“ķ£»
C. dµćČÜŅŗÖŠĮņĖįÄĘ£¬ĒāŃõ»ÆÄĘŗĶ°±Ė®£ŗc(SO42-) >c(OH-)>c(NH4+)¹ŹÕżČ·£»D.ŅņĪŖ¼ÓĖįŗĶ¼īŅÖÖĘĖ®µÄµēĄė£¬Ė®½ā“Ł½ųµēĄė£¬ĖłŅŌ ŹÜµÄa”¢b”¢c”¢d ĖÄøöµćÖŠ£¬aµćĖ®µÄµēĄė³Ģ¶Č×ī“ó.¹ŹD“ķ”£


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ°Ń5.6gµÄFe·ÅČė×ćĮæĻ”ĮņĖįÖŠ£¬FeĶźČ«·“Ó¦”£¼ĘĖć£ŗ
£Ø1£©5.6gFeµÄĪļÖŹµÄĮæ_________£»
£Ø2£©Éś³ÉH2µÄĢå»ż£Ø±ź×¼×“æö£©_________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫ÅØ¶Č¾łĪŖ0.01 mol/L µÄH2O2”¢H2SO4”¢KI”¢Na2S2O3ČÜŅŗ¼°µķ·Ū»ģŗĻ£¬Ņ»¶ØŹ±¼äŗóČÜŅŗ±äĪŖĄ¶É«”£øĆŹµŃéŹĒŅ»ÖÖ”°µāÖÓŹµŃé”±”£Ä³Š”×éĶ¬Ń§ŌŚŹŅĪĀĻĀ¶ŌøĆ”°µāÖÓŹµŃé”±µÄŌĄķ½ųŠŠĢ½¾æ”£
£Ø׏ĮĻ£©
øĆ”°µāÖÓŹµŃé”±µÄ×Ü·“Ó¦£ŗH2O2 +2S2O32-+2H+=S4O62-+2H2O
·“Ó¦·ÖĮ½²½½ųŠŠ£ŗ
·“Ó¦A£ŗH2O2+2I-+2H£«=I2+2H2O
·“Ó¦B£ŗ””
(1)·“Ó¦BµÄĄė×Ó·½³ĢŹ½ŹĒ______”£¶ŌÓŚ×Ü·“Ó¦£¬I-µÄ×÷ÓĆĻąµ±ÓŚ______”£
(2)ĪŖÖ¤Ć÷·“Ó¦A”¢BµÄ“ęŌŚ£¬½ųŠŠŹµŃé¢ń”£
a.ĻņĖį»ÆµÄH2O2ČÜŅŗÖŠ¼ÓČėŹŌ¼ĮXµÄĖ®ČÜŅŗ£¬ČÜŅŗ±äĪŖĄ¶É«”£
b.ŌŁĻņµĆµ½µÄĄ¶É«ČÜŅŗÖŠ¼ÓČėNa2S2O3ČÜŅŗ£¬ČÜŅŗµÄĄ¶É«ĶŹČ„”£
ŹŌ¼ĮXŹĒ______”£
(3)ĪŖĢ½¾æČÜŅŗ±äĄ¶æģĀżµÄÓ°ĻģŅņĖŲ£¬½ųŠŠŹµŃé¢ņ”¢ŹµŃé¢ó”££ØČÜŅŗÅØ¶Č¾łĪŖ0.01 mol/L£©
ŹŌ¼Į ŠņŗÅ ÓĆĮæ£ØmL£© | H2O2 ČÜŅŗ | H2SO4 ČÜŅŗ | Na2S2O3 ČÜŅŗ | KIČÜŅŗ (ŗ¬µķ·Ū) | H2O |
ŹµŃé¢ņ | 5 | 4 | 8 | 3 | 0 |
ŹµŃé¢ó | 5 | 2 | x | y | z |
ČÜŅŗ“Ó»ģŗĻŹ±µÄĪŽÉ«±äĪŖĄ¶É«µÄŹ±¼ä£ŗŹµŃé¢ņŹĒ30 min”¢ŹµŃé¢óŹĒ40 min”£
¢ŁŹµŃé¢óÖŠ£¬x”¢y”¢zĖł¶ŌÓ¦µÄŹżÖµ·Ö±šŹĒ______”£
¢Ś¶Ō±ČŹµŃé¢ņ”¢ŹµŃé¢ó£¬æÉµĆ³öµÄŹµŃé½įĀŪŹĒ______”£
(4)ĪŖĢ½¾æĘäĖūŅņĖŲ¶ŌøĆ”°µāÖÓŹµŃé”±µÄÓ°Ļģ£¬½ųŠŠŹµŃé¢ō”£
£ØČÜŅŗÅØ¶Č¾łĪŖ0.01 mol/L£©
ŹŌ¼Į ŠņŗÅ ÓĆĮæ£ØmL£© | H2O2 ČÜŅŗ | H2SO4 ČÜŅŗ | Na2S2O3 ČÜŅŗ | KIČÜŅŗ(ŗ¬µķ·Ū) | H2O |
ŹµŃé¢ō | 4 | 4 | 9 | 3 | 0 |
ŹµŃé¹ż³ĢÖŠ£¬ČÜŅŗŹ¼ÖÕĪŽĆ÷ĻŌŃÕÉ«±ä»Æ”£
ŹŌ½įŗĻøĆ”°µāÖÓŹµŃé”±×Ü·“Ó¦·½³ĢŹ½¼°·“Ó¦AÓė·“Ó¦BĖŁĀŹµÄĻą¶ŌæģĀż¹ŲĻµ£¬½āŹĶŹµŃé¢ōĪ“²śÉśŃÕÉ«±ä»ÆµÄŌŅņ£ŗ_____________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æKNO3ŹĒÖŲŅŖµÄ»Æ¹¤²śĘ·£¬ĻĀĆęŹĒŅ»ÖÖŅŃ»ńµĆ×ØĄūµÄKNO3Öʱø·½·ØµÄÖ÷ŅŖ²½Öč£ŗ
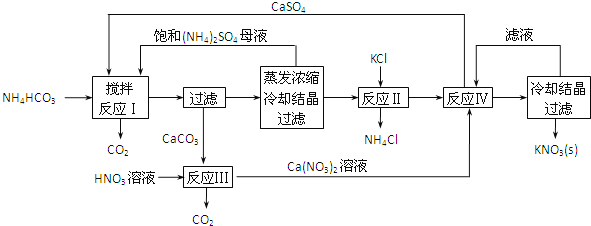
£Ø1£©·“Ó¦¢ńÖŠ£¬CaSO4ÓėNH4HCO3µÄĪļÖŹµÄĮæÖ®±ČĪŖ1:2£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ____________”£
£Ø2£©·“Ó¦¢ņŠčŌŚøÉĢ¬”¢¼ÓČȵÄĢõ¼žĻĀ½ųŠŠ£¬¼ÓČȵÄÄæµÄŹĒ____________£»“Ó·“Ó¦¢ōĖłµĆ»ģŗĻĪļÖŠ·ÖĄė³öCaSO4µÄ·½·ØŹĒ³ĆČČ¹żĀĖ£¬³ĆČČ¹żĀĖµÄÄæµÄŹĒ____________”£
£Ø3£©¼ģŃé·“Ó¦¢ņĖłµĆK2SO4ÖŠŹĒ·ń»ģÓŠKClµÄ·½·ØŹĒ£ŗȔɣĮæK2SO4ѳʷČܽāÓŚĖ®£¬____________”£
£Ø4£©ÕūøöĮ÷³ĢÖŠ£¬æÉŃ»·ĄūÓƵÄĪļÖŹ³ż(NH4)2SO4Ķā£¬»¹ÓŠ____________(Ģī»ÆѧŹ½)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijŗćČŻĆܱÕČŻĘ÷ÖŠ³äČėµČĪļÖŹµÄĮæµÄA ŗĶB£¬Ņ»¶ØĪĀ¶ČĻĀ·¢Éś·“Ó¦A(g)+xB(g)![]() 2C(g)£¬“ļµ½Ę½ŗāŗó£¬ŌŚ²»Ķ¬µÄŹ±¼ä¶Ī£¬·Ö±šøıäÓ°Ļģ·“Ó¦µÄŅ»øöĢõ¼ž£¬²āµĆČŻĘ÷ÖŠĪļÖŹµÄĪļÖŹµÄĮæÅØ¶Č”¢·“Ó¦ĖŁĀŹ·Ö±šĖꏱ¼äµÄ±ä»ÆČēĶ¼ĖłŹ¾£ŗ
2C(g)£¬“ļµ½Ę½ŗāŗó£¬ŌŚ²»Ķ¬µÄŹ±¼ä¶Ī£¬·Ö±šøıäÓ°Ļģ·“Ó¦µÄŅ»øöĢõ¼ž£¬²āµĆČŻĘ÷ÖŠĪļÖŹµÄĪļÖŹµÄĮæÅØ¶Č”¢·“Ó¦ĖŁĀŹ·Ö±šĖꏱ¼äµÄ±ä»ÆČēĶ¼ĖłŹ¾£ŗ

ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
A. 30 min”«40 min Ö®¼äøĆ·“Ó¦Ź¹ÓĆĮĖ“߻ƼĮ
B. ·“Ó¦·½³ĢŹ½ÖŠµÄx=2£¬Õż·“Ó¦ĪŖĪüČČ·“Ó¦
C. 30 min Ź±Ģõ¼žµÄ±ä»ÆŹĒ½µµĶŃ¹Ē棬40 min Ź±Ģõ¼žµÄ±ä»ÆŹĒÉżøßĪĀ¶Č
D. Ē°20 min A µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0.08 molL©1min©1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ£ŗP4(g)£«6Cl2(g) ![]() 4PCl3(g) ¦¤H£½a kJ”¤mol£1£¬P4(g)£«10Cl2(g)
4PCl3(g) ¦¤H£½a kJ”¤mol£1£¬P4(g)£«10Cl2(g) ![]() 4PCl5(g) ¦¤H£½b kJ”¤mol£1£¬P4¾ßÓŠÕżĖÄĆęĢå½į¹¹£¬PCl5ÖŠP”ŖCl¼üµÄ¼üÄÜĪŖc kJ”¤mol£1£¬PCl3ÖŠP”ŖCl¼üµÄ¼üÄÜĪŖ 1.2c kJ”¤mol£1”£
4PCl5(g) ¦¤H£½b kJ”¤mol£1£¬P4¾ßÓŠÕżĖÄĆęĢå½į¹¹£¬PCl5ÖŠP”ŖCl¼üµÄ¼üÄÜĪŖc kJ”¤mol£1£¬PCl3ÖŠP”ŖCl¼üµÄ¼üÄÜĪŖ 1.2c kJ”¤mol£1”£
ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A. PCl3±ČPCl5ĪȶØ
B. æÉĒóCl2(g)£«PCl3(g) ![]() PCl5(s)µÄ·“Ó¦ČȦ¤H
PCl5(s)µÄ·“Ó¦ČȦ¤H
C. Cl”ŖCl¼üµÄ¼üÄÜĪŖ(b £a£«5.6c)/4 kJ”¤mol£1
D. P”ŖP¼üµÄ¼üÄÜĪŖ(5a£3b£«12c)/8 kJ”¤mol£1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ1869Äź¶ķ¹ś»Æѧ¼ŅĆŽŻĮŠ·ņÖĘ³öµŚŅ»ÕÅŌŖĖŲÖÜĘŚ±ķ£¬µ½ĻÖŌŚŠĪ³ÉµÄÖÜĘŚ±ķ¾¹żĮĖÖŚ¶ą»Æѧ¼ŅµÄ¼čŠĮŬĮ¦£¬Ąś¾150Äź”£ŌŖĖŲÖÜĘŚ±ķĢåĻÖĮĖŌŖĖŲĪ»”¢¹¹”¢ŠŌµÄ¹ŲĻµ£¬½ŅŹ¾ĮĖŌŖĖŲ¼äµÄÄŚŌŚĮŖĻµ”£ĻĀ±ķŹĒŌŖĖŲÖÜĘŚ±ķµÄŅ»²æ·Ö£¬Õė¶Ō±ķÖŠµÄ¢Ł”«¢āÖŠŌŖĖŲ£¬ÓĆŌŖĖŲ·ūŗÅ»ņ»ÆѧŹ½ĢīæÕ»Ų“šŅŌĻĀĪŹĢā£ŗ
Ö÷×å ÖÜĘŚ | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ¢Ł | ¢Ś | ||||||
3 | ¢Ū | ¢Ü | ¢Ż | ¢Ž | ¢ß | ¢ą | ¢į | |
4 | ¢ā |
£Ø1£©±ķÖŠ»ÆѧŠŌÖŹ×ī²»»īĘƵÄŌŖĖŲ£¬ĘäŌ×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ___£»
£Ø2£©ŌŖĖŲ¢ŁµÄµ„ÖŹµē×ÓŹ½ĪŖ____”£
£Ø3£©±Č½Ļ¢Ū”¢¢ŻŌŖĖŲµÄ½šŹōŠŌĒæČõ___>___£»²¢Š“³öĖüĆĒ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļ¼ä·“Ó¦µÄ»Æѧ·½³ĢŹ½____”£
£Ø4£©ÉĻŹöŌŖĖŲµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļÖŠ£¬ĖįŠŌ×īĒæµÄŹĒ____”£
£Ø5£©ŌŚŌŖĖŲ¢Ū”¢¢Ü”¢¢Ż”¢¢ß”¢¢ąŠĪ³ÉµÄ¼ņµ„Ąė×ÓÖŠ£¬°ė¾¶×īŠ”µÄŹĒ_____£»
£Ø6£©¹¤ŅµÖĘČ”¢ŽµÄµ„ÖŹµÄ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¢ń£®Ä³ŃŠ¾æŠŌѧĻ°×éĄūÓĆH2C2O4ČÜŅŗŗĶĖįŠŌKMnO4ČÜŅŗÖ®¼äµÄ·“Ó¦Ą“Ģ½¾æ”°Ķā½ēĢõ¼žøıä¶Ō»Æѧ·“Ó¦ĖŁĀŹµÄÓ°Ļģ”±£¬ŹµŃéČēĻĀ£ŗ
ŹµŃéŠņŗÅ | ŹµŃéĪĀ¶Č | KMnO4ČÜŅŗ | H2C2O4ČÜŅŗ | H2O | ČÜŅŗĶŹÉ«Ź±¼ä | ||
V(mL) | C(mol/L) | V(mL) | C(mol/L) | V(mL) | t(s) | ||
A | 293K | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
C | 313K | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
£Ø1£©ĶعżŹµŃéA”¢B£¬æÉĢ½¾æ³ö_______µÄøıä¶Ō·“Ó¦ĖŁĀŹµÄÓ°Ļģ£¬ĘäÖŠV1=_____£¬T1=_____£¬ĶعżŹµŃé_______æÉĢ½¾æ³öĪĀ¶Č±ä»Æ¶Ō»Æѧ·“Ó¦ĖŁĀŹµÄÓ°Ļģ”£
£Ø2£©Čōt1£¼8£¬ŌņÓÉŹµŃéA”¢BæÉŅŌµĆ³öµÄ½įĀŪŹĒ________________________span>£»ĄūÓĆŹµŃéBÖŠŹż¾Ż¼ĘĖć£¬“Ó·“Ó¦æŖŹ¼µ½ÓŠ½įŹų£¬ÓĆKMnO4µÄÅØ¶Č±ä»Æ±ķŹ¾µÄ·“Ó¦ĖŁĀŹĪŖ____________”£
£Ø3£©øĆ·“Ó¦ÖŠÓŠĪŽÉ«ĪŽĪ¶ĘųĢå²śÉś£¬ĒŅĆĢ±»»¹ŌĪŖMn2+£¬Š“³öĻąÓ¦·“Ó¦µÄĄė×Ó·½³ĢŹ½_______”£
£Ø4£©øĆŠ”×éµÄŅ»Ī»Ķ¬Ń§Ķعż²éŌÄ׏ĮĻ·¢ĻÖ£ŗ·“Ó¦Ņ»¶ĪŹ±¼äŗóøĆ·“Ó¦ĖŁĀŹ»į¼Óæģ£¬Ōģ³É“ĖÖÖ±ä»ÆµÄŌŅņŹĒ·“Ó¦ĢåĻµÖŠµÄijÖÖĮ£×Ó¶ŌKMnO4ÓėH2C2O4Ö®¼äµÄ·“ӦӊijÖÖĢŲŹāµÄ×÷ÓĆ£¬ŌņøĆ×÷ÓĆŹĒ_______________£¬ĻąÓ¦µÄĮ£×Ó×īÓŠæÉÄÜŹĒ£ØĢī·ūŗÅ£©_______”£
II.100kPaŹ±£¬·“Ó¦2NO(g)+O2(g)![]() 2NO2(g)ÖŠNOµÄĘ½ŗā×Ŗ»ÆĀŹÓėĪĀ¶ČµÄ¹ŲĻµĒśĻßČēĶ¼1£¬·“Ó¦2NO2(g)
2NO2(g)ÖŠNOµÄĘ½ŗā×Ŗ»ÆĀŹÓėĪĀ¶ČµÄ¹ŲĻµĒśĻßČēĶ¼1£¬·“Ó¦2NO2(g)![]() N2O4(g)ÖŠNO2µÄĘ½ŗā×Ŗ»ÆĀŹÓėĪĀ¶ČµÄ¹ŲĻµĒśĻßČēĶ¼2”£
N2O4(g)ÖŠNO2µÄĘ½ŗā×Ŗ»ÆĀŹÓėĪĀ¶ČµÄ¹ŲĻµĒśĻßČēĶ¼2”£
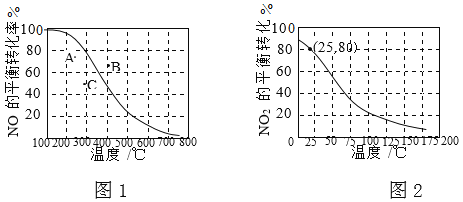
¢Ł Ķ¼1ÖŠA”¢B”¢CČżµć±ķŹ¾²»Ķ¬ĪĀ¶Č”¢Ń¹ĒæĻĀ2NO(g)+O2(g)![]() 2NO2(g)“ļµ½Ę½ŗāŹ±NOµÄ×Ŗ»ÆĀŹ£¬Ōņ________µć¶ŌÓ¦µÄŃ¹Ēæ×ī“ó”£
2NO2(g)“ļµ½Ę½ŗāŹ±NOµÄ×Ŗ»ÆĀŹ£¬Ōņ________µć¶ŌÓ¦µÄŃ¹Ēæ×ī“ó”£
¢Ś 100kPa”¢25”ꏱ£¬2NO2(g)![]() N2O4(g)Ę½ŗāĢåĻµÖŠ£¬ĮŠŹ½¼ĘĖćĘ½ŗā³£ŹżKp£½________”££ØKpÓĆĘ½ŗā·ÖŃ¹“śĢęĘ½ŗāÅØ¶Č¼ĘĖć£¬·ÖŃ¹£½×ÜŃ¹”ĮĪļÖŹµÄĮæ·ÖŹż£©
N2O4(g)Ę½ŗāĢåĻµÖŠ£¬ĮŠŹ½¼ĘĖćĘ½ŗā³£ŹżKp£½________”££ØKpÓĆĘ½ŗā·ÖŃ¹“śĢęĘ½ŗāÅØ¶Č¼ĘĖć£¬·ÖŃ¹£½×ÜŃ¹”ĮĪļÖŹµÄĮæ·ÖŹż£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijČÜŅŗÖŠŗ¬ÓŠSO42-”¢SO32-”¢HCO3-”¢CO32-µČĖÄÖÖĄė×Ó”£½«¹żĮæµÄNa2O2¹ĢĢå¼ÓČėĘäÖŠŗó£¬ČŌÄÜ“óĮæ“ęŌŚµÄĄė×ÓŹĒ£Ø £©
A.SO42-ӢHCO3-B.SO42-ӢSO32-ӢCO32-
C.SO32-ӢHCO3-D.SO42-ӢCO32-
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com