
����Ŀ���ǽ�������A����ͼ��ʾ�Ĺ���ת��Ϊ������D����֪DΪǿ�ᣬ��ش��������⡣
![]()
![]()
![]()
![]()
![]()
![]()
![]()
��1����A�ڳ�����Ϊ���壬B����ʹƷ����Һ��ɫ���д̼�����ζ����ɫ����:
��D�Ļ�ѧʽ��________��
���ڹ�ҵ�����У�B����Ĵ����ŷű���ˮ���պ��γ���________����Ⱦ�˻�����
��2����A�ڳ�����Ϊ���壬C�Ǻ���ɫ������:
��A��C�Ļ�ѧʽ�ֱ��ǣ�A________��C________��
��D��Ũ��Һ�ڳ����¿���ͭ��Ӧ������C���壬��д���÷�Ӧ�Ļ�ѧ����ʽ_______________________________________________���÷�Ӧ________(����������������������)������ԭ��Ӧ��
���𰸡� H2SO4 ���� N2 NO2 Cu��4HNO3(Ũ)===Cu(NO3)2��2NO2����2H2O ����
���������ǽ�������A��ת��Ϊ������D��DΪǿ�ᣬB��C�����������AԪ��Ϊ�ɱ��Ԫ�أ�����������Ԫ����S��NԪ�أ���A�ǵ��������ʡ�(1)��A�ڳ�����Ϊ���壬��A��S���ʣ�B����ʹƷ����Һ��ɫ���д̼�����ζ����ɫ���壬��B��SO2����������������������������C��SO3�����������ˮ��Ӧ�������ᣬ��D��H2SO4����ͨ�����Ϸ���֪��D�����ᣬ�仯ѧʽΪ��H2SO4����B�Ƕ��������������ˮ��Ӧ���������ᣬ������ȶ��ױ������������ᣬ������Һ�����ԣ���ˮ�к���������γ����ꣻ(2)��A�ڳ�����Ϊ���壬C�Ǻ���ɫ���壬��A��N2��C��NO2��B��NO��D��HNO3����ͨ�����Ϸ���֪��A��C�Ļ�ѧʽ�ֱ��ǣ�N2��NO2���ڳ����£�ͭ��Ũ���ᷴӦ��������ͭ������������ˮ����Ӧ����ʽΪCu��4HNO3(Ũ)��Cu(NO3)2��2NO2����2H2O����Ӧ��ͭ�͵�Ԫ�ػ��ϼ۱仯������������ԭ��Ӧ��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л����������ȷ���ǣ�������
A.�Ҵ����ܷ���ȡ����Ӧ
B.C4H10������ͬ���칹��
C.�����ᡢ���۾����ڸ߷��ӻ�����
D.��ϩ�ͼ������������Ȼ�̼��Һ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������һ�ֵ����ǵ�ֽ���װ��ӡ����ͼ��ʾ�����֣�����Ҫ��ش�
��1���õ�ص�������______������ţ���
�ٸɵ�� ������ ��ȼ�ϵ��
��2���õ�غ��еĽ���Ԫ����������������______��дԪ�ط��ţ���
��3���õ�ص�ʹ�ú����ܣ�����˵���в���ȷ����______
A���õ�ؿ�Ӧ�������ӡ����������������
B���õ�ؿɳ���ʹ��
C���õ��ʹ�ú���Ͷ����У�Ӧ��������Է���Ⱦ����
��4����֪�õ�ص��ܷ�ӦΪ��Zn+2MnO2+2NH4Cl��ZnCl2+2NH3��+Mn2O3+H2O��д���õ�طŵ�ʱ����������Ӧ����ʽ��
����___________________________________
����___________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�������ʾ��ͼһ�µ��ǣ� ��
A.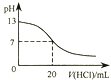
ͼ��ʾ25��ʱ����0.1 molL��1����ζ�20 mL 0.1 molL��1 NaOH��Һ����Һ��pH�����������ı仯
B.
ͼ�����߱�ʾ��Ӧ2SO2��g��+O2��g���T2SO3��g������H��0 �����淴Ӧ��ƽ�ⳣ��K���¶ȵı仯
C.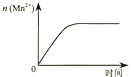
ͼ�۱�ʾ10 mL 0.01 molL��1 KMnO4 ������Һ�������0.1 molL��1 H2C2O4��Һ���ʱ��n��Mn2+�� ��ʱ��ı仯
D.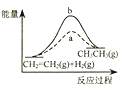
ͼ��a��b���߷ֱ��ʾ��ӦCH2=CH2 ��g��+H2��g����CH3CH3��g������H��0ʹ�ú�δʹ�ô���ʱ����Ӧ�����е������仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������֪34Se��ԭ�ӽṹʾ��ͼ��ͼ��ʾ���ش��������⣺

��1��Se��Ԫ�����ڱ��е�λ����__________��
��2����Se�����ڱ��е�λ�÷����ж�����˵����ȷ����__________��
A�����ȶ��ԣ�PH3>H2S>H2Se B����ԭ�ԣ�H2Se>HBr>HCl
C�����Ӱ뾶��Se2->Cl->K+ D�����ԣ�HClO3>HBrO3>H2SeO3
�����¶�t1��t2�£�X2(g)��H2��Ӧ����HX��ƽ�ⳣ�����±���
��ѧ����ʽ | K(t1) | K(t2) |
F2+H2===2HF | 1.8��1036 | 1.9��1032 |
Cl2+H2===2HCl | 9.7��1012 | 4.2��1011 |
Br2+H2===2HBr | 5.6��107 | 9.3��106 |
I2+H2===2HI | 43 | 34 |
��1����֪��HX�����ɷ�Ӧ�Ƿ��ȷ�Ӧ�����¶�t2__________t1���<����>������
��2���õ���ʽ��ʾHX���γɹ���__________��
��3�����ۼ��ļ����湲�õ��Ӷ�ƫ�Ƴ̶ȵ��������ǿ��HX���ۼ��ļ�����ǿ������˳����__________��
��4��X2������H2��Ӧ����HX����ԭ�ӽṹ����ԭ��__________��
��5��K�ı仯���ֳ�X2��ѧ���ʵĵݱ��ԣ���ԭ�ӽṹ����ԭ��__________��ԭ�Ӱ뾶�����õ�������������
��6��������K�ı仯�������ƶϳ�������±��ԭ�Ӻ˵���������ӣ�__________��ѡ����ĸ����
a������ͬ�����£�ƽ��ʱX2��ת�������� b��HX���ȶ�������
c��X2��H2��Ӧ�ľ��ҳ̶����� d��HX�Ļ�ԭ������
��7����ͬ±��ԭ��֮����γ�±�ػ������������±�ص��������д��BrCl��SO2��ˮ��Һ�з�����Ӧ�Ļ�ѧ����ʽ__________��
���𰸡� ��4���ڵڢ�A�� BC > ![]() HF��HCl��HBr��HI ±��ԭ�ӵ���������������7 ͬһ����Ԫ�ش�������ԭ�Ӻ�����Ӳ����������� ab BrCl+SO2+2H2O=H2SO4+HCl+HBr
HF��HCl��HBr��HI ±��ԭ�ӵ���������������7 ͬһ����Ԫ�ش�������ԭ�Ӻ�����Ӳ����������� ab BrCl+SO2+2H2O=H2SO4+HCl+HBr
��������I.(1). ����Se��ԭ�ӽṹʾ��ͼ��֪��Se���ĸ����Ӳ㣬�������6�����ӣ�����Ӳ�������������������������������������������SeԪ��λ��Ԫ�����ڱ��ĵ�4���ڵ�VIA�壬�ʴ�Ϊ����4���ڵ�VIA����
(2) A. ͬһ���ڴ�����Ԫ�صķǽ���������ǿ��ͬһ������ϵ���Ԫ�صķǽ�������������ǽ�����S��P��S��Se������Ԫ�صķǽ�����Խǿ������̬�⻯�����ȶ���Խǿ���������ȶ���H2S��PH3��H2S��H2Se����A����B. �ǽ�����Cl��Br��Se����ǽ�����Խǿ�����Ӧ�����ӵĻ�ԭ��Խ������ԭ�ԣ�H2Se>HBr>HCl����B��ȷ��C. ���Ӳ���Խ�࣬���Ӱ뾶Խ�������Ӱ뾶Se2->Cl-��������ͬ��������Ų������ӣ�ԭ������Խ�����Ӱ뾶ԽС�������Ӱ뾶Cl->K+���������Ӱ뾶��Se2->Cl->K+����C��ȷ��D. ����������Ӧ��ˮ��������Խǿ��Ԫ�صķǽ�����Խǿ����HClO3��HBrO3��H2SeO3�����Ǹ�Ԫ�ص�����������Ӧ��ˮ����������Ƚ�����ǿ������D����ѡBC��
II. (1). ��HX�����ɷ�Ӧ�Ƿ��ȷ�Ӧ���������¶ȣ�ƽ�������ƶ���ƽ�ⳣ����С���ɱ������ݿ�֪��K(t1)��K(t2)��˵��t2��t1���ʴ�Ϊ������
(2). ��HX���ǹ��ۻ������ԭ������������Xԭ�����������γ�һ�Թ��õ��Ӷԣ����γɹ��̿ɱ�ʾΪ��![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
(3). F��Cl��Br��I���ڢ�A��Ԫ�أ�ͬ����Ԫ�����϶������ź˵����������ԭ�Ӻ�����Ӳ��������࣬����ԭ�Ӱ뾶���������ԭ�Ӻ˶��������ӵ��������������Ӷ����·ǽ�������������������Ԫ�صõ����ӵ���������������HF���ļ�����ǿ��HI�ļ������������HX���ۼ��ļ�����ǿ������˳����HF��HCl��HBr��HI���ʴ�Ϊ��HF��HCl��HBr��HI��
(4). ±��ԭ�ӵ�������������Ϊ7�����ڷ�Ӧ�о��õ�1�����Ӷ��ﵽ8���ӵ��ȶ��ṹ����Hԭ���������һ�����ӣ��ڷ�Ӧ��Ҳ�ܵõ�1�����Ӷ��ﵽ2���ӵ��ȶ��ṹ�����±�ص�������������ʱ��ͨ��һ�Թ��õ��Ӷ��γɻ�����HX���ʴ�Ϊ��±��ԭ�ӵ���������������7��
(5). ƽ�ⳣ��Խ��˵����ӦԽ���У�F. Cl��Br��I�ĵõ����������μ�С����Ҫԭ���ǣ�ͬһ����Ԫ�ش�������ԭ�Ӻ�����Ӳ����������࣬ԭ�Ӱ뾶�����õ�������������ɵģ��ʴ�Ϊ��ͬһ����Ԫ�ش�������ԭ�Ӻ�����Ӳ�������������
(6). a. KֵԽ��˵����Ӧ������̶�Խ��ת����Խ�ߣ���a��ȷ��b. ��Ӧ������̶�ԽС��˵��������Խ���ȶ�����b��ȷ����ѡ��c��d����K�Ĵ�С��ֱ�ӹ�ϵ����c��d����ѡab��
(7). ��ͬ±��ԭ��֮����γ�±�ػ������������±�ص�������������������������Ӧ����HCl�������ԭ�������ƶ�BrCl��SO2��ˮ��Һ�з�����Ӧ�Ļ�ѧ����ʽΪ��BrCl+SO2+2H2O=H2SO4+HCl+HBr���ʴ�Ϊ��BrCl+SO2+2H2O=H2SO4+HCl+HBr��
�����͡�������
��������
16
����Ŀ��CH4��������CO2�����ɵõ�����CO�����壬�����������ֻ�����Ʒ���ü����еĻ�ѧ��ӦΪ��CH4(g)+3CO2(g) ![]() 2H2O(g)+4CO(g) ��H=+330kJ/mol
2H2O(g)+4CO(g) ��H=+330kJ/mol
��1����ͼ��ʾ��ʼͶ�ϱ�n(CH4):n(CO2)Ϊ1:3��1:4��CH4��ת�����ڲ�ͬ�¶ȣ�T1��T2������ѹǿ�Ĺ�ϵ��[ע��Ͷ�ϱ���a1��a2��ʾ]
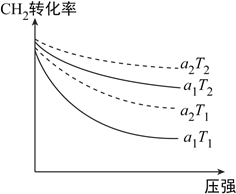
��a2=__________��
���ж�T1��T2�Ĵ�С��ϵ����˵�����ɣ�__________��
��2��CH4��������CO2�Ĵ�ת��ԭ��ʾ��ͼ���£�

�ٹ��̢�����1mol H2ʱ����123.5kJ���������Ȼ�ѧ����ʽ��__________��
�ڹ��̢�ʵ���˺��������뺬̼���ֵķ��롣����H2O(g)�Ļ�ѧ����ʽ��__________��
�ۼ�����̢���̢��еĸ�����ת����ȫ������˵����ȷ����__________��������ţ�
a�����̢���̢��з�����������ԭ��Ӧ
b�����̢���ʹ�õĴ���ΪFe3O4��CaCO3
c�������̢�Ͷ��![]() ���ɵ��¹��̢��д���ʧЧ
���ɵ��¹��̢��д���ʧЧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��CΪ������Ԫ�أ�ԭ���������μ�С��A��������ϼ�Ϊ��2����������ۣ�B�ǿ����к�����ߵ�Ԫ�أ�C��������������Ӳ�����ȣ��ش��������⣺
��1��A��B��C�ֱ�Ϊ��������Ԫ�����Ʊ�ʾ����
��2��������Ԫ����ɵĻ������У��������ӻ�������� �� ���ڹ��ۻ�������� �� ����дһ�ּ��ɣ�
��3��B�ij�����̬�⻯��ĵ���ʽΪ �� B�ij�����̬�⻯����������������Ӧ��ˮ���ﷴӦ����������Ӻ������ѧ�������ࣩ���������Ȼ����ˮ��Һ���ԣ������ӷ���ʽ��ʾΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������θ�����������ǣ� ��
A.��������B.�Ȼ���C.�Ȼ���D.��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I. ijʵ��С���H2O2�ķֽ���������̽�����±����о�Ӱ��H2O2�ֽ����ʵ�����ʱ��¼��һ�����ݣ���������ͬ��״̬��ͬ��MnO2�ֱ����ʢ��15 mL5%��H2O2��Һ�Ĵ��Թ��У����ô����ǵ�ľ�����ԣ�������£�
MnO2 | �����Թ���� | �۲��� | ��Ӧ��������ʱ�� |
��ĩ״ | ���� | ���ҷ�Ӧ�������ǵ�ľ����ȼ | 3.5min |
��״ | �� | ��Ӧ���������Ǻ�������ľ��δ��ȼ | 30min |
��1���÷�Ӧ��_________��Ӧ������Ȼ����ȣ���
��2��ʵ���������������Ĵ�Ч����_____________________�йء�
��ij���淴Ӧ�����Ϊ5L���ܱ������н��У��ڴ�0��3���Ӹ����ʵ����ʵ����仯�����ͼ��ʾ��A��B��C��Ϊ���壩��

��3���÷�Ӧ�ĵĻ�ѧ����ʽΪ_____________��
��4����Ӧ��ʼ��2����ʱ��B��ƽ����Ӧ����Ϊ__________��
��5����˵���÷�Ӧ�Ѵﵽƽ��״̬����_________��
A��v(A)= 2v(B) B��������ѹǿ���ֲ���
C��v��(A)= v��(C) D�������ڻ��������ܶȱ��ֲ���
��6����ͼ���A��ƽ��ʱ��ת����Ϊ__________��
��.��֪���Ͽ�1mol���ۼ����յ��������γ�1mol���ۼ��ͷŵ������������±���
���ۼ� | H��H | N��H | N��N |
�����仯/kJ��mol��1 | 436 | 390.8 | 946 |
��ϳɰ���Ӧ��N2(g) + 3H2(g)= 2NH3(g) ![]() H = ____________kJ��mol��1��
H = ____________kJ��mol��1��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com