
【题目】 研究碳及其化合物的相互转化对能源的充分利用、低碳经济有着重要的作用。
⑴已知:①CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H1=+206.1kJ·mol-1
CO(g)+3H2(g) △H1=+206.1kJ·mol-1
②2H2(g)+CO(g)![]() CH3OH(l) △H2=-128.3kJ·mol-1
CH3OH(l) △H2=-128.3kJ·mol-1
③2H2(g)+O2(g)![]() 2H2O(g) △H3=-483.6kJ·mol-1
2H2O(g) △H3=-483.6kJ·mol-1
25℃时,在合适的催化剂作用下,采用甲烷和氧气一步合成液态甲醇的热化学方程式为 。
⑵利用反应①来制备氢气,为了探究温度、压强对反应①速率、转化率的影响,某同学设计了以下三组对比实验(温度为400℃或500℃,压强为101kPa或404kPa)。
实验序号 | 温度℃ | 压强/kPa | CH4初始浓度/ mol·L-1 | H2O初始浓度/ mol·L-1 |
1 | 400 | p | 3.0 | 7.0 |
2 | t | 101 | 3.0 | 7.0 |
3 | 400 | 101 | 3.0 | 7.0 |
①实验2和实验3相比,其平衡常数关系是K2 K3(填“>”、“<”或“=”)。
②将等物质的量的CH4和水蒸气充入1L恒容密闭容器中,发生上述反应,在400℃下达到平衡,平衡常数K=27,此时容器中CO物质的量为0.10mol,则CH4的转化率为 。
⑶ 科学家提出由CO2制 取 C的太阳能工艺如图1所示。
①“重整系统发生的反应中n(FeO):n(CO2)=6:1,则Fe xOy的化学式为______________。
②“热分解系统”中每分解l mol Fe xOy,转移电子的物质的量为___________。
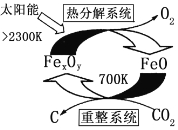

图1 图2
⑷pC类似pH,是指极稀溶液中的溶质浓度的常用负对数值。若某溶液中溶质的浓度为1×10-3mol·L-1,则该溶液中溶质的pC=-lg(1×10-3)=3。如图2为25℃时H2CO3溶液的pC-pH图。请回答下列问题 (若离子浓度小于10-5mol/L,可认为该离子不存在):
①在同一溶液中,H2CO3、HCO3-、CO32-____________(填“能”或“不能”)大量共存。
②求H2CO3一级电离平衡常数的数值Ka1=________________。
③人体血液里主要通过碳酸氢盐缓冲体系![]() 可以抵消少量酸或碱,维持pH=7.4。当过量的酸进入血液中时,血液缓冲体系中的
可以抵消少量酸或碱,维持pH=7.4。当过量的酸进入血液中时,血液缓冲体系中的![]() 最终将_________。
最终将_________。
A.变大 B.变小 C.基本不变 D.无法判断
【答案】
⑴CH4(g)+![]() O2(g)
O2(g)![]() CH3OH(l)△H1=-164.0kJ·mol-1
CH3OH(l)△H1=-164.0kJ·mol-1
⑵①>;②![]() (90.9%、90.91%、
(90.9%、90.91%、![]() ×100%均可)
×100%均可)
⑶①Fe3O4;②2mol
⑷①不能;②1×10-6;③A
【解析】
试题分析:⑴已知:①CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H1=+206.1kJ·mol-1,
CO(g)+3H2(g) △H1=+206.1kJ·mol-1,
②2H2(g)+CO(g)![]() CH3OH(l) △H2=-128.3kJ·mol-1,
CH3OH(l) △H2=-128.3kJ·mol-1,
③2H2(g)+O2(g)![]() 2H2O(g) △H3=-483.6kJ·mol-1,
2H2O(g) △H3=-483.6kJ·mol-1,
根据盖斯定律,将①+![]() ×③+②得:CH4(g)+
×③+②得:CH4(g)+ ![]() O2(g)
O2(g)![]() CH3OH(l)
CH3OH(l)
△H1=(+206.1kJ·mol-1)+![]() (-483.6kJ·mol-1)+(-128.3kJ·mol-1)=-164.0kJ·mol-1,
(-483.6kJ·mol-1)+(-128.3kJ·mol-1)=-164.0kJ·mol-1,
故答案为:CH4(g)+ ![]() O2(g)
O2(g)![]() CH3OH(l)△H1=-164.0kJ·mol-1;
CH3OH(l)△H1=-164.0kJ·mol-1;
⑵①对比实验2、3,只有温度不同,其它条件相同,所以实验2、3的目的是探究温度对化学反应速率的影响;实验1、3温度相同,平衡常数相同,即K1=K3,比较实验1、2,实验2中温度高,温度升高,平衡向吸热方向移动,该反应为吸热反应,所以平衡向正反应方向移动,平衡常数增大,即K2>K1,所以K2>K3,故答案为:>;
②依据化学平衡的三段式列式计算,设CH4与H2O(g)物质的量为a,
CH4(g)+H2O(g) ![]() CO(g)+3H2(g)
CO(g)+3H2(g)
起始量(mol) a a 0 0
变化量(mol) 0.10 0.10
平衡量(mol) a-0.10 a-0.10 0.10 0.30
由平衡常数表达式:K=![]() =
=![]() =27,
=27,
解之得:a=0.11,平衡转化率:![]() ×100%=90.9%;
×100%=90.9%;
⑶①由示意图可知,重整系统中CO2和FeO反应生成FexOy和C,发生的反应中n(FeO):n(CO2)=6,根据Fe原子、O原子守恒可知x:y=6:(6+2)=3:4,故FexOy的化学式为Fe3O4,故答案为:Fe3O4;
②热分解系统中是Fe3O4分解为FeO与氧气,分解l mol Fe3O4转移电子的物质的量为1mol×3×(![]() -2)=2mol,故答案为:2mol;
-2)=2mol,故答案为:2mol;
(4)①碳酸存在的溶液中酸性较强、碳酸根离子存在的溶液中碱性较强,所以碳酸根离子和碳酸不能大量共存,故答案为:不能;
②由图象可知当pH=6时,pC(H2CO3)=pC(HCO3-),结合Ka1(H2CO3)=![]() =
=![]() =10-6,故答案为:10-6;
=10-6,故答案为:10-6;
③氢离子浓度增大,平衡向左移动放出CO2,碳酸浓度基本不变,则c(H+)/c(H2CO3)最终将变大,故选A。


 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案科目:高中化学 来源: 题型:
【题目】铝硅合金材料性能优良。铝土矿(含30%SiO2、40.8% Al2O3、和少量的 Fe2O3等)干法制取该合金的工艺如下:
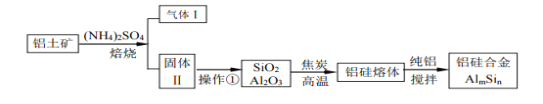
(1)铝硅合金中若含有铁,会影响其抗腐蚀性能,原因是_____________________
(2)焙烧除铁反应时,Fe2O3转化为NH4Fe(SO4 )2,Al2O3 少部分发生类似反应,写出Fe2O3反应的化学方程式:_____________________。氧化物转化为硫酸盐的百分率与温度的关系如图,最适宜的焙烧温度是________________
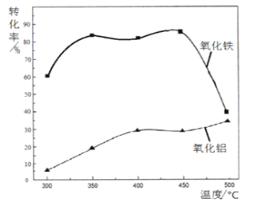
(3)若操作①所得的溶液中加入过量的NaOH溶液,含铝微粒发生的离子反应方程式是:_______________________。
(4)用焦炭还原SiO2、Al2O3会产生SiC等中间体。写出中间体SiC再与Al2O3生成硅、铝单质的化学反应方程式,_________________________。
(5)已知25℃ Ksp[Al(OH)3]=1.0×10-33 , Ksp[Fe(OH)3]=4.0×10-38,向FeCl3和AlCl3的混合溶液中逐滴滴入NaOH溶液,生成Al(OH)3和Fe(OH)3 沉淀,当两种沉淀共存时,上层清液中c(Al3+):c(Fe3+)==___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下图所示的物质转化关系中,A是常见的气态氢化物,其水溶液呈碱性,B是能使带火星的木条复燃的无色无味气体, G是一种红色金属单质。(部分反应中生成物没有全部列出,反应条件未列出)

请回答下列问题:
(1)反应①的化学方程式为 。当有1molA参加反应时,转移 mol电子。
(2)反应②的化学方程式为 。
(3)反应③的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱工业是以电解饱和食盐水为基础的基本化学工业。下图是某氯碱工业生产原理示意图:
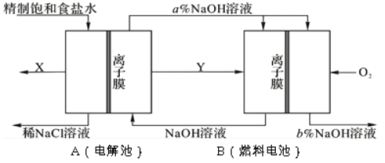
(1)写出装置A在通电条件下反应的化学方程式______________。
(2)A装置所用食盐水由粗盐水精制而成。精制时,为除去食盐水中的Mg2+和Ca2+,要加入的试剂分别为___________、___________。
(3)氯碱工业是高耗能产业,按上图将电解池与燃料电池相组合的新工艺可以节(电)能30%以上,且相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
①图中Y是______________(填化学式);X与稀NaOH溶液反应的离子方程式是:______________。
②分析比较图示中氢氧化钠质量分数a%与b%的大小___________。
③若用B装置作为A装置的辅助电源,每当消耗标准状况下氧气的体积为11.2 L时,则B装置可向A装置提供的电量约为______________(一个e-的电量为1.60×10-19C;计算结果精确到0.01)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与有机物的结构、性质有关的叙述正确的是( )
A.苯、油脂均不能使酸性KMnO4溶液褪色
B.甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应
C.葡萄糖、果糖的分子式均为C6 H12O6,二者互为同分异构体
D.乙醇、乙酸均能与Na反应放出H2,二者分子中官能团相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与有机物的结构、性质的有关叙述中正确的是( )
A.乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色
B.乙酸与乙醇可以发生酯化反应,又均可与金属钠发生置换反应
C.分馏、干馏都是物理变化,裂化、裂解都是化学变化
D.石油经过分馏得到多种烃,煤经过分馏可制得焦炭、煤焦油等产品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在373K时,把0.5molN2O4气体通入体积为5L(恒容)的真空密闭容器中,立即出现红棕色。反应进行到2s时,NO2的浓度为0.02mol·L-1。在60s时,体系已达到平衡,此时容器内压强为反应前的1.6倍。下列说法不正确的是( )
A.前2s,N2O4的平均反应速率为0.005mol·L-1·s-1
B.平衡时,N2O4的转化率为60%
C.平衡时,体系内NO2为0.04mol·L-1
D.在2s时,体系内压强为反应前的1.1倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)将锌片和银片用导线相连浸入稀硫酸中组成原电池。该电池中负极发生___________反应(填“氧化”或“还原”);溶液中的H+移向___________(填“正极”或“负极”)。若该电池中两电极的总质量为60 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质变质量为47 g,试计算产生氢气的体积(标准状况)___ ___________。
(2)现有反应2FeCl3+Cu===2FeCl2+CuCl2,请根据该反应的实质,设计成原电池,画出装置图并标出正、负极材料、电解质溶液 。
(3)实验室制备Fe(OH)2沉淀时,由于其在空气中极易发生反应______________.
(填化学方程式)而很难观察到沉淀的颜色。
为制得Fe(OH)2白色沉淀,有人设计了如右图所示的装置,用NaOH溶液、铁屑、稀H2SO4等试剂制备.实验时试管Ⅰ里应加入

(填试剂名称).在试管Ⅰ和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是_______ _.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com