
【题目】适量的下列四种物质①碘水 ②溴化钠溶液 ③新配制的氯水 ④氯化镁溶液,能使湿润的淀粉碘化钾试纸变蓝的组合是( )
A.①③B.②③C.②④D.①②③④
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式的书写及评价均合理的是( )
选项 | 离子方程式 | 评价 |
A | 将2 mol Cl2通入含1 mol FeI2的溶液中: 2Fe2++2I-+2Cl2===2Fe3++4Cl-+I2 | 正确;Cl2过量,可将Fe2+、I-均氧化 |
B | Ba(HCO3)2溶液与足量的NaOH溶液反应: Ba2++HCO3-+OH-===BaCO3↓+H2O | 正确;酸式盐与碱反应生成正盐和水 |
C | 过量SO2通入NaClO溶液中: SO2+H2O+ClO-===HClO+HSO3- | 正确;说明酸性:H2SO3强于HClO |
D | 1 mol/L的NaAlO2溶液和2.5 mol/L的HCl溶液等体积混合: 2AlO2-+5H+===Al3++Al(OH)3↓+H2O | 正确;第一步反应和第二步反应消耗的H+的物质的量之比为2∶3 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2O2具有强氧化性,可以用来漂白纺织类物品、麦杆、纤维等。
(1)如下图所示实验,反应的化学方程式为_______________。实验结束后,向试管所得溶液中滴加酚酞溶液,现象是___________________________。
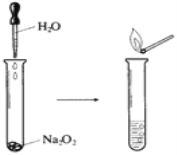
(2)若用嘴通过导管向附着少量Na2O2粉末的棉花吹气,棉花燃烧。原因是Na2O2与H2O和CO2反应,其中与CO2反应的化学方程式为______________________。若标准状况下反应生成了5.6LO2,则转移电子的物质的量为______mol。
过氧化钙(CaO2)是一种白色、无毒、难溶于水的固体,能杀菌消毒,广泛用于果蔬保鲜、空气净化、污水处理等方面。工业生产过程如下:
①在NH4Cl溶液中加入Ca(OH)2;
②在第①步的生成的产物中加入30%H2O2,反应生成CaO28H2O沉淀;
③经过陈化、过滤,水洗得到CaO28H2O,再脱水干燥得到CaO2。
完成下列填空:
(3)第①步反应的化学方程式为_____________________。
(4)生产中可循环使用的物质是_____________________。
(5)检验CaO28H2O是否洗净的方法是___________。
(6)已知CaO2在350℃迅速分解生成CaO和O2。如图是实验室测定产品中CaO2含量的装置(夹持装置省略)。

若所取产品质量是m g,测得气体体积为V mL(标况),产品中CaO2的质量分数为________(用字母表示)。过氧化钙的含量也可用重量法测定,需要测定的物理量有______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示原电池工作时,右池中Y2O72-转化为Y3+。下列叙述正确的是( )

A. 左池电极反应式:X4+ + 2e- = X2+
B. 每消耗1mol Y2O72-,转移3mol电子
C. 左池中阴离子数目增加
D. 盐桥中阴离子移向右池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①CO2(g)+2H2(g)═ CH3OH(g)+![]() O2(g) △H=+192.9kJ/mol
O2(g) △H=+192.9kJ/mol
②H2(g)+ ![]() O2(g)═H2O(l) △H=285.8kJ/mol
O2(g)═H2O(l) △H=285.8kJ/mol
则CH3OH(g) +![]() O2(g)═CO2(g)+2H2O(l)的△H为( )
O2(g)═CO2(g)+2H2O(l)的△H为( )
A. +478.7kJ/mol
B. 764.5kJ/mol
C. 478.7kJ/mol
D. +764.5kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)![]() xC(g)+2D(g),经5min后,测得D的浓度为0.5mol/L,c(A):c(B)=3:5,C的平均反应速率为0.1 mol/(Lmin),试求:(1)x的值_______;
xC(g)+2D(g),经5min后,测得D的浓度为0.5mol/L,c(A):c(B)=3:5,C的平均反应速率为0.1 mol/(Lmin),试求:(1)x的值_______;
(2)5min时A的浓度_______;
(3)此5min内B的转化率_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量的水后,产生1.16g白色沉淀。再向所得悬浊液中逐滴加入1.00mol/L HCl溶液,加入HCl溶液的体积与生成沉淀的关系如图所示。试回答:

(1)写出A点到B点发生反应的离子方程式
(2)C点加入盐酸溶液的体积为 。
(3)原混合物中MgCl2的物质的量是 ,NaOH的质量是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】采用下列装置和操作,能达到实验目的的是

A. 用装置甲分离出溴苯 B. 用装置乙验证乙炔的还原性
C. 用装置丙制取乙烯 D. 用装置丁制取乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)实验室模拟合成氨和氨催化氧化的流程如下:


(1)N元素在周期表中位置_______________________。
(2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合、干燥,还有______________作用。
(3)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热,锥形瓶中还可观察到的现象是_______________________________________。
(4)写出乙装置中氨氧化的化学方程式:__________________________________________。
(二)实验室探究铜与硝酸反应的相关问题,按下图所示装置进行实验。

请回答下列问题:
(5)装置甲中盛放浓硝酸的仪器A的名称是_______________________。
(6)实验过程中,装置丙中出现的现象是:________________________________________。
(7)装置丙中的试管内发生反应的离子方程式为:__________________________________。
取下装置丙中的试管D,在其中滴加FeSO4溶液,再滴加KSCN溶液,溶液变为______________色。
(8)待反应停止后,Cu片有剩余,取下B,加入少量质量分数为25%的稀硫酸,这时铜片上又有气泡产生,离子方程式为________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com