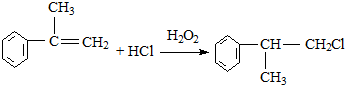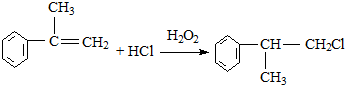�ش��������⣺
��1����Al
2O
3��Ni������̬���ᷢ�����з�Ӧ��
���ᣨg��=CO ��g��+H
2O ��g����H
1=+34.0kJ/mol
���ᣨg��=CO
2 ��g��+H
2��g����H
2=-7.0kJ/mol
�ڸ������£���̬CO
2 ����̬H
2 ������̬CO����̬H
2O���Ȼ�ѧ����ʽΪ
CO2��g��+H2��g��=CO��g��+H2O��g����H=+41.0kJ/mol
CO2��g��+H2��g��=CO��g��+H2O��g����H=+41.0kJ/mol
��
��2������ƽ�����ʢ��ǿ��ԭ��Һ̬�£�N
2H
4����ǿ������Һ̬˫��ˮ��H
2O
2��������0.4molҺ̬�º�0.8mol Һ̬H
2O
2��Ϸ�Ӧ�����ɵ�����ˮ�������ų�256.7kJ���������൱��25�桢101kPa�²�õ�����������Ӧ���Ȼ�ѧ����ʽΪ
N2H4��l��+2H2O2��l���TN2��g��+4H2O��g����H=-641.75kJ?mol-1
N2H4��l��+2H2O2��l���TN2��g��+4H2O��g����H=-641.75kJ?mol-1
��
��3����֪��C��s��+O
2��g��=CO
2��g����H=-393.5kJ?mol
-12H
2��g��+O
2��g��=2H
2O��g����H=-483.6kJ?mol
-1����0.2mol��̿�ۺ�������ɵ����������һ��������������ȫȼ�գ����ų�63.53kJ��������������C��H
2�����ʵ���֮��Ϊ
1��1
1��1
��



 ��ҵ����ϵ�д�
��ҵ����ϵ�д� ͬ��ѧ��һ�ζ���ϵ�д�
ͬ��ѧ��һ�ζ���ϵ�д� �����ܾ�ϵ�д�
�����ܾ�ϵ�д�
 ��һ��ҽҩ�м��壬�������Ʊ�����Ѫҩ����ͨ������·�ߺϳ�
��һ��ҽҩ�м��壬�������Ʊ�����Ѫҩ����ͨ������·�ߺϳ�




 ��XΪ±��ԭ�ӣ�
��XΪ±��ԭ�ӣ� �����ʣ���������һ�����ϣ�
�����ʣ���������һ�����ϣ�