
”¾ĢāÄæ”æĆøŹĒŅ»ÖÖ(””””)
A. ĢĒĄą B. ÓĶÖ¬
C. µ°°×ÖŹ»ņRNA D. Ī¬ÉśĖŲ

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠ¹ŲSO2µÄŠŌÖŹ£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A. ÄÜŹ¹Ę·ŗģČÜŅŗĶŹÉ« B. ÄÜÓėNaOHČÜŅŗ·“Ó¦
C. ÄÜÓėH2O·“Ӧɜ³ÉH2SO4 D. Ņ»¶ØĢõ¼žĻĀÄÜÓėO2·“Ӧɜ³ÉSO3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijģÄā”°ČĖ¹¤Ź÷Ņ¶”±µÄµē»ÆѧŹµŃé×°ÖĆČēĶ¼ĖłŹ¾£¬øĆ×°ÖĆÄܽ«H2OŗĶCO2×Ŗ»ÆĪŖO2ŗĶČ¼ĮĻ£ØC3H8O£©”£ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ
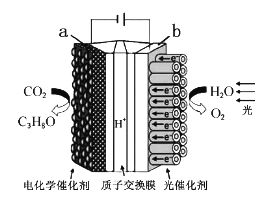
A. øĆ×°ÖĆ¹¤×÷Ź±£¬H+“Ób¼«ĒųĻņa¼«ĒųĒØŅĘ
B. ĆæÉś³É1molO2£¬ÓŠ44gCO2±»»¹Ō
C. aµē¼«µÄ·“Ó¦Ź½ĪŖ3CO2+18H++18e£=C3H8O+5H2O
D. C3H8OŗĶO2ŠĪ³ÉČ¼ĮĻµē³ŲŅŌĒāŃõ»ÆÄĘ×÷ĪŖµē½āÖŹČÜŅŗµÄøŗ¼«·“Ó¦Ź½£ŗC3H8O£18e£+24OH£=3CO32£+16H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潚Źōīę(58Ce)³£ÓĆÓŚÖĘ×÷Ļ”ĶĮ“ÅŠŌ²ÄĮĻ£¬æÉÓ¦ÓĆÓŚÖĘŌģ²£Į§”¢“ņ»šŹÆ”¢ĢÕ“ÉŗĶŗĻ½šµČ”£ŅŃÖŖ£ŗCe4++Fe2+=Ce3++Fe3+”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ( )
A. CeŌŖĖŲĪ»ÓŚŌŖĖŲÖÜĘŚ±ķµŚĮłÖÜĘŚµŚIIIB×å
B. ![]() Ӣ
”¢![]() ŹĒĶ¬ĖŲŅģŠĪĢå
ŹĒĶ¬ĖŲŅģŠĪĢå
C. īęÄÜČÜÓŚHIČÜŅŗ£¬·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗCe+4H+=Ce4++2H2
D. īęµÄŌ×ÓŗĖĶāÓŠ58øöµē×Ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŃõ»Æ»¹Ō·“Ó¦ŌŚÉś²ś”¢Éś»īÖŠÓ¦ÓĆ¹ć·ŗ”£ĻĀĮŠ·“Ó¦²»ŹōÓŚŃõ»Æ»¹Ō·“Ó¦µÄŹĒ
A. ľĢæČ¼ÉÕ£ŗC + O2![]() CO2
CO2
B. ģŃÉÕŹÆ»ŅŹÆ£ŗCaCO3 ![]() CaO + CO2 ”ü
CaO + CO2 ӟ
C. ĢśµÄŅ±Į¶£ŗFe2O3£«3CO![]() 2Fe£«3CO2
2Fe£«3CO2
D. µē½āĖ®£ŗ 2H2O ![]() 2 H2 ”ü + O2 ”ü
2 H2 ӟ + O2 ӟ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĒā·śĖįŹĒŅ»ÖÖČõĖį£¬æÉÓĆĄ“æĢŹ“²£Į§”£
ŅŃÖŖ25”ꏱ£ŗ¢ŁHF(aq)+OH-(aq)=F-(aq)+H2O£Ø1£©¦¤H=-67£®7kJ”¤mol-1£¬¢ŚH+(aq)+OH-(aq)=H2O£Ø1£© ¦¤H=-57£®3kJ”¤mol-1”£ŌŚ20mL0£®1mol”¤L-1Ēā·śĖįÖŠ¼ÓČėVmL0£®1mol”¤L-1NaOHČÜŅŗ£¬ĻĀĮŠÓŠ¹ŲĖµ·Ø²»ÕżČ·µÄŹĒ
A. Ēā·śĖįµÄµēĄė·½³ĢŹ½¼°ČČŠ§Ó¦æɱķŹ¾ĪŖ£ŗ HF(aq)![]() F-(aq)+ H+(aq) ¦¤H=-10£®4kJ”¤mol-1
F-(aq)+ H+(aq) ¦¤H=-10£®4kJ”¤mol-1
B. µ±V=20Ź±£¬ČÜŅŗÖŠ£ŗc(OH-)=c(HF)+c(H+)
C. µ±V=20Ź±£¬ČÜŅŗÖŠ£ŗc(F-)<c(Na+)=0£®1mol”¤L-1
D. µ±V>0Ź±£¬ČÜŅŗÖŠæÉÄÜ“ęŌŚ£ŗc(Na+)>c(F-)>c(OH-)>c(H+)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŹµŃéĻÖĻó»ņĶ¼ĻóŠÅĻ¢²»Äܳä·ÖĖµĆ÷ĻąÓ¦»Æѧ·“Ó¦ŹĒ·ÅČČ·“Ó¦µÄŹĒ£Ø £©
A | B | C | D | |
·“ӦװÖĆĶ¼»ņĶ¼Ļó |
|
|
|
|
ŹµŃéĻÖĻó | ĪĀ¶Č¼ĘµÄĖ®ŅųÖł²»¶ĻÉĻÉż | ·“Ó¦Īļ×ÜÄÜĮæ“óÓŚÉś³ÉĪļ×ÜÄÜĮæ | ·“Ó¦æŖŹ¼ŗ󣬼ד¦ŅŗĆęµĶÓŚŅŅ“¦ŅŗĆę | ·“Ó¦æŖŹ¼ŗó£¬ÕėĶ²»īČūĻņÓŅŅĘ¶Æ |
A. A B. B C. C D. D
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĶ¼ŹĒŌŖĖŲÖÜĘŚ±ķµÄŅ»²æ·Ö£¬Ēė»Ų“šĻĀĮŠĪŹĢā”£
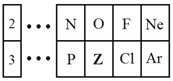
£Ø1£©ZŌŖĖŲŌŚŌŖĖŲÖÜĘŚ±ķÖŠĪ»ÓŚµŚ________×唣
£Ø2£©ZµÄŌ×Ó°ė¾¶__________£ØĢī”°“óÓŚ”±”¢”°Š”ÓŚ”±»ņ”°µČÓŚ”±£©SiµÄŌ×Ó°ė¾¶”£
£Ø3£©ClŌŖĖŲµÄ·Ē½šŹōŠŌ±ČZŌŖĖŲµÄ__________£ØĢī”°Ēæ”±»ņ”°Čõ”±£©”£
£Ø4£©ZŌŖĖŲµÄĘųĢ¬Ēā»ÆĪļµÄ»ÆѧŹ½ĪŖ________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”涞Ńõ»ÆĢ¼ŹĒŅżĘš”°ĪĀŹŅŠ§Ó¦”±µÄÖ÷ŅŖĪļÖŹ£¬Ó¦øĆ¼õÉŁ¶žŃõ»ÆĢ¼µÄÅÅ·Å”£
£Ø1£©ÓŠŅ»ÖÖÓĆCO2Éś²ś¼×“¼Č¼ĮĻµÄ·½·Ø£ŗ
ŅŃÖŖ£ŗCO2£Øg£©+3H2£Øg£©ØTCH3OH£Øg£©+H2O£Øg£©”÷H=-a kJmol-1£»
CH3OH£Øg£©ØTCH3OH£Øl£©”÷H=-b kJmol-1£»
2H2£Øg£©+O2£Øg£©ØT2H2O£Øg£©”÷H=-c kJmol-1£»
H2O£Øg£©ØTH2O£Øl£©”÷H=-d kJmol-1£¬
Ōņ±ķŹ¾CH3OH£Øl£©Č¼ÉÕČȵÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗ_______________”£
£Ø2£©ŌŚŅ»¶ØĪĀ¶ČĻĀµÄ2L¹Ģ¶ØČŻ»żµÄĆܱÕČŻĘ÷ÖŠ£¬ĶØČė2mol CO2ŗĶ3mol H2£¬·¢ÉśµÄ·“Ó¦ĪŖ£ŗCO2£Øg£©+3H2£Øg£©![]() CH3OH£Øg£©+H2O£Øg£©”÷H<0£¬²āµĆCO2£Øg£©ŗĶCH3OH£Øg£©µÄÅضČĖꏱ¼ä±ä»ÆČēÓŅĶ¼ĖłŹ¾”£
CH3OH£Øg£©+H2O£Øg£©”÷H<0£¬²āµĆCO2£Øg£©ŗĶCH3OH£Øg£©µÄÅضČĖꏱ¼ä±ä»ÆČēÓŅĶ¼ĖłŹ¾”£
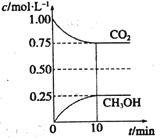
¢Ł“Ó0minµ½10min£¬v£ØH2£©=______”£
¢ŚĻĀĮŠ“ėŹ©ÖŠÄÜŹ¹![]() Ōö“óµÄŹĒ______£ØŃ”3Ģī±ąŗÅ£©”£
Ōö“óµÄŹĒ______£ØŃ”3Ģī±ąŗÅ£©”£
A£®ÉżøßĪĀ¶Č B£®ŗćĪĀŗćČŻĻĀ³äČėHe£Øg£©
C£®½«H2O£Øg£©“ÓĢåĻµÖŠ·ÖĄė D£®ŗćĪĀŗćČŻŌŁ³äČė2mol CO2ŗĶ3mol H2
¢Ū¼ĘĖćøĆĪĀ¶ČĻĀ“Ė·“Ó¦µÄĘ½ŗā³£ŹżK=______£ØĢī·ÖŹż»ņ±£ĮōĮ½Ī»ÓŠŠ§Źż×Ö£©”£Čōøıä______Ģõ¼ž£ØĢī±ąŗÅ£©£¬æÉŹ¹K=1”£
A£®Ōö“óŃ¹Ēæ B£®Ōö“ó·“Ó¦ĪļÅØ¶Č C£®½µµĶĪĀ¶Č D£®ÉżøßĪĀ¶Č E£®¼ÓČė“߻ƼĮ
£Ø3£©Ä³¼×“¼Č¼ĮĻµē³ŲŌĄķČēĶ¼1ĖłŹ¾
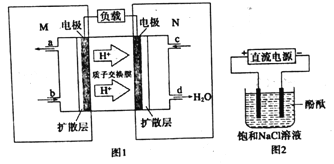
¢ŁŌņMĒų·¢ÉśµÄµē¼«·“Ó¦Ź½ĪŖ______”£
¢ŚÓĆÉĻŹöµē³Ų×öµēŌ“£¬ÓĆĶ¼2×°ÖƵē½ā±„ŗĶŹ³ŃĪĖ®£Øµē¼«¾łĪŖ¶čŠŌµē¼«£©£®ŌņøƵē½ā·“Ó¦µÄ×Ü·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ__________________”£
¼ŁÉčČÜŅŗĢå»żĪŖ300mL£¬µ±ČÜŅŗµÄpHÖµĪŖ13Ź±£ØŌŚŹŅĪĀĻĀ²ā¶Ø£©£¬ĄķĀŪÉĻĻūŗļד¼µÄÖŹĮæĪŖ______£ØŗöĀŌČÜŅŗĢå»ż±ä»Æ£©”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com