
【题目】一定温度下,在3个容积均为![]() 的恒容密闭容器中反应
的恒容密闭容器中反应![]() 达到平衡,下列说法正确的是
达到平衡,下列说法正确的是
容器 | 温度 | 物质的起始浓度 | 物质的平衡浓度 | ||
|
|
|
| ||
Ⅰ | 400 |
|
| 0 |
|
Ⅱ | 400 |
|
| 0 |
|
Ⅲ | 500 |
|
| 0 |
|
A. 该反应的正反应是吸热反应
B. 达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的小
C. 达到平衡时,容器Ⅱ中![]() 小于容器Ⅲ中
小于容器Ⅲ中![]()
D. 达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的小
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:
【题目】在某固定容积的密闭容器中,存在下列化学平衡aA(g) ![]() bB(g)+cC(g),在温度不变的条件下,向容器中再充入一定量的A物质,重新达到平衡时,判断在下列情况下有关物质量的变化趋势(在下列空白中填写“增大”“减小”或“不变”)
bB(g)+cC(g),在温度不变的条件下,向容器中再充入一定量的A物质,重新达到平衡时,判断在下列情况下有关物质量的变化趋势(在下列空白中填写“增大”“减小”或“不变”)
(1)当a=b+c时,B的物质的量分数___________。
(2)当a>b+c时,A的物质的量分数_______。
(3)当a<b+c时,A的转化率___________。
(4)当a<b+c时,混合气体的平均相对分子质量 ___,混合气体的密度 _____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式书写正确的是(ΔH的绝对值均正确) ( )
A. C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) ΔH=-1 367.0 kJ·mol-1(燃烧热)
B. NaOH(aq)+HI(aq)=NaI(aq)+H2O(l) ΔH=-57.3 kJ·mol-1(中和热)
C. S(s)+![]() O2(g)=SO3(g) ΔH=-296.8 kJ·mol-1(燃烧热)
O2(g)=SO3(g) ΔH=-296.8 kJ·mol-1(燃烧热)
D. 2NO2=O2+2NO ΔH=+116.2 kJ·mol-1(反应热)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是373K时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是 ( )

A. 该反应的热化学方程式为:N2+3H2![]() 2NH3 △H=-92kJ·mol-1
2NH3 △H=-92kJ·mol-1
B. 加入催化剂,该化学反应的反应热不变
C. a曲线是加入催化剂时的能量变化曲线
D. 在温度体积一定的条件下,通入1mol N2和3 mol H2反应后放出的热量为Q1kJ,则Q1=92
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列物质中原子数最多的是
A. 64 g SO2 B. 3.01×1023个N2
C. 0.75 mol H2S D. 36 mL H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)工业上利用N2和H2合成NH3,NH3又可以进一步制备联氨(N2H4)等。由NH3制备N2H4的常用方法是NaClO氧化法,其离子反应方程式为___________,有学者探究用电解法制备的效率,装置如图,试写出其阴极电极反应式__________________;

(2)某种铅酸蓄电池具有廉价、长寿命、大容量的特点,它使用的电解质是可溶性的甲基磺酸铅,电池的工作原理:Pb+PbO2+4H+![]() 2Pb2++2H2O充电时,阳极的电极反应式为_________;
2Pb2++2H2O充电时,阳极的电极反应式为_________;
(3)乙醇汽油是被广泛使用的新型清洁燃料,工业生产乙醇(CH3CH2OH)的一种反应原理为:2CO(g)+4H2(g)![]() CH3CH2OH(g)+H2O(g) △H=-akJ/mol
CH3CH2OH(g)+H2O(g) △H=-akJ/mol
己知:CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-bkJ/mol
CO2(g)+H2(g) △H=-bkJ/mol
以CO2(g)与H2(g)为原料也可合成乙醇,并放出热量,写出该反应的热化学反应方程式:___________。
(4)如图是一个电化学过程的示意图。

请回答下列问题:
![]() 写出通入CH3OH的电极的电极反应式______。
写出通入CH3OH的电极的电极反应式______。
②乙池中C棒电极反应的方程式为__________________,当乙池中B极质量增加10.8g,此时丙池中析出3.2g某金属,则丙池中的某盐溶液可能是______(填序号)
A.MgSO4溶液 B.CuSO4溶液 C.NaCl溶液 D.AgNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列叙述正确的是
A. 9g超重水(3H216O)含中子数为6NA
B. 标准状况下,22.4L CCl4含有的分子数目为NA
C. 78g过氧化钠中含有的阴阳离子总数为4NA
D. 28g乙烯与聚乙烯的混合物完全燃烧生成水的分子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学想通过实验探究硫和碳得电子能力的强弱,通过比较它们最高价氧化物对应水化物的酸性强弱来验证,设计了如图实验。
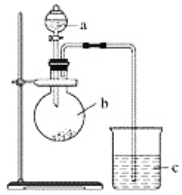
(1)仪器a的名称是________,应盛放下列药品中的________(填字母)。
A.稀硫酸 B.亚硫酸C.氢硫酸 D.盐酸
(2)仪器b的名称是________,应盛放下列药品中的________(填字母)。
A.碳酸钙 B.硫酸钠 C.氯化钠 D.碳酸钠
(3)仪器c中应盛放的试剂是________,如果看到的现象是____________________,证明b中反应产生了________,即可证明________比________酸性强,得电子能力________比________强,b中发生反应的离子方程式为______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com