
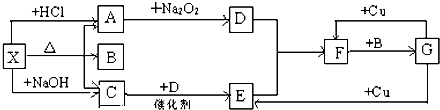
| ||
| △ |
| ||
| △ |
| ||
| ||
| 1mol×[5-(-3)]a |
| 4 |


科目:高中化学 来源: 题型:
| A、现象相同,所得气体的体积相等 |
| B、现象相同,所得气体的体积不等 |
| C、现象不同,所得气体的体积相等 |
| D、现象不同,所得气体的体积不等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
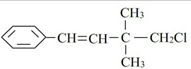
| A、不能使酸性KMnO4溶液褪色 |
| B、不能发生取代反应 |
| C、在加热和催化剂作用下,最多能和4 mol H2反应 |
| D、一定条件下,能和NaOH醇溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N5+有24个电子 |
| B、N5+离子中存在三对未成键的电子对 |
| C、N5+阳离子中存在两个氮氮三键 |
| D、N5+在水中可以稳定存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X、Y、Z、W的原子半径的大小关系为:W>Y>Z>X |
| B、在Y2X2、Z2X4、X2W2的一个分子中,所含的共用电子对数相等 |
| C、X、Y、Z、W四种元素可形成化学式为X7Y2ZW2的化合物 |
| D、与元素Y、Z相比,元素W形成的简单氢化物最稳定,是因为其分子间存在氢键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
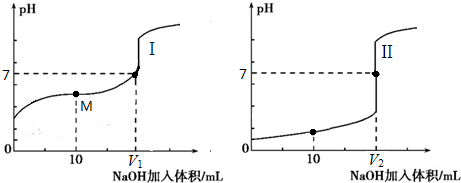 电解质的水溶液中存在电离平衡.
电解质的水溶液中存在电离平衡.| 操作步骤 | 现象 |
| 步骤1:向2mL 0.005mol?L-1 AgNO3溶液中加入2mL 0.005mol?L-1KSCN溶液,静置. | 出现白色沉淀. |
| 步骤2:取1mL上层清液于试管中,滴加1滴2mol?L-1 Fe(NO3)3溶液. | 溶液变红色. |
| 步骤3:向步骤2的溶液中,继续加入5滴3mol?L-1AgNO3溶液. | |
| 步骤4:向步骤1余下的浊液中加入5滴3mol?L-1KI溶液. | 出现黄色沉淀. |
查看答案和解析>>
科目:高中化学 来源: 题型:
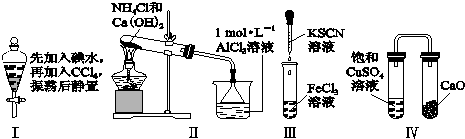
| A、实验Ⅰ:液体分层,下层呈无色 |
| B、实验Ⅱ:烧杯中先出现白色沉淀,后溶解 |
| C、实验Ⅲ:试管中立刻出现红色沉淀 |
| D、实验Ⅳ:放置一段时间后,饱和CuSO4溶液中出现蓝色晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ca2+ |
| B、Na+ |
| C、OH- |
| D、Ag+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com