
【题目】如图所示,一密闭容器被无摩擦、可滑动的两隔板a和b分成甲、乙两室。标准状况下,在乙室中充入1.2molHCl,甲室中充入NH3、H2的混合气体,静止时活塞位置如下图。已知甲室中气体的质量比乙室中气体的质量少33.8g。

请回答下列问题:
(1)甲室中气体的物质的量为___________mol。
(2)甲室中气体的质量为__________g。
(3)甲室中NH3、H2的物质的量之比为_____________,质量比为___________。
(4)经过查资料知道HCl+NH3=NH4Cl(NH4Cl常温下是固体,假设固体的体积可忽略),如果将板a去掉,当HCl与NH3完全反应后,活塞b将静置于刻度“___________”处(填数字)
【答案】
(1)2;
(2)10;
(3)1:4;17:8;
(4)6
【解析】
试题分析:(1)由图可知甲、乙两室气体的体积之比为5:3,故其物质的量之比也为5:3,所以甲室中气体为2mol,故答案为:2;
(2)HCl气体的质量为1.2mol×36.5g/mol=43.8g,则甲室中气体的质量为43.8g-33.8g=10g,故答案为:10;
(3)设氨气的物质的量为x,氢气的物质的量为y,根据其物质的量、质量列方程组为:x+y=2,17x+2y=10,解得x=0.4,y=1.6,所以氨气和氢气的物质的量之比=0.4mol:1.6mol=1:4,其质量之比=(0.4mol×17g/mol):(1.6mol×2g/mol)=17:8,故答案为:1:4;17:8;
(4)甲室中NH3的物质的量为2mol×1/5=0.4mol,能与0.4molHCl反应,剩余气体为2.4mol,相同条件下,气体的体积之比等于其物质的量之比,所以活塞b会移至“6”处,故答案为:6。


科目:高中化学 来源: 题型:
【题目】氯碱工业是以电解饱和食盐水为基础的基本化学工业。下图是某氯碱工业生产原理示意图:
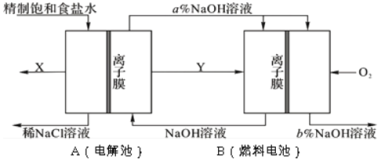
(1)写出装置A在通电条件下反应的化学方程式______________。
(2)A装置所用食盐水由粗盐水精制而成。精制时,为除去食盐水中的Mg2+和Ca2+,要加入的试剂分别为___________、___________。
(3)氯碱工业是高耗能产业,按上图将电解池与燃料电池相组合的新工艺可以节(电)能30%以上,且相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
①图中Y是______________(填化学式);X与稀NaOH溶液反应的离子方程式是:______________。
②分析比较图示中氢氧化钠质量分数a%与b%的大小___________。
③若用B装置作为A装置的辅助电源,每当消耗标准状况下氧气的体积为11.2 L时,则B装置可向A装置提供的电量约为______________(一个e-的电量为1.60×10-19C;计算结果精确到0.01)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若将基态P原子的电子排布式写成1s22s22p63s23px23py1,它违背了
A. 泡利原理 B. 能量守恒原理 C. 构造原理 D. 洪特规则
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
①硫酸、烧碱、醋酸钠和石灰石分别属于酸、碱、盐和氧化物;
②蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质;
③Mg、Fe、Ag在工业上分别用电解熔融MgO法、热还原法、热分解法冶炼制取;
④刚玉、石英、草酸的主要成分分别为Al2O3、SiO2、HOOCCOOH
A.①② B.③④
C.②③ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在下列物质中①![]() Li ②
Li ②![]() Na③
Na③![]() Mg④
Mg④![]() Li⑤
Li⑤![]() C⑥C60⑦异丁烷⑧正丁烷⑨石墨
C⑥C60⑦异丁烷⑧正丁烷⑨石墨
互为同位素的是 (填编号,下同);互为同素异形体的是 ;
互为同分异构体的是 。
(2)在下列事实中,是什么因素影响了化学反应的速率?
夏天的食品易发霉,冬天就不易发生该现象。影响因素是 ;
MnO2加入双氧水中反应更剧烈。影响因素是 ;
同浓度、同体积的盐酸中放入同样大小的锌粒和镁条,镁条产生气体更快。影响因素是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)将锌片和银片用导线相连浸入稀硫酸中组成原电池。该电池中负极发生___________反应(填“氧化”或“还原”);溶液中的H+移向___________(填“正极”或“负极”)。若该电池中两电极的总质量为60 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质变质量为47 g,试计算产生氢气的体积(标准状况)___ ___________。
(2)现有反应2FeCl3+Cu===2FeCl2+CuCl2,请根据该反应的实质,设计成原电池,画出装置图并标出正、负极材料、电解质溶液 。
(3)实验室制备Fe(OH)2沉淀时,由于其在空气中极易发生反应______________.
(填化学方程式)而很难观察到沉淀的颜色。
为制得Fe(OH)2白色沉淀,有人设计了如右图所示的装置,用NaOH溶液、铁屑、稀H2SO4等试剂制备.实验时试管Ⅰ里应加入

(填试剂名称).在试管Ⅰ和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是_______ _.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是
A.向0.1mol![]() CH3COOH溶液中加入少量水,溶液中
CH3COOH溶液中加入少量水,溶液中![]() 减小
减小
B.将CH3COONa溶液从20℃升温至60℃,溶液中![]() 增大
增大
C.向盐酸中加入氨水至中性,溶液中![]()
D.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中![]() 不变
不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于资源、能源、环保方面的叙述正确的是
A.天然气是较清洁的可再生能源,因此发展前景非常好
B.地壳中有丰富的金属资源,其中最多的金属元素是铁,也是人类需要最多的金属
C.空气是重要的自然资源.其中氮氮气约占空气体积的87%
D.使用乙醇汽油能减少污染,节约石油资源
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com