
| A. | Fe3O4是还原剂 | B. | CO是氧化剂 | ||
| C. | 1mol Fe3O4得到6mol电子 | D. | 4molCO失去8mol电子 |
分析 Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2中,Fe元素的化合价由+$\frac{8}{3}$降低0价,C元素的化合价由+2升高到+4,以此来解答.
解答 解:A.Fe3O4中Fe元素的化合价降低,做氧化剂,故A错误;
B.CO中C元素的化合价升高,则CO为还原剂,故B错误;
C.Fe元素的化合价由+$\frac{8}{3}$降低0价,所以1molFe3O4得到8mol电子,故C错误;
D.C元素的化合价由+2升高到+4,所以4molCO失去8mol电子,故D正确.
故选D.
点评 本题考查氧化还原反应,把握元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意氧化剂的判断,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
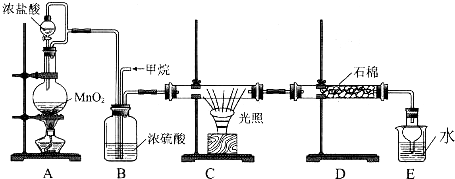
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大于0.6mol | B. | 大于零 | C. | 等于1mol | D. | 任意值 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴乙烷与氢氧化钠溶液共煮后,加入硝酸银检验Br- | |
| B. | 用电石和饱和食盐水制取乙炔 | |
| C. | 用苯、12mol/L的硝酸和18mol/L的硫酸制硝基苯 | |
| D. | 用稀硝酸洗涤做过银镜反应的试管 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某化合物焰色反应呈黄色,说明该物质中一定含有Na+ | |
| B. | 向某溶液中加入盐酸有气泡产生,说明一定有CO32- | |
| C. | 向某溶液中加入氯化钡溶液,有白色沉淀产生,说明一定有SO42- | |
| D. | 向某溶液中加入硝酸银溶液,有白色沉淀产生,说明一定有Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO是氧化剂 | B. | CO发生还原反应 | ||
| C. | NO失去电子 | D. | 该反应是复分解反应 |
查看答案和解析>>
科目:高中化学 来源:2017届吉林省高三上第二次模拟化学试卷(解析版) 题型:填空题
2 g Cu2S和CuS的混合物在酸性溶液中用400 mL 0.075 mol·L-1 KMnO4溶液处理,发生反应如下:
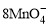 +5Cu2S+44H+= 10Cu2++5SO2↑+8Mn2++22H2O
+5Cu2S+44H+= 10Cu2++5SO2↑+8Mn2++22H2O
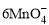 +5CuS+28H+ = 5Cu2++5SO2↑+6Mn2++14H2O
+5CuS+28H+ = 5Cu2++5SO2↑+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350 mL 0.1 mol·L-1(NH4)2Fe(SO4)2溶液完全反应。(1)配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式
______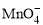 +______Fe2++______H+ =______Mn2++______Fe3++___
+______Fe2++______H+ =______Mn2++______Fe3++___ ___H2O
___H2O
(2)KMnO4溶液与混合物反应后,剩余KMnO4的物质的量为________mol。
(3)混合物中Cu2S的质量分数为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com