
【题目】利用醇的消去反应是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图所示,可能用到的有关数据如下:
相对分子质量 | 密度(g·cm-3) | 沸点/℃ | 溶解性 | |
环乙醇 | 100 | 0.9618 | 161 | 微溶于水 |
环已烯 | 82 | 0.8102 | 83 | 难溶于水 |
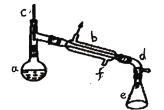
a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓硫酸。b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃。反应粗产物倒入f中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环已烯。回答下列问题:
(1)由环己醇制取环己烯的方程式___________________________________________;
(2)装置b的冷凝水方向是______(填下进上出或上进下出);
(3)加入碎瓷片的作用是______;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是______(填正确答案标号)。
A.立即补加B.冷却后补加C.不需补加D.重新配料
(4)本实验中最容易产生的副产物所含的官能团名称为___________。
(5)在分离提纯中,使用到的仪器f名称是______,分离氯化钙的操作是_______。
(6)合成过程中加入浓硫酸的作用是_______。
【答案】
![]()
![]() +H2O 下进上出 防止暴沸 B 醚键 分液漏斗 过滤 催化剂、脱水剂
+H2O 下进上出 防止暴沸 B 醚键 分液漏斗 过滤 催化剂、脱水剂
【解析】
(1)环己醇在浓硫酸、加热条件下发生消去反应生成环己烯;
(2)冷凝管采用逆向通水,冷凝效果好;
(3)碎瓷片的存在可以防止在加热过程中产生暴沸现象,补加碎瓷片时需要待已加热的试液冷却后再加入;
(4)加热过程中,环己醇除可发生消去反应生成环己烯外,还可以发生取代反应生成二环己醚;
(5)环己烯不溶于水,可通过分液操作分离;氯化钙不溶于环己烯,可通过过滤操作分离;
(6)浓硫酸环己烯的制取过程中起到了催化剂和脱水剂的作用。
(1)在浓硫酸存在条件下,加热环己醇可制取环己烯,反应的化学方程式为:
![]()
![]() +H2O,故答案为:
+H2O,故答案为:
![]()
![]() +H2O;
+H2O;
(2)蒸馏操作中,冷凝管采用逆向通水,即下进上出通水,冷凝效果较好,故答案为:下进上出;
(3)碎瓷片的存在可以防止在加热过程中产生暴沸现象,补加碎瓷片时需要待已加热的试液冷却后再加入,故答案为:防止暴沸;B;
(4)加热过程中,环己醇除可发生消去反应生成环己烯外,还可以发生取代反应,分子间发生脱水反应生成二环己醚,副产物的结构简式为![]() ,含有的官能团为醚键,故答案为:醚键;
,含有的官能团为醚键,故答案为:醚键;
(5)环己烯难溶于水,可通过分液操作分离,使用的仪器为分液漏斗;氯化钙不溶于环己烯,可通过过滤操作分离出氯化钙,故答案为:分液漏斗;过滤;
(6)在反应
![]()
![]() +H2O中,浓硫酸起到了催化剂和脱水剂的作用,故答案为:催化剂、脱水剂。
+H2O中,浓硫酸起到了催化剂和脱水剂的作用,故答案为:催化剂、脱水剂。


 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:
【题目】T°C时,在某恒容的密闭容器中,发生如下反应:SO2(g) +2CO(g) ![]() 2CO2 (g)+ S(l)△H < 0;下列情况不能说明该反应达到平衡状态的是
2CO2 (g)+ S(l)△H < 0;下列情况不能说明该反应达到平衡状态的是
A.容器内混合气体的密度不变
B.容器内压强不变
C.v(CO)生成= v(CO2)消耗
D.S的质量不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】兴趣小组在实验室中模拟利用甲烷和氯气发生取代反应制取副产品盐酸,设计如图装置,下列说法错误的是( )
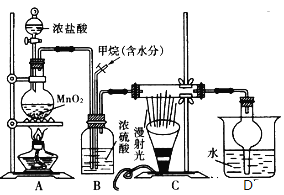
A.实验时先点燃A处酒精灯再通甲烷
B.装置B有均匀混合气体、控制气流速度、干燥混合气体等作用
C.从D中分离出盐酸的方法为过滤
D.装置C经过一段时间的强光照射后,生成的有机物有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)广泛应用于冶金、电镀、医药等行业。某同学以含铜废料(主要成分是 CuO、MgO、MnO、SiO2及少量的杂质)为主要原料制备CuCl的主要流程如下:
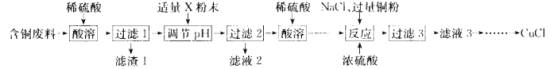
已知:①CuCl难溶于水和乙醇 ,在潮湿的空气中易被氧化;
②在水溶液中存在平衡 :CuCl(白色)+2Cl-![]() [CuCl3]2-(色无溶液)。
[CuCl3]2-(色无溶液)。
③几种金属氢氧化物开始沉淀和完全沉淀的pH如下表:
氢氧化物 | 开始沉淀的 pH | 完全沉淀的 pH |
Mg(OH)2 | 8. 4 | 10. 8 |
Cu(OH)2 | 4.2 | 6. 7 |
Mn(OH)2 | 7. 8 | 8. 8 |
问答下列问题:
(1)滤渣1 的主要成分是 _________________(写化学式,下同)。
(2)“调pH”所用粉末状试剂 X 是_____________;pH的调节范闱为____________。
(3)“反应”发生 Cu2+ +Cu+6Cl-=2[CuCl3]2-,表明已完全反应的现象是_______________。
(4)向“滤液3” 加大量的水,过滤可得 CuCl。所得沉淀需再用乙醇洗涤.并在低温下干燥,其原因是___________。
(5)产品纯度的测定,步骤如下:称取mg试样置于锥形瓶中,加入直径 4 ~ 5 mm 玻璃珠适量,并加入 10 mL FeCl3溶液,摇动至样品全部溶解后(CuCl+FeCl3=CuCl2+FeCl2),再加入50 mL,水和2滴邻菲罗啉指示剂,立刻用c mol L-1 的硫酸高铈[Ce(SO4)2]标准溶液滴定(Fe2++Ce4+=Fe3++Ce3+)'滴至终点时共消耗硫酸高铈标准溶液V mL。
①锥形瓶中加入玻璃珠的作用是____________________。
②样品中 CuCl 的质量分数为_____(列出表达式即可 , 用含(c、m、V的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“达菲”是瑞士罗氏公司研制的有效治疗人类禽流感的药物。达菲的主要合成原料是我国盛产的莽草酸。


下列说法不正确的是( )
A.莽草酸可溶于水
B.1 mol莽草酸最多可和4 molNaOH溶液反应
C.从结构上推测,达菲既可与盐酸反应又可与氢氧化钠溶液反应
D.从结构上推测,以莽草酸为原料合成达菲须经过酯化反应等步骤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下两个容积相等的储气瓶,一个装有C2H4,另一个装有C2H2和C2H6的混合气体,两瓶气体一定具有相同的( )
A.质量B.密度C.碳原子数D.原子总数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分。
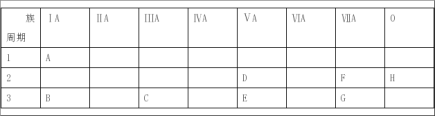
根据A~G元素在周期表中的位置,用化学式填写空白。
(1)单质中氧化性最强的是_______,还原性最强的是_____,化学性质最不活泼的是______。
(2)最高价氧化物对应水化物的酸性最强的酸是_________,最稳定的氢化物是__________。
(3)按碱性逐渐减弱、酸性逐渐增强的顺序,将B、C、E、G四种元素的最高价氧化物对应水化物的化学式排列成序是________。
(4)D、E、F三种元素按原子半径由大到小的顺序排列为____。
(5)A的氧化物常温下呈____态,它和B的单质反应后所得溶液的pH____7。
(6)B2O2的电子式为______,其中化学键的类型有____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予了锂离子电池领域做出巨大贡献的三位科学家。某锂离子电池![]() 为负极,
为负极,![]() 为正极,锂盐有机溶液作电解质溶液,电池反应为
为正极,锂盐有机溶液作电解质溶液,电池反应为![]() 则下列有关说法正确的是
则下列有关说法正确的是
A.金属锂的密度、熔点和硬度均比同族的碱金属低
B.该锂离子电池可用乙醇作有机溶剂
C.电池放电时,Li+从正极流向负极
D.电池充电时,阳极的电极反应式为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com