
����Ŀ��A��B��C��D��E��F��G���ֶ�����Ԫ�ص�ԭ�����������������н���һ��ϡ������Ԫ�ء�A��E������������ͬ������������Ԫ�ص�ԭ���У�A ԭ�ӵİ뾶��С��EԪ����ɫ��Ӧ��ɫΪ��ɫ��B��C��F��G�����ڱ������ڣ�B��Cͬ���ڣ�F��Gͬ����C��Fͬ���壬 CԪ���ǵؿ��к�������Ԫ�أ�A��C���γ����ֳ�����Һ̬������X��Y����Է�������X��Y����D�γɵķ���Ϊ��ԭ�ӷ��ӡ��ش����⣺
��1��GԪ��Ϊ______(��Ԫ�ط���)�� Y�ĵ���ʽΪ_______________��
��2��Һ̬������Y��ϡH2SO4�ữ��K2Cr2O7��Һ���ÿɲ���һ����ɫ��ȼ�����弰�����Ե�Cr2(SO4)3����÷�Ӧ�����ӷ���ʽΪ______________________________________��
��3����ij�ֽ�����������A��C��E��ɵĻ������ˮ��Һ��Ӧ������������ɳ���������д���÷�Ӧ�����ӷ���ʽ____________��ʹ������������ڵ�������________________��
��4��P��Q�������ʶ�����A��C��E��F����Ԫ����ɵ��Σ���ˮ��Һ�������ԣ������ʵ�����P��Qǡ����ȫ��Ӧ��д���÷�Ӧ�����ӷ���ʽ��_________________________���������ξ����еĻ�ѧ������Ϊ________________________��
��5����A��B��Ԫ���γɵĻ�����W����Ϊ����ƽ����е�ǿ��ԭ������֪һ��W���Ӻ�һ��Y�����ж�����18�����ӣ�0.5molҺ̬W������Һ̬Y��Ӧ������һ����ɫ��ζ��������B2��Һ̬X��д���÷�Ӧ�Ļ�ѧ����ʽΪ__________________________��
���𰸡�Cl ![]() 3H2O2+Cr2O72-+8H+=2Cr3++3O2��+7H2O 2Al+2OH-+2H2O=2A1O2-+3H2�� ������ᷢ����ը H++HSO3-=H2O+SO2�� ���Ӽ������ۼ� N2H4+2H2O2=N2��+4H2O
3H2O2+Cr2O72-+8H+=2Cr3++3O2��+7H2O 2Al+2OH-+2H2O=2A1O2-+3H2�� ������ᷢ����ը H++HSO3-=H2O+SO2�� ���Ӽ������ۼ� N2H4+2H2O2=N2��+4H2O
��������
A ԭ�ӵİ뾶��С������Ϊ��(H)��EԪ����ɫ��Ӧ��ɫΪ��ɫ������Ϊ��(Na)��CԪ���ǵؿ��к�������Ԫ�أ�����Ϊ��(O)��C��Fͬ���壬��FΪ��(S)��F��Gͬ������ԭ������F<G����GΪ��(Cl)��B��Cͬ������ԭ������B<C����BΪ��(N)��D�γɵķ���Ϊ��ԭ�ӷ��ӣ���ԭ����������C������Ϊ��(Ne)��A��C���γ����ֳ�����Һ̬������X��Y����Է�������X��Y������XΪH2O��YΪH2O2��
��1�������Ϸ�������ȷ��GԪ�أ�YΪH2O2��
��2��H2O2��ϡH2SO4�ữ��K2Cr2O7��Һ���ã�����O2��Cr2(SO4)3�ȡ�
��3��Al��NaOH��ˮ��Һ��Ӧ������H2�ȣ�H2��������ᷢ����ը��
��4��P��QΪNaHSO3��NaHSO4����ˮ��Һ�������ԣ����ߵ�Ħ��Ӧ���������ơ�ˮ�Ͷ�������
��5����H��N��ɵ�W���Ӻ���18�����ӣ����仯ѧʽΪN2H4����H2O2��Ӧ������N2��H2O��
��1�������Ϸ�����֪��GԪ��ΪCl��Y�ĵ���ʽΪ![]() ����Ϊ��Cl��
������Cl��![]() ��
��
��2��H2O2��ϡH2SO4�ữ��K2Cr2O7��Һ���ã�����O2��Cr2(SO4)3�ȣ��÷�Ӧ�����ӷ���ʽΪ3H2O2+Cr2O72-+8H+=2Cr3++3O2��+7H2O����Ϊ��3H2O2+Cr2O72-+8H+=2Cr3++3O2��+7H2O��
��3��Al��NaOH��ˮ��Һ��Ӧ������H2�ȣ��÷�Ӧ�����ӷ���ʽ2Al+2OH-+2H2O
=2A1O2-+3H2����ʹ������������ڵ�������������ᷢ����ը����Ϊ��2Al+2OH-+2H2O=2A1O2-+3H2����������ᷢ����ը��
��4��P��QΪNaHSO3��NaHSO4����ˮ��Һ�������ԣ����ߵ�Ħ��Ӧ���������ơ�ˮ�Ͷ������÷�Ӧ�����ӷ���ʽ��H++HSO3-=H2O+SO2�����������ξ����еĻ�ѧ������Ϊ���Ӽ������ۼ�����Ϊ��H++HSO3-=H2O+SO2�������Ӽ������ۼ���
��5����H��N��ɵ�W���Ӻ���18�����ӣ����仯ѧʽΪN2H4����H2O2��Ӧ������N2��H2O���÷�Ӧ�Ļ�ѧ����ʽΪN2H4+2H2O2=N2��+4H2O����Ϊ��N2H4+2H2O2=N2��+4H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ڳ�ʪ�����е����ܵ����������λ�ԭ�������£��ܱ��������ʴ����绯ѧ��ʴԭ����ͼʾ���������ԭ���й�˵���������
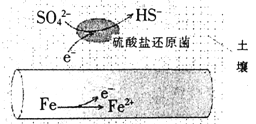
A. ������ӦΪ��SO42-+5H2O+8e-=HS-+9OH-
B. ����ů���Ĺܵ����������ฯʴ
C. ��������£�Fe��ʴ�����ղ���ΪFe2O3��xH2O
D. �ܵ���ˢ��п��������ӻ��ܵ��ĸ�ʴ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о�С��Ϊ��̽��һ����������![]() ��������Ԫ��
��������Ԫ��![]() ����ɺ����ʣ���Ʋ����������ʵ�飺
����ɺ����ʣ���Ʋ����������ʵ�飺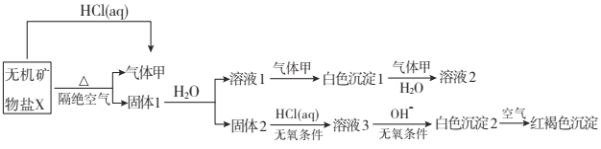
��ȡ![]() �ڶ��������м�������ȫ�ֽ⣬�õ�
�ڶ��������м�������ȫ�ֽ⣬�õ�![]() ����1����ش��������⣺
����1����ش��������⣺
(1)������ɫ����1�н���Ԫ�ص�ԭ�ӽṹʾ��ͼ__________��д������ĵ���ʽ __________��
(2)![]() �Ļ�ѧʽ��__________���ڶ��������м���X����ȫ�ֽ�Ļ�ѧ��Ӧ����ʽΪ__________��
�Ļ�ѧʽ��__________���ڶ��������м���X����ȫ�ֽ�Ļ�ѧ��Ӧ����ʽΪ__________��
(3)��ɫ����2�ڿ����б�ɺ��ɫ������ԭ����__________![]() �û�ѧ��Ӧ����ʽ��ʾ
�û�ѧ��Ӧ����ʽ��ʾ![]() ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Cu(s)��2H��(aq)===Cu2��(aq)��H2(g) ��H1
2H2O2(l)===2H2O(l)��O2(g) ��H2
2H2(g)��O2(g)===2H2O(l) ��H3
��ӦCu(s)��H2O2(l)��2H��(aq)===Cu2��(aq)��2H2O(l)����H��
A. ��H����H1��1/2��H2��1/2��H3 B. ��H����H1��1/2��H2��1/2��H3
C. ��H����H1��2��H2��2��H3 D. ��H��2��H1����H2����H3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)����Ӧ�ù㷺�Ľ�������������(��Ҫ�ɷ�ΪAl2O3����SiO2��Fe2O3������)Ϊԭ���Ʊ�����һ�ֹ����������£�

�����������ǵ������Al2O3������������������ʯī�����ģ�ԭ����_______________��
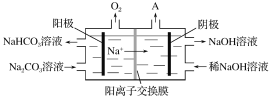
�����������ǵ��Na2CO3��Һ��ԭ����ͼ��ʾ�������ĵ缫��ӦʽΪ___________����������������A�Ļ�ѧʽΪ________��
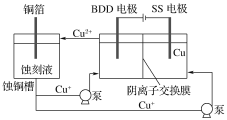
(2)�볣�淽����ͬ�����о�����HCl��CuCl2��ʴ��Һ��ʴͭ�����������������Cu����Һ��������ͼ��ʾ�������ɴﵽʴ��Һ���������ս���ͭ��Ŀ�ġ��˷����ò����������ʯBDD�缫����ֱ�Ӵ�ˮ���γ�һ�־���ǿ�����Ե��������ɻ�(HO��)����д��BDD�缫�ϵĵ缫��Ӧ________����һ����Ӧ��ʵ��ʴ��Һ��������д����ʴҺ���������ӷ���ʽ__________��
(3)������������������������Һ��ͬʱ�õ������ԭ������ͼ��ʾ(ͼ����HA����ʾ������ӣ�A����ʾ���������)��
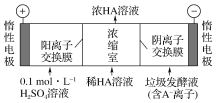
�������ĵ缫��ӦʽΪ____________��
�ڼ���Ũ�����еõ�Ũ�����ԭ����__________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݻ�Ϊ1.00L�������У�ͨ��һ������N2O4��������ӦN2O4(g)![]() 2NO2(g)�����¶����ߣ�����������ɫ���
2NO2(g)�����¶����ߣ�����������ɫ���
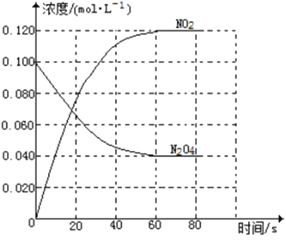
�ش��������⣺
��1����Ӧ����H______0��������������С��������100��ʱ����ϵ�и�����Ũ����ʱ��仯����ͼ��ʾ����0~60sʱ�Σ���Ӧ����v(N2O4)Ϊ___________molL-1s-1��Ӧ��ƽ�ⳣ��K1Ϊ___________��
��2��100��ʱ�ﵽƽ��ı䷴Ӧ�¶�ΪT��c(N2O4)��0.0020 molL-1s-1��ƽ�����ʽ��ͣ���10s�ִﵽƽ�⡣
��T_______100�������������������������������_____��
����ʽ�����¶�T�Ƿ�Ӧ��ƽ�ⳣ��K2___________
��3���¶�Tʱ��Ӧ��ƽ�����Ӧ�������ݻ�����һ�룬ƽ����___________����������Ӧ�������淴Ӧ���������ƶ����ж�������___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ����Ҫ�Ĺ�ҵԭ�ϣ�Һ�ȴ��������е�˵�������£�
��װ | ��ƿ |
����Ҫ�� | Զ�������ĩ���������ࡢ�������ʣ�������������� |
й©���� | NaOH��NaHSO3��Һ���� |
���н�����ʵ�ķ���ʽ����ȷ����
A. ������������ˮ������Cl2 + H2O![]() 2H+ + Cl��+ ClO��
2H+ + Cl��+ ClO��
B. ��ⱥ��ʳ��ˮ��ȡCl2��2Cl�� +2H2O![]() 2OH��+ H2��+Cl2��
2OH��+ H2��+Cl2��
C. Ũ��ˮ����й¶���������������̣�8NH3 + 3Cl2 === 6 NH4Cl + N2
D. ������й©��������NaHSO3��Һ�����ã�HSO3��+ Cl2 + H2O === SO42��+ 3H+ + 2Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Aminolevulinic acid��һ������С����ҩ���ṹΪ![]() ������˵��������ǣ� ��
������˵��������ǣ� ��
A. Aminolevulinic acid �ķ���ʽ��C5H7NO3
B. lmol�÷������ֻ����lmol���������ӳɷ�Ӧ
C. Aminolevulinic acid�ܷ���������Ӧ����ԭ��Ӧ��ȡ����Ӧ
D. Aminolevulinic acid�����к������ֹ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ᣨH2N2O2����һ�ֶ�Ԫ�ᣬ��������N2O���塣
��1�������£���0.01mol/L��NaOH��Һ�ζ�10mL0.01mol/L��H2N2O2��Һ�������ҺpH��NaOH��Һ����Ĺ�ϵ��ͼ��ʾ��

c��ʱ��Һ�и�����Ũ���ɴ�С��˳��Ϊ___��
��b��ʱ��Һ��c(N2O22-)___c(H2N2O2)���������������=������
��2����������Һ����������������Һ��ϣ����Եõ���ɫ����������������������÷�ɢϵ�еμ���������Һ������ɫ�����ͻ�ɫ��������ʱ����ɢϵ�� =___��
=___��
[��֪KSP��Ag2SO4)=1.4��10��5��KSP��Ag2N2O2)=5.6��10��9 ]��
��3�������£���b mol/L��������Һ�еμӵ������amol/L�����ᣬʹ��Һǡ�ó����ԣ������ĵ���ƽ�ⳣ��=___���ú�a��b�Ĵ���ʽ��ʾ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com