
| A. | 0.3 mol/L Na2SO4溶液中含有Na+和SO42-总物质的量为0.9mol | |
| B. | 当1L水吸收22.4LNH3时所得氨水的浓度不是1 mol/L,只有当22.4L NH3溶于水制得1L氨水时,其浓度才是1 mol/L | |
| C. | 10℃时0.5 mol/L的稀盐酸100mL,蒸发掉5g水,冷却到10℃时,其体积小于100mL,它的物质的量浓度大于0.5 mol/L | |
| D. | 10℃时0.5 mol/L的KCl饱和溶液100mL,蒸发掉5g水,冷却到10℃时,其体积小于100 mL,它的物质的量浓度仍为0.5 mol/L |
分析 A.溶液体积未知,不能确定离子物质的量;
B.氨气不一定处于标况下,22.4L氨气的物质的量不一定为1mol;
C.盐酸易挥发,加热蒸发后溶液浓度减小;
D.10℃时,100 mL 0.5 mol•L-1的KCl饱和溶液蒸发掉5g水,冷却到10℃时,剩余溶液仍为饱和溶液,溶液浓度与密度不变,溶液质量减小,则溶液体积减小.
解答 解:A.溶液体积未知,不能确定离子物质的量,故A错误;
B.氨气不一定处于标况下,22.4L氨气的物质的量不一定为1mol,故B错误;
C.盐酸易挥发,加热蒸发后溶液浓度减小,故C错误;
D.10℃时,100 mL 0.5 mol•L-1的KCl饱和溶液蒸发掉5g水,冷却到10℃时,剩余溶液仍为饱和溶液,溶液浓度不变,它的物质的量浓度仍为0.5 mol•L-1,溶液密度不变,而溶液质量减小,则溶液体积减小,故D正确,
故选:D.
点评 本题考查物质的量浓度计算、溶解度、气体摩尔体积等,难度不大,注意B选项中气体摩尔体积的使用条件.


科目:高中化学 来源: 题型:选择题
| A. | 用漂白粉可以净化饮用水 | |
| B. | 铜的金属性比铁弱,所以可用铜罐代替铁罐贮藏浓硝酸 | |
| C. | 合成纤维和光导纤维都是人工合成的有机高分子化合物 | |
| D. | 工业上可用石灰乳对煤燃烧形成的烟气进行脱硫,最终能制得石膏 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 80gCuO和Cu2S的混合物含有的Cu原子数一定是NA | |
| B. | 标准状况下,5.6L O2作为氧化剂时转移的电子数一定为NA | |
| C. | 常温常压下,14g C2H4和C3H6混合气体中含有的原子数为3NA | |
| D. | 25℃,1LpH=13的NaOH溶液中含有OH-的数目为 0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验编号 | HA物质的量浓度 (mol•L-1) | NaOH物质的量浓度 (mol•L-1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | C1 | 0.2 | pH=7 |
| 丙 | 0.1 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=10 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
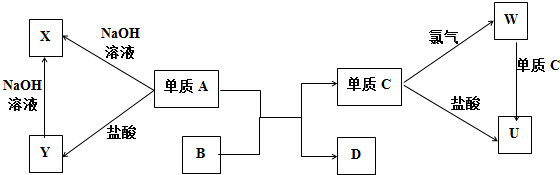
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酒精、硫酸钡和水分别属于电解质、强电解质和弱电解质 | |
| B. | Mg、Al、Cu可以分别用置换法、直接加热法和电解法冶炼得到 | |
| C. | 硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 | |
| D. | 天然气、沼气和水煤气分别属于化石能源、可再生能源和二次能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 整个反应过程中:c(H+)+c(Na+)+c(NH4+)=c(OH-)+c(SO42-) | |
| B. | 当滴入30mL NaOH溶液时(pH>7):c(NH4+)>c(NH3•H2O)>c(OH-)>c(H+) | |
| C. | 当滴入20mL NaOH溶液时:2c(SO42-)═c(NH3•H2O)+c(NH4+) | |
| D. | 当溶液呈中性时:c(NH4+)>c(SO42-)>c(Na+)>c(H+)=c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com