
科目:高中化学 来源:2016-2017学年江苏省苏州市高二上学期学业模拟三化学试卷(解析版) 题型:选择题
下列化学用语正确的是
A.乙醇分子的结构式:
B.氯原子的结构示意图: 
C.过氧化氢分子的电子式: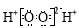
D.硫酸钠的电离方程式:Na2SO4=Na2+ + SO42?
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省钦州市高新区高一12月月考化学试卷(解析版) 题型:计算题
已知 Cl - 和Ag + 反应生成AgCl,每次新生成的AgCl中又有10%见光分解成单质银和氯气,氯气又可在水溶液中岐化成HClO 3 (为强酸)和HCl。而这样生成的Cl - 又与剩余的Ag + 作用生成沉淀,如此循环往复,直至最终。现有含1.1molNaCl的溶液,向其中加入足量AgNO 3 ,求最终能生成多少克难溶物(AgCl和Ag)?若最后溶液体积为1L,求溶液中H + 物质的量浓度是多少?
Cl - 和Ag + 反应生成AgCl,每次新生成的AgCl中又有10%见光分解成单质银和氯气,氯气又可在水溶液中岐化成HClO 3 (为强酸)和HCl。而这样生成的Cl - 又与剩余的Ag + 作用生成沉淀,如此循环往复,直至最终。现有含1.1molNaCl的溶液,向其中加入足量AgNO 3 ,求最终能生成多少克难溶物(AgCl和Ag)?若最后溶液体积为1L,求溶液中H + 物质的量浓度是多少?
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省钦州市高新区高一12月月考化学试卷(解析版) 题型:选择题
科学家发现C60 后,近年又合成了许多球形分子(富勒烯),如C50 、C70 、C120 、C540 等,它们互称为 ( )
A. 同系物 B. 同分异构体 C. 同素异形体 D. 同位素
查看答案和解析>>
科目:高中化学 来源:2017届四川省广元市高三上学期一诊化学试卷(解析版) 题型:实验题
高铁酸钾(K2FeO4)是一种集氧化,吸附,絮凝于一体的新型多功能水处理剂,高铁酸盐热 稳定性差。制备方法有湿法、干法两种,其原理如下表所示:
湿法的生产工艺如下:
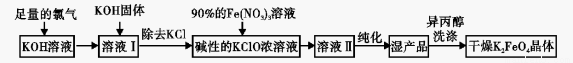
回答下列问题:
(1)K2FeO4 中Fe的化合价 ;实验室干法制备中选用的仪器是
A.蒸发皿 B.铁坩埚 C.氧化铝坩埚 D.陶瓷坩埚
(2)在温度较高时KOH与Cl2反应生成的是KClO3,写出在温度较高时KOH与Cl2反应的化学方程式
___________________;
(3)在溶液 I 中加入KOH 固体的目的是
A.使 KClO3 转化为 KClO
B.为下一步反应提供碱性的环境
C.KOH 固体溶解放热,有利于提高反应速率
D.与溶液 I 中过量的 Cl2 继续反应,生成更多的 KClO
(4)向次氯酸钾强碱浓溶液中加入 90%的 Fe(NO3)3,发生反应的离子方程式为:
① Fe3++3OH-═Fe(OH)3;② 。
(5)用异丙醇代替蒸馏水洗涤湿产品,除能洗去杂质外,其优点有 。
(6)如何判断 K2FeO4 晶体已经洗涤干净 。
(7)高铁酸钾(K2FeO4)作为水处理剂的优点之一是能除去悬浮杂质,配平该反应的离子方程式:
____FeO42-+ H2O= Fe(OH)3(胶体)+ O2↑+ ( )
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高二上期末化学卷(解析版) 题型:实验题
现使用酸碱中和滴定法测定市售白醋的总酸量(g·100mL-1)。
Ⅰ.实验步骤
(1)配制100ml待测白醋溶液:用 (填仪器名称)量取10.00 mL食用白醋,在烧杯中用水稀释后转移到 (填仪器名称)中定容,摇匀即得待测白醋溶液。
(2)用酸式滴定管取待测白醋溶液20.00 mL于锥形瓶中,向其中滴加2滴 作指示剂。

(3)读取盛装0.1000 mol·L-1 NaOH 溶液的碱式滴定管的初始读数。如果液面位置如图所示,则此时的读数为________mL。
(4)滴定。当___________________________时,停止滴定,并记录NaOH溶液的终读数。重复滴定3次。
Ⅱ.实验记录
滴定次数实验数据(mL) | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00[ | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
Ⅲ.数据处理与讨论
(1)按实验所得数据,可得c(市售白醋)= mol·L-1;
市售白醋总酸量= g·100 mL-1。
(2)在本实验的滴定过程中,下列操作会使实验结果偏大的是________填写序号)。
a. 碱式滴定管在滴定时未用标准NaOH溶液润洗
碱式滴定管在滴定时未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
c.锥形瓶中加入待测白醋溶液后,再加少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高二上期末化学卷(解析版) 题型:选择题
一定温度下,将一定量的冰醋酸加水稀释,稀释过程中溶液的导电性变化如图所示。则下列说法错误的是
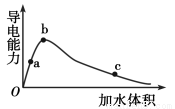
A.醋酸的电离程度:a<b<c
B.溶液的pH值:b>a>c
C.蘸取c点溶液滴在湿润的pH试纸上,测得pH值一定偏大
D.若分别向a、b、c三点的溶液中,加入同浓度的氢氧化钠溶液中和,消耗NaOH溶液的体积a=b=c
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高二上期末化学卷(解析版) 题型:选择题
关于水的离子积常数,下列说法不正确的是( )
A.100 ℃水中,c(H+)·c(OH-)=1×10-14
B.纯水中,25 ℃时,c(H+)·c(OH-)=1×10-14
C.25 ℃时,任何以水为溶剂的稀溶液中c(H+)·c(OH-)=1×10-14
D.KW值随温度升高而增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北定州中学高一承智班12月月考化学卷(解析版) 题型:选择题
饲养金鱼所用的自来水(经氯气消毒),需经日晒或放置一段时间后,再注入鱼缸。其主要目的是( )
A.提高水温,有利于金鱼生长
B.利用紫外线杀灭水中的细菌
C.增加水中氧气的含量
D.除去溶于水中Cl2,并促使次氯酸分解,以利于金鱼存活
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com