
 、-CHO
、-CHO ,故答案为:
,故答案为: ;
; ,故答案为:
,故答案为: ;
;

 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
| A、该溶液中由水电离出的c(H+)=1×10-3mol?L-1 |
| B、pH=2的HA溶液与pH=3的HCl溶液:c(HA)=10 c(HCl) |
| C、pH=3的HA溶液与pH=11的NaOH溶液等体积混合后所得的溶液中:c(Na+)>c(A-)>c(OH-)>c(H+) |
| D、0.1mol?L-1HA溶液与0.05mol?L-1NaOH溶液等体积混合后所得的溶液中:c(A-)+c(HA)=0.05mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHCO3+HCl |
| B、K2CO3+H2SO4 |
| C、Na2CO3+HNO3 |
| D、(NH4)2CO3+HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
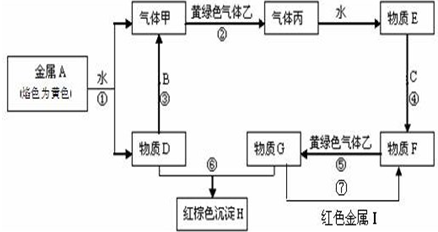 现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,金属A的焰色为黄色,金属B既能跟酸又能跟强碱反应,金属C在地壳中的含量居第四位.它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出).
现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,金属A的焰色为黄色,金属B既能跟酸又能跟强碱反应,金属C在地壳中的含量居第四位.它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出).查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知在常温常压下,A是固体,B、C、D、E是非金属单质且都是气体;C呈黄绿色;F是淡黄色的化合物;化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;J能使湿润的红色石蕊试纸变蓝.
如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知在常温常压下,A是固体,B、C、D、E是非金属单质且都是气体;C呈黄绿色;F是淡黄色的化合物;化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;J能使湿润的红色石蕊试纸变蓝.查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验 序号 |
0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
| B、c(H+)=c(NH3?H2O)+c(OH-) |
| C、加水稀释,溶液中所有离子的浓度均减小 |
| D、向溶液中加入少量CH3COONa固体,NH4+的水解程度增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com