
已知1~18号元素的离子aW3+、bX+、cY2-、dZ-具有相同的电子层结构,下列关系正确的是
A.质子数:c>d
B.离子的还原性:Y2->Z-
C.氢化物的稳定性:H2Y>HZ
D.原子半径:X<W
B
【解析】
试题分析:元素周期表前三周期元素的离子aW3+、bX+、cY2-、dZ-具有相同电子层结构,核外电子数相等,所以a-3=b-1=c+2=d+1,Y、Z为非金属,应处于第二周期,故Y为O元素,Z为F元素,W、X为金属应处于第三周期,W为Al元素,X为Na元素。A、由以上分析可知c=8,b=11,则质子数c<b,故A错误;B、非金属性F>O,非金属性越强,对应的单质的氧化性越强,则阴离子的还原性越弱,则离子还原性O2->F-,故B正确;C、非金属性F>O,非金属性越强氢化物越稳定性,氢化物稳定性为HF>H2O,故C错误;D、W为Al元素,X为Na元素,同周期随原子序数增大原子半径减小,故原子半径Na>Al,故D错误。
考点:本题考查元素的推断、原子结构、元素周期律。


 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源:2015届福建省高二上学期第二次月考化学试卷(解析版) 题型:选择题
可逆反应aA(g)+bB(g) cC(g)+dD(g) ΔH,同时符合下列两图中各曲线的是( )
cC(g)+dD(g) ΔH,同时符合下列两图中各曲线的是( )
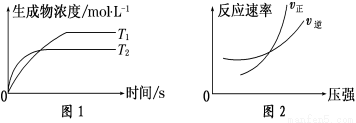
A.a+b>c+d T1>T2 ΔH>0 B.a+b>c+d T1<T2 ΔH<0
C.a+b<c+d T1>T2 ΔH>0 D.a+b<c+d T1<T2 ΔH<0
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
氯气是一种重要的工业原料。工业上利用反应在3Cl2 + 2NH3 = N2 + 6HCl检查氯气管道是否漏气。下列说法错误的是
A.该反应属于复分解反应
B.该反应利用了Cl2的强氧化性
C.若管道漏气遇氨就会产生白烟
D.生成1molN2有6mol电子转移
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期期中考试化学试卷(解析版) 题型:填空题
(12分)Ⅰ、现有常温条件下甲、乙、丙三种溶液,甲为0.1 mol·L-1的NaOH溶液,乙为0.1 mol·L-1的HCl溶液,丙为0.1 mol·L-1的CH3COOH溶液,试回答下列问题:
(1)甲溶液的pH=________;
(2)丙溶液中存在电离平衡为______________________(用电离平衡方程式表示);
(3)甲、乙、丙三种溶液中由水电离出的c(OH-)的大小关系为_________;
Ⅱ、某一元弱酸(用HA表示)在水中的电离方程式是HA ??H++A-,回答下列问题:
??H++A-,回答下列问题:
(1)向溶液中加入适量NaA固体,以上平衡将向________(填“正”、“逆”)反应方向移动,理由是_______________________________________。
(2)在25 ℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显________性(填“酸”、“碱”或“中”)。
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
现有如下几个离子方程式①CaCO3+2H+===Ca2++H2O+CO2↑
② 
③
④  ,
,
由此得出的如下结论中不正确的是
A. 与H+、Ca2+不能大量共存
与H+、Ca2+不能大量共存
B.H2CO3的酸性比HClO强,比H2SO3弱
C.H2SO3是一种强酸
D.H2CO3、HClO都属于弱酸
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
双羟基铝碳酸钠是医疗上常用的一种抑酸剂,其化学式是NaAl(OH)2CO3。关于该物质的说法正确的是
A.该物质属于两性氢氧化物
B.该物质是Al(OH)3和Na2CO3的混合物
C.1 mol NaAl(OH)2CO3最多可消耗3 mol H+
D.该药剂不适合于胃溃疡患者服用
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
向某晶体的溶液中加入含Fe2+的溶液无明显变化,当滴加几滴溴水后,混合液出现红色,下列结论中错误的是
A.Fe3+的氧化性比溴的氧化性强
B.该晶体中一定含有SCN-
C.Fe2+与SCN-不能形成红色化合物
D.Fe2+被溴氧化成Fe3+
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期第一次阶段考试化学试卷(解析版) 题型:实验题
(13分)过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。
Ⅰ.测定过氧化的含量,请填写下列空白:
移取10.00 ml密度为ρ g/mL的过氧化氢溶液至烧杯后全部将其转移到250 ml (填仪器名称)中,加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里。
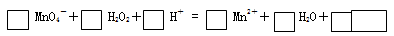
(3)滴定时,将高锰酸钾标准溶液注入 (填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是 。
(4)复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为 。
Ⅱ.探究过氧化氢的性质
该化学兴趣小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾演粉溶液、饱和硫化氢溶液,实验仪器及用品可自选。)请将他们的实验方法和实验现象填入下表:
实 验 内 容 | 实 验 方 法 | 实 验 现 象 |
验证氧化性 |
|
|
验证不稳定性 |
|
|
查看答案和解析>>
科目:高中化学 来源:2015届福建省、安溪一中高三上学期期中联考化学试卷(解析版) 题型:选择题
某溶液中可能含有H+、NH4+、Mg2+、Fe3+、Al3+、SO42- 等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随加入NaOH溶液的体积变化如图所示,

下列说法正确的是
A.d点溶液中含有的溶质有Na2SO4 、NaAlO2、NH3?H2O
B.原溶液中含有的Fe3+、Mg2+和Al3+的物质的量之比为1:1:1
C.ab段发生的离子反应为:Al3++3OH-= Al(OH)3↓, Mg2++2OH—= Mg(OH)2↓,Fe3++3OH-=Fe(OH)3↓
D.原溶液中含有的阳离子必定有H+、NH4+、Al3+,但不能肯定Mg2+和Fe3+中的哪一种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com