
某化学小组欲以CO2为主要原料,采用下图所示装置模拟“侯氏制碱法”制取NaHCO3,并对CO2与NaOH的反应进行探究。
【资料获悉】“侯氏制碱法”原理:NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl
然后再将NaHCO3制成Na2CO3。
【实验设计】

|
【实验探究】
(1)装置乙的作用是 。
(2)由装置丙中产生的NaHCO3制取Na2CO3时,NaHCO3转化为Na2CO3的化学方程式为
。
(3)若在(2)中灼烧时间较短,NaHCO3将分解不完全。取经短暂加热的NaHCO3 样品29.6 g完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中有关离子的物质的量的变化如下图所示。
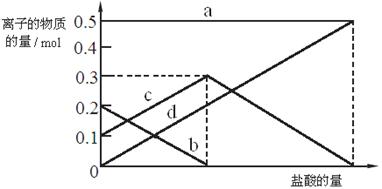
则曲线b对应的溶液中的离子是 (填离子符号);该样品中Na2CO3和NaHCO3的物质的量之比是 。
(4)若将装置甲产生的纯净的CO2 1.12 L(标准状况下)缓慢地全部通入到100 mL NaOH溶液中,充分反应后,将溶液低温蒸干,得到不含结晶水的固体W,其质量为4.86 g,则W的成分为 (填化学式),原NaOH溶液的物质的量浓度为 。
科目:高中化学 来源: 题型:
下列叙述与对应图式正确的是 ( )
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径 | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 主要化合价 | -2 | +2 | +1 | +5、-3 | +7、-1 | +1 | +5、-3 | +3 |



A.由下列短周期元素性质的数据推断元素③最高价氧化物对应的水化物碱性最强
B.图甲装置中,待镀铁制品应与电源负极相连
C.图乙表示H2与O2发生反应过程中的能量变化,则H2的燃烧热的热化学方程式为:
2H2(g)+O2(g)=2H2O(g) △H= — 483.6 kJ/mol
D.图丙表示某一放热反应,若使用催化剂E1、E2、△H都会发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等),下列分析推理正确的是
| 30 mL盐酸 | 30 mL盐酸 | 30 mL盐酸 | |
| m(混合物) | 9.2 g | 15.7 g | 27.6 g |
| V(CO2)(标况) | 2.24 L | 3.36 L | 3.36 L |
A.向50 mL盐酸中加入混合物27.6 g时,盐酸过量
B.根据表中数据不能计算出混合物中NaHCO3的质量分数
C.15.7 g混合物与盐酸恰好能完全反应 D.盐酸的物质的量浓度为5.0 mol / L
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值,则下列说法正确的是
A.1mol苯酚中“C=C”的个数为3 NA
B.2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA
C.标准状况下,1L戊烷充分燃烧后生成的气态产物的分子数为5/22.4 NA
D.常温常压下,22.4L丙烷所含有的共价键数目为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
某链状有机物分子中含有m个 —CH3 ,n个 —CH2— ,a个 ,其余为 —NH2,则—NH2的数目可能是
,其余为 —NH2,则—NH2的数目可能是
A.2n + 3-m B.a + 2-m C.n + m + a D.a + 2n + 2-m
查看答案和解析>>
科目:高中化学 来源: 题型:
下列几种说法中正确的是 ( )
A.摩尔是化学上常用的一个物理量
B.某物质含有6.02×1023个微粒,含有这个数目微粒的物质一定是1 mol
C.1摩尔氢气分子可以表示为1 mol H2
D.硫酸的摩尔质量为98 g
查看答案和解析>>
科目:高中化学 来源: 题型:
在硫酸铝、硫酸和硫酸镁的混合溶液1000mL中,c(Al3+) = 0.2mol/L,当加入等体积1.6mol/L KOH溶液时,生成的沉淀最多,再加入过量的KOH溶液后,经过滤、洗涤、干燥,得白色沉淀11.6g。则反应前的混合溶液中c(H2SO4)是 ( )
A. 0.20mol/L B.0.30mol/L C.0.40mol/L D.0.60mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com