
某有机物在O2中充分燃烧,生成36 g水和44 g CO2,则该有机物的组成必须满足的条件是( )
A.分子式一定是CH4
B.分子式一定是CH4O
C.分子式可能是CH4或CH4O
D.以上说法均不正确
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
在2 L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图。反应在t时刻达到平衡,依图所示:
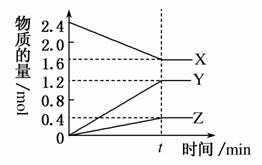
(1)该反应的化学方程式是___________________________。
(2)反应起始至t,Y的平均反应速率是_________________。
(3)X的转化率是_____________________________________。
(4)关于该反应的说法正确的是________。
A.到达t时刻反应已停止
B.在t时刻之前X的消耗速率大于它的生成速率
C.在t时刻正反应速率等于逆反应速率
D.在t时刻达到平衡是因为此时反应物总物质的量与生成物总物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
化学反应N2+3H2===2NH3的能量变化如图所示,该反应的热化学方程式是( )
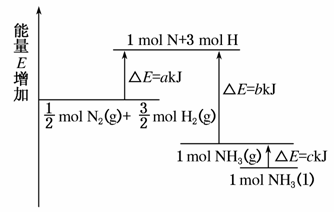
A.N2(g)+3H2(g)===2NH3(l)
ΔH=2(a-b-c)kJ·mol-1
B.N2(g)+3H2(g)===2NH3(g)
ΔH=2(b-a)kJ·mol-1
C.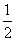 N2(g)+
N2(g)+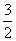 H2(g)===NH3(l)
H2(g)===NH3(l)
ΔH=(b+c-a)kJ·mol-1
D.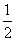 N2(g)+
N2(g)+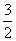 H2(g)===NH3(g)
H2(g)===NH3(g)
ΔH=(a+b)kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
核磁共振技术(NMR)已广泛应用于复杂分子结构的测定和医学诊断等高科技领域。已知只有质子数或中子数为奇数的原子核有NMR现象。试判断下列哪组原子均可产生NMR现象( )
A.18O、31P、23Na B.27Al、19F、12C
C.7Li、14N、35Cl D.4He、24Mg、28Si
查看答案和解析>>
科目:高中化学 来源: 题型:
一种由C,H,O三种元素组成的有机物,相对分子质量为70,红外光谱表征该分子中存在C===C键和C===O键,1H-NMR谱图如图所示:
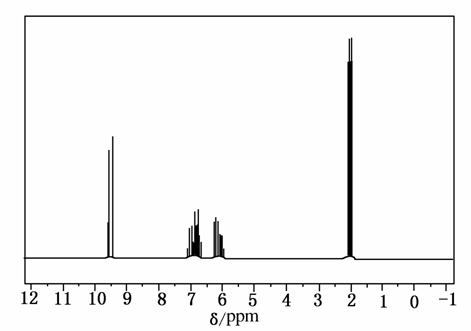
(1)写出该有机物的分子式:____________________。
(2)写出该有机物可能的一种结构简式:____________________
_____________________________________________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
可以由下列反应合成三聚氰胺:CaO+3C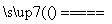 CaC2+CO↑,
CaC2+CO↑,
CaC2+N2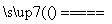 CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,
CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,
NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式:_____ ;CaCN2中阴离子为CN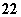 ,与CN
,与CN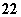 互为等电子体的
互为等电子体的
分子有N2O和________(填化学式),由此可以推知CN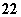 的空间构型为______ __。
的空间构型为______ __。
(2)尿素分子中C原子采取________杂化。
(3)三聚氰胺(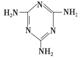 )俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸 (
)俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸 (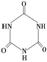 )后,三聚氰酸与三聚氰胺分子相互之间通过________结合,在肾脏内易形成结石。
)后,三聚氰酸与三聚氰胺分子相互之间通过________结合,在肾脏内易形成结石。
(4)CaO晶胞如图所示,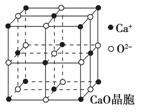 CaO晶体中Ca2+的配位数为 ,
CaO晶体中Ca2+的配位数为 ,
Ca2+采取的堆积方式为 ,
O2-处于Ca2+堆积形成的 空隙中;
CaO晶体和NaCl晶体的晶格能分别为:CaO 3401 kJ·mol-1、NaCl 786 kJ·mol-1。导致两者晶格能差异的主要原因是___________________________________。
(5)配位化合物K3[Fe(CN)n]遇亚铁离子会产生蓝色沉淀,因此可用于检验亚铁离子,已知铁原子的最外层电子数和配体提供电子数之和为14,求n= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
2X+Y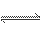 2Z(气) △H<0,温度升高,气体平均相对分子质量减小,说法正确的是( )
2Z(气) △H<0,温度升高,气体平均相对分子质量减小,说法正确的是( )
A.X和Y可能都是固体 B.X和Y一定都是气体
C.若Y为固体,X一定是气体 D.X和Y不可能都是气体
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物的结构简式为
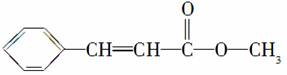 ,由此推测它最不可能具有的性质是( )
,由此推测它最不可能具有的性质是( )
A.能发生水解反应
B.能被新制Cu(OH)2氧化
C.能使溴水褪色
D.能加聚得高分子化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com