
下列有关说法正确的是( )
A.反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的△H<0
B.高温下,工业上用纯碱和石英砂制玻璃,说明硅酸的酸性强于碳酸
C.加热蒸干氯化铝溶液并灼烧残留物至质量不变,所得固体为氧化铝
D.高温下,用金属钠与氯化钾可以置换出金属钾,说明钠的金属性比钾强
【知识点】物质的性质及化学规律的解释G2 D1 C1
【答案解析】AC 解析:A、反应NH3(g)+HCl(g)=NH4Cl(s)是熵减的反应,在室温下可自发进行,一定是放热反应,△H<0,故A正确;B、因为反应在高温下进行,不能说明硅酸的酸性强于碳酸,根据反应Na2SiO3+H2O+CO2=Na2CO3+H2SiO3常温下进行,判断碳酸的酸性强于硅酸,故B错误;C、AlCl3+3H2O Al(OH)3+3HCl,HCl挥发,水解平衡右移,得氢氧化铝,灼烧残留物至质量不变,所得固体为氧化铝,故C正确;D、高温下,用金属钠与氯化钾可以置换出金属钾,是因为钾的沸点比钠的低,不能说明钠的金属性比钾强,故D错误。
Al(OH)3+3HCl,HCl挥发,水解平衡右移,得氢氧化铝,灼烧残留物至质量不变,所得固体为氧化铝,故C正确;D、高温下,用金属钠与氯化钾可以置换出金属钾,是因为钾的沸点比钠的低,不能说明钠的金属性比钾强,故D错误。
故答案选AC
【思路点拨】本题考查了物质的性质及化学规律的解释,注意钾的金属性比钠强,但是用金属钠与氯化钾可以置换出金属钾,学习中多思考出现反常的原因。


科目:高中化学 来源: 题型:
下列各组物质充分反应后过滤,将滤液加热、蒸干至质量不变,最终不能得到纯净物的是( )
A.向漂白粉浊液中通入过量的CO2
B.向带有氧化膜的铝片中加入盐酸
C.向含有1molCa(HCO3)2的溶液中加入1molNa2O2
D.向含有1molKAl(SO4)2的溶液中加入2molBa(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,常用于水的消毒以及纺织高漂白。过氧化氢法生产亚氯酸钠的流程图如下
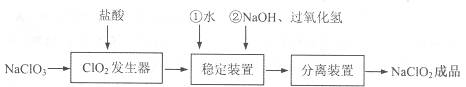
已知NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O且NaClO2在碱性条件下稳定性较高。试回答下列问题:
(1)在ClO2发生器中同时有氯气产生,则在发生器中发生反应的化学方程式为
(2)在NaClO2稳定装置中,H2O2作 (选填序号)。
A.氧化剂 B.还原剂
C.既作氧化剂又作还原剂 D.既不作氧化剂也不作还原剂
(3)在实验室模拟“固体分离装置”中的技术,必须进行的实验操作是 (按实验后顺序填写操作代号)。
A.过滤 B.加热 C.分液 D.蒸馏 E.冷却
(4)经查阅资料知道:当pH≤2.0时,ClO-2能被I完全还原成Cl—;
溶液中Na2S2O3能与I2反应生成NaI和Na2S4O6。
欲测定成品中NaClO2的含量,现进行如下操作:

①步骤Ⅱ中发生反应的离子方程式是 ,
步骤Ⅲ中达到滴定终点时的现象是 。
②若上述滴定操作中用去了V mL Na2S2O3溶液,则样品中NaClO2的质量分数 (用字母表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
次氯酸钠(NaClO)和藏氯酸钠(NaClO)都是重要的含氯消毒剂。
(l) NaClO2中,氯元素的化合价为________。
(2)某同学在实验室探究并制作一种家用环保型消毒液(NaClO)发生器,设计了如图的装置,用石墨作电极电解饱和氯化钠溶液。
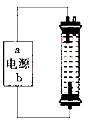
①通电时,为使Cl2被完全吸收,制得有较强杀菌能力的消毒液,则电源有b电极名称为_________(填“正”、“负”、“阴”或“阳”)投。
②装置中发生反应的有关化学方程式为________; 充分电解后溶液中各离子浓度由大到小顺序为____________。
③请说出使用该装置生产消毒液的一个优点和一个注意事项____ 。
(3)化学课外活动小组为测定某品牌“84消毒液”中NaClO的含量(单位体积溶液含有 NaCIO的质量),做了如下实验。已知:
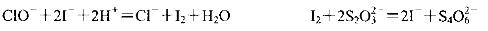
取10 mL该消毒液于锥形瓶中,迅速加入适量的硫酸酸化的碘化钾溶液,密封、充分
混合,暗处放置几分钟。然后加入几滴淀粉溶液,用c mol/L的硫代硫酸钠(Na2S2O3)
标准溶液滴定,平均用去VmL硫代硫酸钠溶液。则该“84消毒液”中NaCIO的含量
为_________g/mL(用含c、V的式子表示)。
(4)以下是过氧化氢法生产亚氯酸钠的工艺流程图:
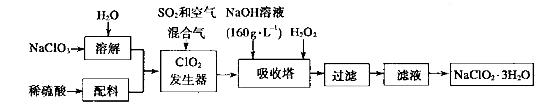
己知:(i)NaClO2 的溶解度随温度升高而增大,适当条件下可结晶析出: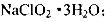
(ii)纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下较安全;
(iii) HClO2可看成是强酸。
①发生器中发生反应的离子方程式为___________________在发生器中鼓入空气的作用可能是__________________。
②吸收塔内的反应的化学方程式为__________________。在吸收塔中为防止被还原成NaCI,所用还原剂的还原性应适中。除外,还可以选择的还原剂_________(填序号)。
A.Na2O2 B.Na2S C.FeCl2
③从滤液中得到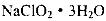 粗晶体的实验操作依次是_________(填序号)。
粗晶体的实验操作依次是_________(填序号)。
A.蒸馏 B.蒸发 C.灼烧 D.过滤 E.冷却结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
某学习兴趣小组讨论辨析以下说法,其中说法正确的是( )
①通过化学变化可以实现16O与18O间的相互转化
②灼烧钠的化合物时,火焰呈黄色,发生化学反应
③碱性氧化物一定是金属氧化物
④只由一种元素组成的物质一定为纯净物
⑤石墨和C60是同素异形体
⑥糖类、蛋白质、油脂属于天然高分子化合物
A.③⑤⑥ B.①② C.③⑤ D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
已知硫酸亚铁溶液中加入过氧化钠时发生反应:
4Fe2++4Na2O2+6H2O= 4Fe(OH)3↓+O2↑+8Na+ 则下列说法正确的是( )
A、该反应中 Fe2+是还原剂,O2 是还原产物
B、4molNa2O2 在反应中共得到 8NA 的电子
C、Fe(OH)3 既是氧化产物又是还原产物,每生成 4mol Fe(OH)3 反应过程中共转移电子 6mol
D、反应过程中可以看到白色沉淀转化为灰绿色再转化为红褐色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
)前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子数相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2。
回答下列问题:
(1)D2+的价层电子排布图为__________________。
(2)四种元素中第一电离能最小的是______,电负性最大的是____(填元素符号)。
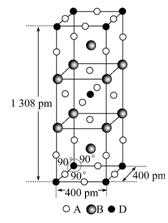
(3)A、B和D三种元素组成的一个化合物的晶胞如图所示。
①该化合物的化学式为________;D的配位数为______;
②列式计算该晶体的密度______g·cm-3。
(4)A-、B+和C3+三种离子组成的化合物B3CA6,其中化学键的类型有________;该化合物中存在一个复杂离子,该离子的化学式为________________,
配位体是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
电离常数(Ka或Kb)、溶度积常数(Ksp)是判断物质性质的重要常数,下列关于这些常数的计算或运用正确的是( )
A.某亚硫酸溶液pH=4.3,若忽略二级电离,则其一级电离平衡常数K1=1.0×10-8.60 mol2·L-2
B.Ka(HCN)<Ka(CH3COOH),说明同浓度时氢氰酸的酸性比醋酸强
C.Ksp(AgI)<Ksp(AgCl),向AgCl悬浊液中加入KI溶液会出现黄色沉淀
D.Ksp(AgCl)<Ksp(AgOH),说明AgOH和AgCl均不溶于稀硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
柠檬烯醇是一种实用香精,其结构简式如图所示。下列有关柠檬烯醇的说法正确的是

A.能与氢氧化钠溶液发生中和反应
B.能发生加成反应和取代反应
C.不能使酸性高锰酸钾溶液褪色
D.与对丙基苯甲醇( )互为同分异构体
)互为同分异构体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com