
【题目】
氮元素是自然界最丰富的元素,在化学中有很重要的地位。回答下列问题:
(1)基态氮原子的价层电子轨道表达式为_______________________。第二周期的元素中,第一电离能比氮元素的第一电离能小的元素共有__________种。
(2)预计于2017年发射的“嫦饿五号”探测器采用的长征五号运载火箭燃料为偏二甲肼[(CH3)2NNH2]。
(CIUXNH:中N’原子的杂化方式为__________。
(3)利用价层电子互斥理论解释NH3的立体构型为三角锥形的原因:__________________________。与NH3互为等电子体的离子为__________(填化学式,举一例即可)。
(4)在CuSO4溶液中加过量氨水后,再向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O,若要确定[Cu(NH3)4]SO4·H2O是晶体还是非晶体,最科学的方法是对其进行_______________________实验。lmol [Cu(NH3)4]2-含有的σ键的数目为__________。
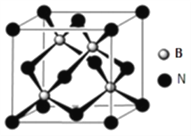
(5)氮化硼可用于制造飞机轴承,其晶胞如图所示,则处于晶胞顶点上的原子的配位数为__________。若立方氮化硼的密度为ρ g/cm3,氮化硼的摩尔质量为M,阿伏伽德罗常数为NA。如果硼原子的半径为r pm,则硼原子的空间利用率为__________。(用含有ρ、M、NA、r的式子表示)
【答案】 ![]() 5 sp3 NH3 中 N 原子成 3 个σ键,有一对孤对电子,价层电子对数为4,形成四面体的VSEPR模型,略去VSEPR模型中心原子上的孤电子对,氨气分子空间构型就是三角锥形 H3O+和 CH3- 等 X 射线衍射 16NA(或 9.632×1024) 4
5 sp3 NH3 中 N 原子成 3 个σ键,有一对孤对电子,价层电子对数为4,形成四面体的VSEPR模型,略去VSEPR模型中心原子上的孤电子对,氨气分子空间构型就是三角锥形 H3O+和 CH3- 等 X 射线衍射 16NA(或 9.632×1024) 4 ![]() ×100%
×100%
【解析】(1)基态氮原子的价层电子轨道表达式为![]() ;第二周期的元素中,第一电离能比氮元素的第一电离能小的元素共有Li、Be、B、C、O共5种;(2)[(CH3)2NNH2]中N’原子的杂化方式为 sp3 杂化;(3)利用价层电子互斥理论解释NH3的立体构型为三角锥形的原因:NH3 中 N 原子成 3 个σ键,有一对孤对电子,价层电子对数为4,形成四面体的VSEPR模型,略去VSEPR模型中心原子上的孤电子对,氨气分子空间构型就是三角锥形 ;可将中心原子N的核电荷放大和缩小的方法获得,与NH3互为等电子体的离子为H3O+和 CH3- 等;(4)确定物质是晶体还是非晶体,最科学的方法是对其进行X 射线衍射;lmol [Cu(NH3)4]2-含有的σ键的数目为:N―H是12mol,Cu―N键4mol,共16mol,或 9.632×1024。(5) 观察面心的N,每个N连有4个B原子,处于晶胞顶点上的原子的配位数为4;晶体中N位于晶胞体对角线的1/4处,将体心与下底面相对的两顶点相连可构成等腰三角形,距离最近的两个N原子相连有连线为三角形的中位线,所以晶体中最近的两个N原子的距离为底面对角线的一半,晶胞中N原子个数为
;第二周期的元素中,第一电离能比氮元素的第一电离能小的元素共有Li、Be、B、C、O共5种;(2)[(CH3)2NNH2]中N’原子的杂化方式为 sp3 杂化;(3)利用价层电子互斥理论解释NH3的立体构型为三角锥形的原因:NH3 中 N 原子成 3 个σ键,有一对孤对电子,价层电子对数为4,形成四面体的VSEPR模型,略去VSEPR模型中心原子上的孤电子对,氨气分子空间构型就是三角锥形 ;可将中心原子N的核电荷放大和缩小的方法获得,与NH3互为等电子体的离子为H3O+和 CH3- 等;(4)确定物质是晶体还是非晶体,最科学的方法是对其进行X 射线衍射;lmol [Cu(NH3)4]2-含有的σ键的数目为:N―H是12mol,Cu―N键4mol,共16mol,或 9.632×1024。(5) 观察面心的N,每个N连有4个B原子,处于晶胞顶点上的原子的配位数为4;晶体中N位于晶胞体对角线的1/4处,将体心与下底面相对的两顶点相连可构成等腰三角形,距离最近的两个N原子相连有连线为三角形的中位线,所以晶体中最近的两个N原子的距离为底面对角线的一半,晶胞中N原子个数为![]() ,B原子个数为4,4个B原子的体积为:
,B原子个数为4,4个B原子的体积为:![]() ,晶胞体积
,晶胞体积![]() ,B的空间利用率为
,B的空间利用率为![]() ×100%=
×100%=![]() ×100%。
×100%。


 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
【题目】已知在25℃的水溶液中,AgCl、AgBr、AgI均难溶于水,且Ksp(AgCl)=1.8×10-10,Ksp(AgBr)=1.0×10-12,Ksp(AgI)=8.7×10-17;
(1)若向AgBr的饱和溶液中加入少量的AgCl固体,则c(Br-)_______________。(填“增大”、“减小”或“不变”)。
(2)在25℃时,若取0.188g的AgBr(相对分子质量188)固体放入100mL水中(忽略溶液体积的变化),则溶液中Br-的物质的量浓度为_____________。
(3)①由上述Ksp判断,在上述(2)的体系中,能否实现AgBr向AgI的转化_______(填“能”或“否”),简述理由:_____________________________________________________________。
②若某KCl溶液的浓度为1.0×10-2mol·L-1,将等体积的该KCl溶液与AgNO3溶液混合,则生成沉淀所需AgNO3溶液的最小浓度为__________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分两步以1-溴丁烷和必要的无机试剂制取1,2-二溴丁烷(CH3CH2CHBrCH2Br),写出有关反应的方程式。
_____________________________________________,________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为证明溴乙烷在NaOH的乙醇溶液中加热发生消去反应,可将反应后的气体通入
A.溴水B.AgNO3溶液
C.酸性KMnO4溶液D.酸化的AgNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气和氯气是重要的工业原料,某兴趣小组设计了相关实验探究它们的某些性质。实验一:用氨气认识喷泉实验的原理,并测定电离平衡常数K(NH3H2O)。


(1)检査图1的装置Ⅰ的气密性的方法是_____________________________________________。
(2)喷泉实验结束后,发现三颈烧瓶未充满水(假如装置的气密性良好),原因是_______________。用___________(填仪器名称)量取25.00mL喷泉实验后的氨水至锥形瓶中,用0.0500mol/L盐酸滴定测定氨水的浓度,滴定曲线如图2所示。下列关于该滴定实验的说法中正确的是__________(选填字母)。
A.当pH=7.0时,氨水与盐酸恰好中和 B.选择酚酞作为指示剂,测定结果偏低
C.酸式滴定管未用盐酸润洗会导致测定结果偏低 D.当 pH=11.0 时,K(NH3H2O)约为2.2×10-5
实验二:拟用如下装置设计实验来探究纯净、干燥的氯气与氨气的反应。

(3)A中所发生反应的化学方程式为__________________________________________________。
(4)上图中的装置连接顺序为A→_________→_________→_________→_________→_________ (用大写字母表示)。若按照正确顺序连接实验装置后,整套实验装置存在的主要缺点是________________________。
(5)写出F装置中的反应的一种工业用途_________________________________________。
(6)反应完成后,F装罝中底部有固体物质生成。请利用该固体物质设计一个实验方案证明NH3H2O为弱碱(其余实验用品自选)_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含大量NH4+、Na+、HCO3-、CO32-、CH3COO-离子,其中加入足量的Na2O2固体后,溶液中离子浓度基本保持不变的是(假设溶液体积无变化)
A. Na+ B. CO32-、NH4+
C. CH3COO- D. CH3COO-、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼镁矿(主要成分为Mg2B2O5·H2O)与硫酸反应可制备硼酸(H3BO3),下列措施能增大该反应速率的是( )
A. 增加反应时间 B. 降低反应温度
C. 减小H2SO4浓度 D. 减小硼镁矿颗粒粒度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】感光性高分子作为新材料在各种领域中得到广泛应用。感光高分子F的一种合成路线如下:

已知:
A的相对分子质量为60,氧元素的质量分数为0.533,核磁共振氢谱显示为两组峰,峰面积比为1∶3。
回答下列问题:
(1)A的结构简式为____________,D的化学名称是____________。
(2)①、②的反应类型分别是____________、____________。
(3)反应③的化学方程式是_____________。
(4)F中的官能团有______________(填官能团名称)。
(5)芳香族化合物G是E的同分异构体,能发生银镜反应且分子中只有4种不同化学环境的氢。写出三种G的结构简式:______________。
(6)写出以甲苯为原料(其他无机试剂任选)制备化合物D的合成路线(箭头上方标试剂,下方标条件)。
__________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com