
分析 (1)依据热化学方程式和盖斯定律计算所需化学方程式;
(2)歧化反应磷元素升高为次磷酸盐,磷元素化合价为+1价,降低的只能为负价,则为氢化物;
(3)H3PO4?H++H2PO4-K1=7.1×10-3;H2PO4-?H++HPO42-K2=6.3×10-8;HPO42-?H++HPO43-K3=4.2×10-13;上一级电离产生的H+对下一级电离有抑制作用;为获得尽可能纯的NaH2PO4,需H2PO4-浓度最大,根据K1、K2、以及pH=-lgc(H+)计算;
若向Na2HPO4溶液中加入足量的CaCl2溶液,HPO42-离子和Ca2+离子反应生成沉淀,促进HPO42-的电离,溶液显示酸性;
(4)Cu元素的化合价由+2价降低到+1价,CuSO4是氧化剂,P4部分磷元素由0价降低到-3价,部分磷元素由0价升高到+5价,磷元素的化合价既升高又降低,所以P4既是氧化剂又是还原剂,若有11molP4参加反应,其中5mol的P4做氧化剂,60mol硫酸铜做氧化剂,只有6mol的P4做还原剂,结合电子守恒来解答.
解答 解:(1)①4Ca3(PO4)2(s)+10C(s)=12CaO(s)+2P4(s)+10CO2(g)△H1=+Q1kJ•mol-1
②CaO(s)+SiO2(s)=CaSiO3(s)△H2=-Q2 kJ•mol-1
③CO2(g)+C(s)=2CO(g)△H3=+Q3kJ•mol-1
依据热化学方程式和盖斯定律计算得到①×$\frac{1}{2}$+③+②×6得到化学方程式为:2Ca3(PO4)2+6SiO2+10C$\frac{\underline{\;高温\;}}{\;}$6CaSiO3+P4+10CO;
故答案为:2Ca3(PO4)2+6SiO2+10C$\frac{\underline{\;高温\;}}{\;}$6CaSiO3+P4+10CO;
(2)白磷在热的浓氢氧化钾溶液中岐化得到一种次磷酸盐(KH2PO2)和一种气体,歧化反应磷元素升高为次磷酸盐,磷元素化合价为+1价,降低的只能为负价,则为氢化物PH3;
故答案为:PH3;
(3)为获得尽可能纯的NaH2PO4,需配制磷酸、磷酸二氢钠的缓冲溶液,当溶液全部为磷酸溶液时,磷酸以第一步电离为主,所以H3PO4?H++H2PO4-K1=7.1×10-3;PH=-lgc(H+)=3-lg7.1≈2.1,
当溶液全部为NaH2PO4溶液时,H2PO4-?H++HPO42-K2=6.3×10-8,所以pH=-lgc(H+)=8-lg6.3≈7.2,
所以pH应控制介于2.1~7.2之间;HPO42-离子既能发生电离又能发生水解,电离反应式为HPO42-?PO43-+H+,水解反应式为HPO42-+H2O?H2PO4-+OH-,溶液呈碱性,说明水解程度大于电离程度;由于HPO42-离子和Ca2+离子反应生成沉淀:3Ca2++2HPO42-═Ca3(PO4)2↓+2H+,促进HPO42-的电离,溶液则显酸性;
故答案为:2.1~7.2;3Ca2++2HPO42-=Ca3(PO4 )2↓+2H+.
(4)Cu元素的化合价由+2价降低到+1价,CuSO4是氧化剂,P4部分磷元素由0价降低到-3价,部分磷元素由0价升高到+5价,磷元素的化合价既升高又降低,所以P4既是氧化剂又是还原剂,若有11molP4参加反应,其中5mol的P4做氧化剂,60mol硫酸铜做氧化剂,只有6mol的P4做还原剂,
则由电子守恒可知,有60mol的CuSO4参加反应,60molCuSO4得到60mol电子,1molP4参加反应失去20mol电子,所以60molCuSO4能氧化白磷的物质的量是$\frac{60}{20}$=3mol,
故答案为:3mol.
点评 本题考查反应热的计算、PH计算、氧化还原反应电子转移计算,离子方程式的书写等知识,侧重于学生的分析能力和计算能力的考查,为高考常见题型和高频考点,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 白炽灯工作时,电能全部转化为光能 | |
| B. | 风力发电时,风能主要转化为电能 | |
| C. | 煤燃烧时,化学能主要转化热能 | |
| D. | 电解水生成H2和O2时,电能主要转化为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该元素原子中共有25个电子 | B. | 该元素原子核外有4个能层 | ||
| C. | 该元素原子最外层共有2个电子 | D. | 该元素原子M电子层共有8个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑤⑧⑨ | B. | ①②③⑥⑦⑨ | C. | ①②③④⑥⑦⑨⑩ | D. | ①②③④⑥⑦⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
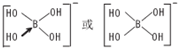 ,
,查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉、纤维素、蛋白质均属于天然高分子化合物,水解产物都只有一种 | |
| B. | 油脂在碱性条件下水解属于皂化反应,酸性条件下的水解产物为甘油和高级脂肪酸 | |
| C. | 用pH计、电导率仪(一种测量溶液导电能力的仪器)均可监测乙酸乙酯的水解程度 | |
| D. | TiCl4+(x+2)H2O$\stackrel{△}{?}$TiO2•xH2O↓+4HCl 属于水解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com