
����Ŀ�����������Ʊ�ʱ���ȼ��װ�õ������ԣ����и�ͼ��ʾװ�ã��϶������������Լ��Ҫ����ǡ� ����
������������ѧ��ѧʵ���г����ļ���������
a����Ͳ b������ƿ c����Һ©�� d��������ƽ e���¶ȼ�
��1�����б�ʾ������ʹ���¶ȵ��� �����ţ���
��2����ȡ10.5g������Ʒ��1g����ʹ�����룩ʱ������Ʒ��������ƽ�����̣���������Ʒ��ʵ������Ϊ�� ��g��
��3��ʹ��ǰҪ��������Ƿ�©Һ���ǡ� �����ţ���
����ʵ������Ҫ95mL 1.0molL��1ϡ���ᣬ����98%��Ũ���ᣨ���ܶ�Ϊ1.84g/mL�����������ƣ���ʵ�������У�
A��100mL��Ͳ B��������ƽ C�������� D��250mL����ƿ
E��10mL��Ͳ F����ͷ�ι� G��50mL�ձ� H��100mL����ƿ
��1������ȡŨ��������Ϊ�� ��mL��
��2��ʵ��ʱѡ�õ������У�����ţ���
��3�����ƹ����У����������ʹ���ƽ��ƫ�ߵ��ǣ�����ţ���
A����ϡ�͵�����Һת��������ƿ��δϴ���ձ��Ͳ�������
B�����ձ��ڵ�ϡ����������ƿ��ת��ʱ�����������ʹ����ϡ���ὦ��ƿ�⣮
C��δ��ȴ�����¾Ͷ��ݣ�
D���ý�ͷ�ιܼ�ˮʱ�����ӹ۲���Һ��Һ��������ƿ�̶����У�
E������ƿʹ��ʱδ����
F�����ݺ���ҡ�ȡ����ã�����Һ����ڿ̶��ߣ��ټ�����ˮ�����̶��ߣ�
���𰸡�D��ab��9.5��bc��5.4��C��E��F��G��H��CD
������������A��B��C�����γɵ��ȶ���Һ�������ж�װ�õ��������Ƿ���ã�Dװ����Һ�汣��ˮƽʱ��������ѹ���ұ�װ���е�ѹǿ��ȣ�û��ѹǿ�����Բ��ܼ���װ�õ������ԣ����Դ��ǣ�D��
����1��Һ���������¶ȵ�Ӱ�죬�¶Ȳ�ͬʹ������Ͳ��ȡ��Һ�塢����ƿ�е�Һ��������ͬ�����²��������Դ��ǣ�ab��
��2����������ʱ���������ֵҪ��������һ�ߣ�����������ŷ�λ��ʱ�������������������������������������������10.5g����ʱ�������������10g�������������ֵ��0.5g�������������10g��0.5g=9.5g�����Դ��ǣ�9.5��
��3��d��e����ʢװҺ�壬�ʴ���aʹ��ʱ�������©Һ���ʴ���b��c�����ӣ�������©Һ�Ŀ��ܣ�����Ҫ����Ƿ�©Һ�����Դ��ǣ�bc��
����1������ϡ��ǰ�����ʵ����ʵ���������ʽ������ȡ��Һ�����ΪxmL������ʽΪ��
0.1L��1.0molL��1=![]() x=5.4�����Դ��ǣ�5.4��
x=5.4�����Դ��ǣ�5.4��
��2����ȡ5.4mL������10mL��Ͳ��50mL���ձ�����ϡ����Һ���������������衢��������ͷ�ιܵ������Ƕ��ݣ�100mL����ƿ��������������Һ��
���Դ��ǣ�C��E��F��G��H��
��3���������ʵ���Ũ�ȹ�ʽC=![]() �жϣ�
�жϣ�
A��nƫСV���䣬�������õ���ҺŨ��ƫ�ͣ�
B��nƫСV���䣬�������õ���ҺŨ��ƫ�ͣ�
C����Һ���������������ʣ��������õ���Һ���ƫСn���䣬Ũ��ƫ��
D�����õ���Һ���ƫСn���䣬Ũ��ƫ��
E����n��V��Ӱ�죬���Զ�Ũ����Ӱ�죻
F��Vƫ��n���䣬������Һ��Ũ��ƫС��
���Դ��ǣ�CD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ұ��������ԭ���У������Ȼ�ԭ�����ǣ� ��
A.2Ag2O ![]() 4Ag+O2��
4Ag+O2��
B.Fe2O3+3CO ![]() 2Fe+3CO2��
2Fe+3CO2��
C.Fe+CuSO4=FeSO4+Cu
D.MgC12 ![]() Mg+C12��
Mg+C12��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�ҳ����ý�ҩ�������ڸ߷��������ϣ��Ƴɻ��ͳ�Чҩ���֪ij�ֽ�����ʹ��ҩ���ṹ��ʽΪA���������ӵ��߷��Ӿۺ���B�ϣ��γɻ��ͳ�Чҩ��C��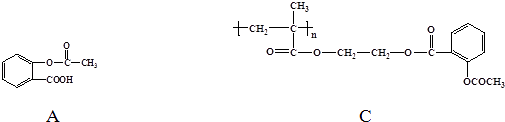
��1�����Ӿۺ���B�Ľṹ��ʽΪ ��
��2��A��B��Ӧ����C���л���Ӧ������ ��
��3��A��ˮ�������д�ṹ��ʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��Al2O3��Fe3O4��Al��Cu�е�ij���ַ�ĩ��϶��ɣ���Ƴɷַ����������£����з�������ȷ���ǣ� ��
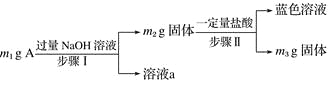
A. ��m1>m2ʱ����Һa��������ֻ��1��
B. ������ɫ��Һ�����ӷ���ʽ��Cu��2Fe3��===Cu2����2Fe2��
C. Ҫȷ����������Ƿ�Al����ȡA��������ϡHCl
D. ��m2��m3��2.96 g��Fe3O4����������Ϊ2.32 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һƿ�ס��ҵĻ�����֪���ǵ��������±����ݴˣ����ס��һ���������ѷ����ǣ� ��
���� | �۵� | �е� | �ܶ� | �ܽ��� |
�� | -11.5�� | 198�� | 1.11 g/mL-1 | �ס��һ��� |
�� | -17.9�� | 290�� | 1.26 g/mL-1 |
A.��ȡ��B.����C.��Һ��D.�ᾧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ��X��Y��Z��R��T��ԭ�Ӱ뾶��ԭ��������ϵ����ͼ��ʾ��Rԭ�������������ǵ��Ӳ�����2����Y��Z���γ�Z2Y��Z2Y2�����ӻ����Z��T�γɵĻ�����Z2T���ƻ�ˮ�ĵ���ƽ�⡣�����ƶ���ȷ���ǣ� ��
A.ԭ�Ӱ뾶�����Ӱ뾶�����㣺Y<Z
B.�⻯��ķе㲻һ���ǣ�Y>R
C.����������Ӧˮ��������ԣ�T<R
D.��X��R��Y��Z����Ԫ����ɵĻ�����ˮ��Һһ���Լ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E���������о�����ͬһ�ַǽ���Ԫ�أ������ܷ�����ͼ��ʾ��ת����ϵ������Ԫ����R��ʾ����AΪR�������D��NaOH��Һ��Ӧ����C��H2��
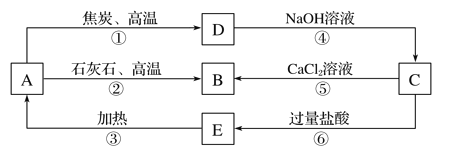
��ش�
(1)д����Ӧ���ʵĻ�ѧʽ��A________________�� C________________�� E________________��
(2)��Ӧ�ٵĻ�ѧ����ʽΪ_______________________________________��
(3)��Ӧ�ܵ����ӷ���ʽΪ_____________________________________��
(4)H2CO3������ǿ��E�ģ��������ӷ���ʽ����֤����_______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ������ġ���������������ʹ�����������˸��ϸ�ķ������ݣ�
��1����ȼú�м��� �� �ɴ����������е�SO2������
��2��Ư������������ˮ��ɱ��������Ư�۵���Ч�ɷ������ѧʽ����
��3���Ͼɵ�ش�������������ؽ�����Ⱦ��������ˮ�е��ؽ�����Ⱦ����ó����������磬����Ǧ��Pb2+����ˮ�м���Na2SʹPb2+ת��Ϊ���ѧʽ����������ȥ��
��4���������żҿ����ѳɹ����2022�궬�»ᣬĿǰ��������������ȫ�����ƿ�������������ָ�겻�ڿ����������淶Χ�ڵ���������ĸ����a��SO2Ũ�� b��CO2Ũ�� c�������������
��5��������������γ���Ҫ���������ŷŵ�β�����£�����β���еĵ�����������ð��������������磬��������������ڴ��������·�Ӧ���ɵľ��ǶԿ�������Ⱦ�����ʣ���д����ʱ���������������Ӧ�Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йص������Һ��˵����ȷ���ǣ� ��
A.Na2SO3��Һ��ˮϡ�ͺ�pH��KW����С
B.0.1molL��1Na2CO3��Һ�У�c��OH����=c��H+��+c��HCO3����+2c��H2CO3��
C.Ũ�ȷֱ�Ϊ0.2molL��1��0.1molL��1��CH3COOH��Һ�У�c��H+��֮�ȵ���2��1
D.�����£�PH=12�İ�ˮ��pH=2��H2SO4��Һ�������Ϻ���Һ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com