
 钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一.
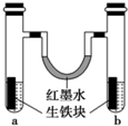
钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一.分析 生铁中含有铁和碳,铁、碳和电解质溶液构成了原电池,较活泼的金属铁作负极,碳作正极,负极上失电子发生氧化反应,正极上得电子发生还原反应;a、b试管内分别盛有氯化铵(显酸性)溶液和食盐水,左边试管中是酸性溶液,发生析氢腐蚀,右边试管中是中性溶液发生吸氧腐蚀.
(1)红墨水柱两边的液面变为左低右高,左边发生析氢腐蚀,右边发生吸氧腐蚀;
(2)中性或弱酸性条件下,钢铁发生吸氧腐蚀,b试管中是中性溶液食盐水,铁发生的吸氧腐蚀,负极上铁失电子发生氧化反应,正极上氧气得电子发生还原反应,正极和负极反应加和得到总反应.
解答 解:a、b试管内分别盛有氯化铵(显酸性)溶液和食盐水,左边a试管中是酸性溶液,发生析氢腐蚀,右边b试管中是中性溶液发生吸氧腐蚀,这两种腐蚀都属于电化学腐蚀,
故答案为:电化学;
(1)导致U型管内红墨水左低右高,左边试管内气体的压强不大,右边试管内气体的氧气减小,所以左边试管中是酸性溶液氯化铵(显酸性),发生析氢腐蚀,右边试管中是中性溶液食盐水,发生吸氧腐蚀,
故答案为:b;
(2)b试管中是中性溶液食盐水,铁作负极,发生失电子的氧化反应,即Fe=Fe2++2e-,碳作正极,正极上氧气得电子发生还原反应,电极反应式为:2H2O+O2+4e-=4OH-,
所以总反应为2Fe+2H2O+O2═2Fe(OH)2,
故答案为:吸氧2H2O+O2+4e-=4OH-,;2Fe+O2+2H2O=2Fe(OH)2.
点评 本题考查了金属的腐蚀与防护,明确生铁发生吸氧腐蚀和析氢腐蚀的环境是解本题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | lmolNacl 固体中含有NA个Na+ | |
| B. | 18gD2O和18gH2 O中含有的质子数均为10NA | |
| C. | 标准状况下2.24LH2O 含有的共价键数为0.2NA | |
| D. | 密闭容答中2molNO 与lmolO2充分反应,产物的分子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑥ | B. | ①②⑤⑥ | C. | ③⑤⑥④ | D. | ①③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3、BaCl2、HCl | B. | BaCl2、Na2CO3、H2SO4 | ||
| C. | BaCl2、Na2CO3、HCl | D. | Ba(NO3)2、Na2CO3、HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只测定它的C、H比 | |
| B. | 只需证明它完全燃烧后产物只有H2O和CO2 | |
| C. | 只测定其燃烧产物中H2O与CO2的物质的量的比值 | |
| D. | 测定该试样的质量及试样完全燃烧后生成CO2和H2O的质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ②③④ | C. | ②③⑤ | D. | ②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.03 mol | B. | 0.04 mol | C. | 0.05 mol | D. | 0.06 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
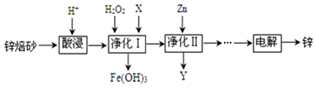
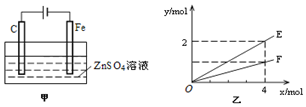
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com