
| A. | 用1g98%的浓硫酸加4g水配制成19.6%的硫酸 | |
| B. | 配制一定物质的量浓度的硫酸溶液时,定容后,塞好塞子倒转摇匀后,发现液面低于刻度线 | |
| C. | 10%的硫酸和90%的硫酸等体积混合配制50%的硫酸溶液 | |
| D. | 质量分数为5x%和x%的两种氨水等体积混合配制成3x%的氨水 |
分析 A.根据溶剂质量不变,溶液质量由1g变为5g,质量分数变为原先的$\frac{1}{5}$;
B.由于容量瓶刻度线上方有部分残留溶液,所以摇匀后液面会低于刻度线,属于正确现象;
C.硫酸的质量分数越大,溶质的密度越大,10%的硫酸和90%的硫酸等体积混合后溶质质量分数大于两溶液质量分数的平均值;
D.氨水密度小于1,5x%和x%的两种氨水等体积混合后溶液质量分数小于两溶液质量分数的平均值.
解答 解:A.用1g 98%的浓硫酸加4g水,所得溶液中硫酸的质量分数为:$\frac{1×98%}{1+5}$×100%=19.6%,该操作合理,浓度正确,故A不选;
B.配制一定物质的量浓度的硫酸溶液时,定容后,塞好塞子倒转摇匀后,由于容量瓶刻度线上方有残留的溶液,所以液面会低于刻度线,不会影响配制结果,故B不选;
C.硫酸的密度大于1,10%的硫酸和90%的硫酸等体积混合,所得溶液的质量分数大于50%,故C选;
D.氨水密度小于1,质量分数为5x%和x%的两种氨水等体积混合所得溶液质量分数小于3x%,故D不选;
故选:C.
点评 本题考查了配制一定浓度的溶液方法及误差分析的判断,题目难度中等,注意掌握配制一定浓度的溶液步骤,明确分析误差的方法与技巧,试题培养了学生灵活应用所学知识的能力.


 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:解答题
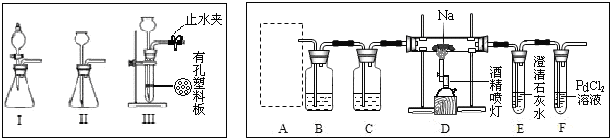
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
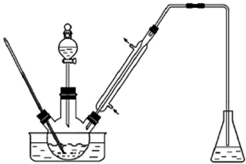 实验室以苯甲醛为原料制备间溴苯甲醛(实验装置主要部分如图,相关物质的沸点见附表),附表相关物质的沸点(101kPa)
实验室以苯甲醛为原料制备间溴苯甲醛(实验装置主要部分如图,相关物质的沸点见附表),附表相关物质的沸点(101kPa)| 物质 | 沸点/℃ | 物质 | 沸点/℃ |
| 溴 | 58.8 | 1,2-二氯乙烷 | 83.5 |
| 苯甲醛 | 179 | 间溴苯甲醛 | 229 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
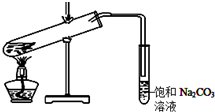 某学生做乙酸乙酯的制备实验装置如图所示.
某学生做乙酸乙酯的制备实验装置如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ④ | ⑥ | ||||||
| 3 | ① | ② | ③ | ⑤ | ⑦ | ⑧ |
 .
. .
. ,形成的晶体是离子晶体.
,形成的晶体是离子晶体.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
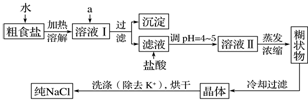
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl固体(KNO3)溶解配成热饱和溶液、降温结晶 | |
| B. | CO(水蒸气)通过浓硫酸的洗气瓶 | |
| C. | CaO固体(CaCO3)高温煅烧 | |
| D. | KCl固体(MnO2)溶解、过滤、蒸发 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O(g)=H2(g)+$\frac{1}{2}$ O2(g)△H=+242 kJ/mol | B. | 2H2(g)+O2(g)=2H2O (l)△H=-484 kJ/mol | ||
| C. | H2(g)+$\frac{1}{2}$ O2(g)=H2O (g)△H=-242 kJ | D. | 2H2(g)+O2(g)=2H2O (g)△H=+484 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molOH-的质量是17g/mol | |
| B. | CO2的摩尔质量是44 | |
| C. | 标况下气体的摩尔体积是22.4L | |
| D. | 12gC-12中含的C原子数是阿伏伽德罗常数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com