
| A. | a-c=m-n | B. | a-b=n-m | C. | c-d=m+n | D. | b-d=m+n |
分析 由aXm+、bYn+、cZn-、dRm-四种离子的电子层结构相同知,这四种离子的核外电子数相等,根据构成离子的原子序数、电荷数、质子数之间的关系判断.
解答 解:由aXm+、bYn+、cZn-、dRm-四种离子的电子层结构相同知,这四种离子的核外电子数相等,得核外电子数=核内质子数-阳离子的电荷数=核内质子数+阴离子的电荷数,原子序数=核内质子数,所以得:a-m=b-n=c+n=d+m,即b-d=m+n.
故选D.
点评 本题考查了原子结构,为高频考点,侧重于学生的分析能力的考查,注意在离子的电子层结构相同的条件下,如果电荷的正负性相同,其原子序数之差=电荷数之差,如果电荷的正负性相反,其原子序数之差=电荷数之和,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 10 (b-2a)mol•L-1 | B. | 5(b-2a)mol•L-1 | C. | 2(b-a)mol•L-1 | D. | 10(2a-b)mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

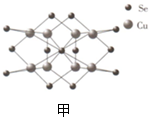
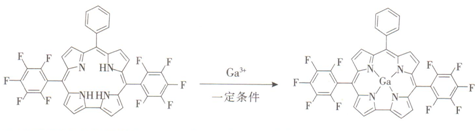
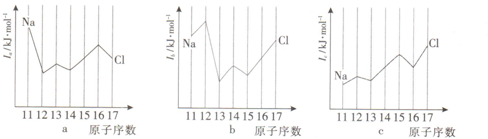
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数为34 | |
| B. | 最高价氧化物的水化物的分子式为:H2SeO4 | |
| C. | Se的非金属性比Br强 | |
| D. | 气态氢化物的稳定性比硫化氢气体弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 金属 | 电子流动方向 | 电压/V |
| Fe | Fe→Cu | +0.78 |
| Zn | Zn→Cu | +1.10 |
| A | Cu→A | -0.15 |
| B | B→Cu | +0.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ,其中含有的化学键类型为离子键、非极性键
,其中含有的化学键类型为离子键、非极性键查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. |  研究的是温度、压强对平衡的影响,横坐标表示压强 | |
| B. | 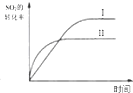 研究的是温度对平衡的影响,Ⅱ采用的温度更高 | |
| C. | 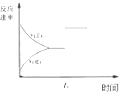 图中t0时使用了催化剂,使平衡向正反应方向进行 | |
| D. | 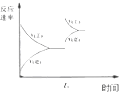 图中t0时增大压强,使平衡向正反应方向进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
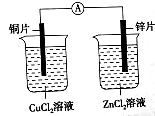 某实验小组拟用铜片、锌片、CuCl2溶液、ZnCl2溶液等设计原电池.并将装置图画到了如图所示程度.
某实验小组拟用铜片、锌片、CuCl2溶液、ZnCl2溶液等设计原电池.并将装置图画到了如图所示程度.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com