
分析 (1)该反应中I元素化合价由-1价变为0价,碘酸根离子和亚硫酸根离子发生氧化还原反应生成硫酸根离子、碘、氢离子和水;
(2)①碘离子具有还原性、碘酸根离子具有强氧化性,试样加酸酸化,如果加淀粉溶液后试样溶液变蓝,说明有碘单质生成,则存在碘离子和碘酸根离子;
②试样酸化后,然后向溶液中加入氧化剂,如果加入淀粉溶液后试样溶液变蓝,说明试样中存在I-;
③试样酸化后,如果直接使淀粉碘化钾试纸变蓝色,就说明含有碘酸根离子.
解答 解:(1)该反应中I元素化合价由-1价变为0价,则生成1mol I2时转移的电子数是2mol,
碘酸根离子和亚硫酸根离子发生氧化还原反应生成硫酸根离子、碘、氢离子和水,离子方程式为2IO3-+5HSO3-=3H++5SO42-+I2+H2O,
故答案为:2;2IO3-+5HSO3-=3H++5SO42-+I2+H2O;
(2)①碘离子具有还原性、碘酸根离子具有强氧化性,试样加酸酸化,如果加淀粉溶液后试样溶液变蓝,说明有碘单质生成,则存在碘离子和碘酸根离子,离子反应方程式为5I-+IO3-+6H+=3I2+3H2O,故答案为:5I-+IO3-+6H+=3I2+3H2O;
②试样酸化后,然后向溶液中加入氧化剂,如FeCl3(或H2O2),如果加入淀粉溶液后试样溶液变蓝,说明试样中存在I-,故答案为:FeCl3(或H2O2);
③试样酸化后,如果直接使淀粉碘化钾试纸变蓝色,则碘离子被氧化生成碘单质,就说明原溶液含有碘酸根离子,故答案为:淀粉-KI.
点评 本题考查碘元素及其化合物的性质,侧重考查性质实验方案设计,涉及离子检验、离子方程式的书写,明确物质性质是解本题关键,会利用已知知识采用知识迁移方法解答问题,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 沸点HBr>HCl,则同族元素氢化物沸点HCl>HF | |
| B. | Fe3O4可表示为FeO•Fe2O3,则Pb3O4可表示为PbO•Pb2O3 | |
| C. | CO2与Na2O2反应只生成Na2CO3和O2,故SO2与Na2O2反应也只生成Na2SO3和O2 | |
| D. | 因为N元素的非金属性比P元素强,所以HNO3的酸性强于H3PO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,33.6L氟化氢中含有氟原子的数目为1.5NA | |
| B. | 3mol铁与足量的水蒸气充分反应,转移8NA个电子 | |
| C. | 50mL18.4mol•L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA | |
| D. | 某密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应,转移电子的数目为0.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A是Zn,B是Cu,C为稀硫酸 | B. | A是Cu,B是Zn,C为稀硫酸 | ||
| C. | A是Fe,B是Ag,C为稀AgNO3溶液 | D. | A是Ag,B是Fe,C为稀AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
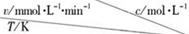 | 0.600 | 0.500 | 0.400 | 0.300 |
| 318.2 | 3.60 | 3.00 | 2.40 | 1.80 |
| 328.2 | 9.00 | 7.50 | a | 4.50 |
| b | 2.16 | 1.80 | 1.44 | 1.08 |
| A. | a=7.50 | |
| B. | 同时改变反应温度和蔗糖的浓度,v可能不变 | |
| C. | b>318.2 | |
| D. | 温度为b时,蔗糖浓度减少一半所需的时间比318.2K时短 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4、C2H6 | B. | C2H4、C3H6 | C. | C2H4、C2H4O | D. | C4H8、C6H12O6 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
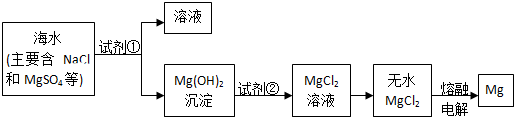
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水中的钢闸门连接电源的负极 | |
| B. | 地下钢管连接锌板 | |
| C. | 铁件镀铜 | |
| D. | 自行车的钢圈和车铃上镀上一层铬,既耐腐蚀又美观耐磨 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
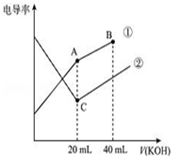 电导率是衡量电解质溶液导电能力大小的物理量,据溶液电导率变化可以确定滴定反应的终点.如图是某同学用0.1mol/L KOH溶液分别滴定体积均为20mL、浓度均为0.1mol/L的HCl和CH3COOH溶液滴定曲线示意图(混合溶液体积变化忽略不计).下列有关判断不正确的是( )
电导率是衡量电解质溶液导电能力大小的物理量,据溶液电导率变化可以确定滴定反应的终点.如图是某同学用0.1mol/L KOH溶液分别滴定体积均为20mL、浓度均为0.1mol/L的HCl和CH3COOH溶液滴定曲线示意图(混合溶液体积变化忽略不计).下列有关判断不正确的是( )| A. | 曲线①代表0.1 mol/L KOH溶液滴定CH3COOH溶液的滴定曲线,曲线②代表0.1 mol/L KOH溶液滴定HCl溶液的滴定曲线 | |
| B. | 在相同温度下,C点水电离的c(H+)小于A点水电离的 c(H+) | |
| C. | 在A点的溶液中有:c(CH3COO-)+c(OH-)-c(H+)=0.1 mol/L | |
| D. | 在B点的溶液中有:c(K+)>c(OH-)>c(CH3COO-)>c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com