
 ,由于醚键比较稳定故利用 此反应可保护醛基,也可以合成缩醛类有机物,下列说法中不正确的是( )
,由于醚键比较稳定故利用 此反应可保护醛基,也可以合成缩醛类有机物,下列说法中不正确的是( )| A. | 保护 1mol 醛基时也可用2molCH3CH2OH | |
| B. | 合成 1mol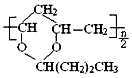 需要 1mol 需要 1mol 和 nmolCH3CH2CH2CHO 和 nmolCH3CH2CH2CHO | |
| C. | 通过上述反应合成的 其核磁共振氢谱中峰面积之比为1:1:1:1:1:2:2:3 其核磁共振氢谱中峰面积之比为1:1:1:1:1:2:2:3 | |
| D. | 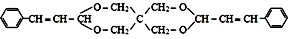 可由 C(CH2OH)4 与 可由 C(CH2OH)4 与 通过上述反应得到 通过上述反应得到 |
分析 A.由题给信息可知1mol醛基可与2mol羟基反应;
B. 由CH2=CHOH与CH3CH2CH2CHO生成;
由CH2=CHOH与CH3CH2CH2CHO生成;
C. 结构不对称,含有8种H;
结构不对称,含有8种H;
D.由信息可知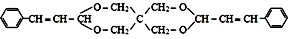 对应的反应物之一应含有4个-OH.
对应的反应物之一应含有4个-OH.
解答 解:A.由题给信息可知1mol醛基可与2mol羟基反应,则保护 1mol 醛基时也可用2molCH3CH2OH,故A正确;
B. 对应的单体含有C=C键,由nmol CH2=CHOH与0.5nmolCH3CH2CH2CHO生成,故B错误;
对应的单体含有C=C键,由nmol CH2=CHOH与0.5nmolCH3CH2CH2CHO生成,故B错误;
C. 结构不对称,含有8种H,且核磁共振氢谱中峰面积之比为1:1:1:1:1:2:2:3,故C正确;
结构不对称,含有8种H,且核磁共振氢谱中峰面积之比为1:1:1:1:1:2:2:3,故C正确;
D.由信息可知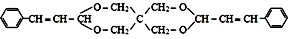 对应的反应物之一应含有4个-OH,为 C(CH2OH)4 与
对应的反应物之一应含有4个-OH,为 C(CH2OH)4 与 ,故D正确.
,故D正确.
故选B.
点评 本题考查有机物的合成,为高频考点,侧重考查学生的分析能力,注意把握有机物的结构和官能团的性质以及题给信息,答题时注意仔细审题,难度较大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | Li是正极,电极反应为Li-e-═Li+ | |
| B. | Li是负极,电极反应为Li-2e-═Li2+ | |
| C. | MnO2是负极,电极反应为MnO2+e-═MnO2- | |
| D. | Li是负极,电极反应为Li-e-═Li+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S2Cl2晶体中存在离子键和极性共价键 | |
| B. | S2Cl2分子中各原子均达到8电子稳定结构 | |
| C. | S2Cl2的水溶液能导电,所以S2Cl2是电解质 | |
| D. | S2Cl2与水反应后生成的气体通入石蕊试液中,现象是溶液先变红后褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+一定存在,且c(K+)≥0.02mol•L-1 | B. | 100mL溶液中含CO32-0.0lmol | ||
| C. | K+不一定存在 | D. | Cl-一定存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该合金中铜与镁的物质的量之比是 2:1 | |
| B. | 该浓硝酸中 HNO3 的物质的量浓度是 14.0 mol/L | |
| C. | NO2 和 N2 O4 的混合气体中,NO2 的体积分数是 80% | |
| D. | 得到 2.54 g 沉淀时,加入 NaOH 溶液的体积是 600 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某溶液中可能含有H+、Na+、NH4+、Fe3+、Al3+、SO42-等离子.向该溶液中滴加NaOH溶液,生成沉淀的物质的量变化曲线如右图所示.下列有关判断正确的是( )
某溶液中可能含有H+、Na+、NH4+、Fe3+、Al3+、SO42-等离子.向该溶液中滴加NaOH溶液,生成沉淀的物质的量变化曲线如右图所示.下列有关判断正确的是( )| A. | m点处反应:H++OH-=H2O | |
| B. | 溶液中n(SO42- )=2.5mol | |
| C. | 若取原溶液做焰色反应实验,焰色应为黄色 | |
| D. | 原溶液中存在的主要离子:n(H+ )=n(NH4+ )=n(Al3+ ) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com