
| A. | 氯化钠溶液中滴入硝酸银溶液 | B. | 碳在氧气中燃烧 | ||
| C. | 铁片置于硫酸铜溶液中 | D. | 氢氧化钠溶液与稀硫酸反应 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
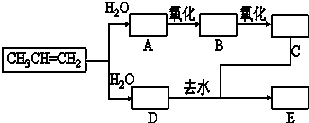 已知:①丙烯与水进行加成反应,其可能的产物有两种;②图中E为开链的酯类化合物,其分子式为C6H12O2.
已知:①丙烯与水进行加成反应,其可能的产物有两种;②图中E为开链的酯类化合物,其分子式为C6H12O2.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 周期族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | A | B | C | D | ||||
| 3 | E | F | G | H |
| X | ||
| Y | Z | W |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该有机物的最简式为C2H3 | |
| B. | 该有机物分子中肯定不含有碳碳叁键 | |
| C. | 该有机物不可能含有氧元素 | |
| D. | 该有机物不可能是丁烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原电池是把电能转化为化学能的装置 | |
| B. | 原电池中电子流出的一极是负极,发生还原反应 | |
| C. | 构成原电池的两极必须是两种不同的金属 | |
| D. | Cu-Fe稀硫酸原电池工作时,铜是正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验编号 | 盐酸的浓度(mol?L-1) | MOH溶液的浓度(mol?L-1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | a |
| 乙 | 0.2 | c1 | 7 |
| 丙 | 0.1 | 0.1 | 5 |
| A. | 甲组混合溶液中M+水解程度较丙组中大,且a<5 | |
| B. | 甲组混合溶液中:c(Cl-)>c(M+)>c(H+)>c(OH-) | |
| C. | 乙组混合溶液中:c(M+)+c(MOH)>0.1mol?L-1,且c1>0.2 | |
| D. | 丙组混合溶液中:c(OH-)+c(MOH)=1×10-5 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
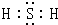 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com