
�����й�ʵ��ԭ���������ͽ��۶���ȷ����
A.��FeCl3��Һ�еμӹ�����ˮ������ȡFe(OH)3����
B.ȡ������ҺX�������м����������ư�ˮ���ټӼ���KSCN��Һ����Һ��죬˵��X��Һ��һ������Fe2��
C.���������������ӵĻ����Һ�м�������NaOH��Һ�������ú��Һ���ɳ�ȥ������������
D.��֪I3�� I2��I������ʢ��KI3��Һ���Թ��м�������CCl4�����ú�CCl4������ɫ��˵��KI3��CCl4�е��ܽ�ȱ���ˮ�еĴ�
I2��I������ʢ��KI3��Һ���Թ��м�������CCl4�����ú�CCl4������ɫ��˵��KI3��CCl4�е��ܽ�ȱ���ˮ�еĴ�
 �������ͬ������ϵ�д�
�������ͬ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ͼ�У�PΪһ�����ɻ����Ļ������ر�K���ֱ�������A��B�и�����2 mol X�� 2 mol Y����ʼʱ��VA��a L��VB��0.8a L(��ͨ�ܵ�������Բ���)������ͬ�¶Ⱥ��д������ڵ������£��������и��Է���������Ӧ��3X(g)��3Y(g)
2 mol Y����ʼʱ��VA��a L��VB��0.8a L(��ͨ�ܵ�������Բ���)������ͬ�¶Ⱥ��д������ڵ������£��������и��Է���������Ӧ��3X(g)��3Y(g)  2Z(g)��2W(g)���ﵽƽ��ʱ��VB��0.6a L������˵��������� ( )
2Z(g)��2W(g)���ﵽƽ��ʱ��VB��0.6a L������˵��������� ( )
A��B��X��ת����Ϊ75%
B��A��X��ת���ʱ�B�еĵ�
C��ƽ��ʱA�л�������ܶȱ�BС
D����K��һ��ʱ���Ӧ�ٴδﵽƽ�⣬��B�����Ϊ1.2a L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ϩ����һ�������·���������Ӧ��̼̼˫�����ѣ��磺R1CH=== CHR2��������Ϊ
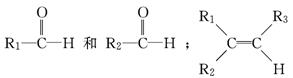 | |||
������Ϊ 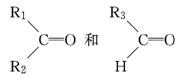 ���ɴ��ƶϷ���ʽΪC4H8��ϩ��������������
���ɴ��ƶϷ���ʽΪC4H8��ϩ��������������
(�� ��)
A��2�� B��3�� C��4�� D��6��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ͼ��ʾA��F����������
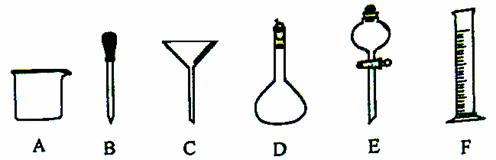
��1��д���������ƣ�D ��E ��
��2�������˵������A����;�����ֻ��������ϣ� ��
��3��ʵ��������һ�����ʵ���Ũ�ȵ����ᣬ����36.5%��Ũ����4.5mL��ȡ��4.5mL����ʱ����Ҫ����ͼ�����е�F�� �����ţ���
��4������ʵ��������õ�����C���� ��ѡ������ѡ�����ĸ��ţ���
a������ˮ��CCl4�Ļ����
b������ˮ�;ƾ��Ļ����
c������ˮ����ɰ�Ļ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ϩͪ(CH2=C=O)��һ�����������뺬������Ļ�������ӳɷ�Ӧ����Ӧ�ɱ�ʾ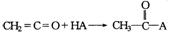 ����ϩͪ��һ�������¿��������Լ��ӳɣ�����ﲻ��ȷ����
����ϩͪ��һ�������¿��������Լ��ӳɣ�����ﲻ��ȷ����
A����CH3OH�ӳ�����CH3CH2COOH B����H2O�ӳ�����CH3COOH
C����CH3COOH�ӳ�����CH3��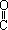 ��O��
��O��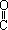 ��CH3 D����HCl�ӳ�����CH3COCl
��CH3 D����HCl�ӳ�����CH3COCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���е����ʵ�����ͭ�����Ļ����17.2 g����50.0 mL��Ũ����ǡ����ȫ��Ӧ����������4.48 L(��״��)��������˵����ȷ����
A��������������0.2 mol NO2
B����������ʵ���Ũ��Ϊ12 mol·L��1
C����Ӧ�б���ԭ��δ����ԭ���������ʵ���֮��Ϊ3��2
D��Ҫʹ����������ǡ����ȫ��ˮ������Ҫͨ������0.075 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������зḻ��ʳƷ���������Դ��ҩ���ˮ����Դ�ȣ�����ͼ��ʾ����
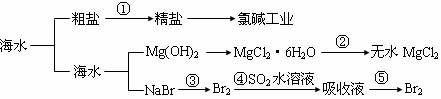
�����й�˵����ȷ����
A���ڢٲ��г�ȥ�����е�SO42-��Ca2+��Mg2+��Fe3+���ʣ������ҩƷ˳��Ϊ��
Na2CO3��Һ��NaOH��Һ��BaCl2��Һ�����˺������
B����ҵ�Ͻ�������ͨ���ȼҵ������ȡ
C���ӵڢ۲����ڢݲ���Ŀ����Ϊ��Ũ��
D���ڵڢۢܢݲ�����Ԫ�ؾ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���бȽϻ������ȷ����( )
A���ȶ��ԣ�NH3<PH3<ASH3
B�����Ӱ뾶��Cl->S2->Al3+
C�����ԣ�HClO4>H2SO4>H3PO4
D�����ԣ�Be��OH��2>Mg��OH��2>Al��OH��3
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com