

| 滴定次数 实验数据(mL) | 1 | 2 | 3 | 4 |
| V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |


科目:高中化学 来源:不详 题型:单选题
 2SO3(g) △H=-196 kJ·mol-1,维持容器温度不变,第一次反应达到平衡时共放出热量176.4kJ,此时再向容器中充入2 molSO2和1 molO2,达到新平衡,则下列说法正确的是
2SO3(g) △H=-196 kJ·mol-1,维持容器温度不变,第一次反应达到平衡时共放出热量176.4kJ,此时再向容器中充入2 molSO2和1 molO2,达到新平衡,则下列说法正确的是| A.若使用高效催化剂,第一次达到平衡时放出热量大于176.4kJ |
| B.第一次反应达到平衡时,容器内压强为0.7p |
| C.达到新平衡时,该反应的平衡常数增大 |
| D.若升高容器的温度可使新平衡时各物质的体积分数与第一次平衡时相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
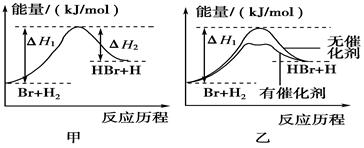
| A.正反应吸热 |
| B.加入催化剂,该化学反应的反应热不变 |
| C.加入催化剂后,该反应的能量对反应历程的示意图可用图乙表示 |
| D.加入催化剂可增大正反应速率,降低逆反应速率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.物质发生化学反应的反应热仅指反应放出的热量 |
| B.热化学方程式中各物质的化学计量数只表示物质的量,不表示分子的个数 |
| C.所有的燃烧反应都是放热的 |
| D.热化学方程式中,化学式前面的化学计量数可以是分数 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.需要加热才能发生的反应就一定是吸热反应 |
| B.将Ba(OH)2·8H2O晶体与NH4Cl晶体混合、搅拌,会放出大量的热 |
| C.在反应2CO+O2==2CO2中,反应物的总能量高于生成物的总能量 |
| D.1mol CaCO3固体完全分解会吸收178.5kJ的热量,其热化学方程式表示为:CaCO3 ="=" CaO + CO2△H = +178.5kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.△H>0 | B.X能量一定高于M |
| C.该反应一定不必加热就可以发生 | D.该反应为放热反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com