
分析 (1)A.增加Ni的量不影响平衡移动;
B.缩小容器容积,增大压强,平衡向气体体积减小的方向移动,但焓变不变;
C.反应达到平衡后,充入CO再次达到平衡时,相当于增大压强;
D.同一物质的正逆反应速率相等或反应体系中改变的物理量不变时,可逆反应达到平衡状态;
(2)CO (g)+$\frac{1}{2}$ O2(g)═CO2(g)△H=-Q1 kJ•mol-1①
S(s)+O2(g)═SO2(g)△H=-Q2 kJ•mol-1②
将方程式2①-②得SO2(g)+2CO (g)═S(s)+2CO2(g)△H进行相应的改变;
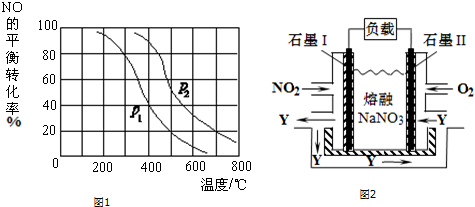
(3)①相同温度下,增大压强平衡正向移动,NO转化率增大;
②该反应2NO(g)+O2(g)?2NO2(g),
开始(mol/L)10 10 0
反应(mol/L)10×0.2=2 1 2
平横(mol/L)8 9 2
化学平衡常数K=$\frac{{c}^{2}(N{O}_{2})}{{c}^{2}(NO).c({O}_{2})}$;
(4)据题意,根据通入气体判断两极,电极反应式和电池反应式,根据电池总反应4NO2+O2=2N2O5,求出消耗O2的量.
解答 解:(1)A.Ni是固体,增加Ni的量不影响平衡移动,所以CO的转化率不变,故A错误;
B.缩小容器容积,增大压强,平衡向气体体积减小的方向移动,焓只与化学计量数有关,方程式不变,则焓变不变,故B错误;
C.反应达到平衡后,充入CO再次达到平衡时,相当于增大压强,平衡正向移动,CO转化率增大,故C正确;
D.当4v正[Ni(CO)4]=v正(CO)时,反应速率方向一致,不能判断平衡状态,但反应前后气体总质量改变、容器体积不变,所以反应前后容器中混合气体密度改变,当容器中混合气体密度不变时,该反应达到平衡状态,故D错误;
故选C;
(2)CO (g)+$\frac{1}{2}$ O2(g)═CO2(g)△H=-Q1 kJ•mol-1①
S(s)+O2(g)═SO2(g)△H=-Q2 kJ•mol-1②
将方程式2①-②得SO2(g)+2CO (g)═S(s)+2CO2(g)△H=(Q2-2Q1)kJ•mol-1,
故答案为:(Q2-2Q1)kJ•mol-1;
(3)①相同温度下,增大压强平衡正向移动,NO转化率增大,相同温度下P1到P2,NO转化率增大,平衡正向移动,则p2>p1,故答案为:p2>p1;
②该反应2NO(g)+O2(g)?2NO2(g),
开始(mol/L)10 10 0
反应(mol/L)10×0.2=2 1 2
平横(mol/L)8 9 2
化学平衡常数K=$\frac{{c}^{2}(N{O}_{2})}{{c}^{2}(NO).c({O}_{2})}$=$\frac{{2}^{2}}{{8}^{2}×9}$L/mol=$\frac{1}{144}$L/mol,
故答案为:$\frac{1}{144}$L/mol;
(4)据题意,通O2一极为正极,电极反应式为O2+2N2O5+4e-=4NO3-;通NO2一极为负极,电极反应为:NO2+NO3--e-=N2O5,根据电池总反应4NO2+O2=2N2O5,收集到20molN2O5需消耗O2为10mol,标准状况下体积为224L.
故答案为:NO2+NO3--e-=N2O5; 224.
点评 本题考查较综合,涉及化学平衡计算、原电池原理、化学平衡影响因素、盖斯定律等知识点,为高考常考查点,侧重考查学生分析判断、计算及知识综合运用能力,注意:固体或纯液体不影响平衡移动,难点是电极反应式的书写,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | NaOH溶解后未经冷却,迅速转移到容量瓶中 | |
| B. | 容量瓶未干燥 | |
| C. | 定容时俯视液面 | |
| D. | 洗涤烧杯和玻璃棒的溶液未转移到容量瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
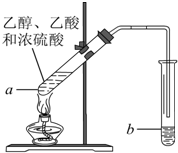 红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯.在实验室也可以用如图所示的装置制取乙酸乙酯,请回答下列问题.
红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯.在实验室也可以用如图所示的装置制取乙酸乙酯,请回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ③ | ④ | ⑤ | |||||
| 3 | ① | ② | ⑥ | ⑦ | ⑧ | |||
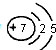 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高温、低压 | B. | 适宜的温度、高压、催化剂 | ||
| C. | 低温、低压 | D. | 低温、高压、催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| N2+3H2?2NH3 | ||||
| 温度 | 25℃ | 200℃ | 400℃ | 600℃ |
| 平衡常数K | 5×108 | 650 | 0.507 | 0.01 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2、SO3都是极性分子 | |
| B. | KF是离子化合物,HF为共价化合物 | |
| C. | 在NH4+和[Cu(NH3)4]2+中都存在配位键 | |
| D. | PCl3和NF3分子中所有原子的最外层都达到8电子稳定结构 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com