
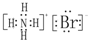 .
.分析 (1)溴化铵为离子晶体,由铵根离子与溴离子通过离子键结合在一起;
(2)氯气和石灰乳反应生成氯化钙、次氯酸钙和水;
(3)碳酸钠与氢氧化钙反应生成碳酸钙和氢氧化钠,碳酸钠为易溶于水易电离的物质,石灰乳为悬浊液离子反应中应写化学式;
(4)根据氧化还原反应中得失电子数相等和质量守恒配平.
解答 解:(1)溴化铵是离子化合物,由铵根离子与溴离子构成,电子式为: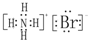 ,
,
故答案为: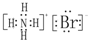 ;
;
(2)以氯气和石灰乳为原料制造漂白粉,反应生成CaCl2、Ca(ClO)2、H2O,该反应为2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O,
故答案为:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O;
(3)碳酸钠与氢氧化钙反应生成碳酸钙和氢氧化钠,碳酸钠、氢氧化钠拆成离子,离子反应为:Ca(OH)2+CO32-═CaCO3+2OH-,
故答案为:Ca(OH)2+CO32-═CaCO3+2OH-;
(4)双氧水中氧元素的化合价从-1价升高到0价,失去1个电子.而高锰酸钾中锰元素的化合价从+7价降低到+2价,得到2个电子,所以根据电子的得失守恒可知,配平后的反应为2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑,
故答案为:2;5;6H+;2;8;5O2↑.
点评 本题考查了电子式、化学方程式的书写,注意掌握电子式的概念及表示方法,氧化还原反应应把握反应中元素的化合价变化为解答的关键,侧重分析、应用能力的考查,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 丙烯(CH3CH=CH2)在一定条件下加聚后可得聚丙烯: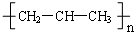 | |
| B. | 某塑料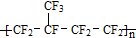 可由CF2=CF2和CF2=CFCF3通过加聚反应制得 可由CF2=CF2和CF2=CFCF3通过加聚反应制得 | |
| C. | 合成高分子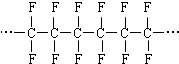 的单体是CF2=CF2 的单体是CF2=CF2 | |
| D. | 一种全降解塑料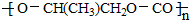 可由 可由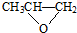 和 CO2在催化剂作用下加聚生成 和 CO2在催化剂作用下加聚生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2016年9月“G20”峰会即将在杭州举行,为了给外国友人一个美好蓝天,全国各地各化工企业推进脱硫、脱硝、除尘等设施改造,能大量减排SO2、NO2,使天空重现“APEC蓝” | |
| B. | 视频《穹顶之下》再次引起公众对“PM2.5”的关注.“PM2.5”是指大气中直径小于或等于2.5×10-6m的细小颗粒物,这些颗粒扩散在空气中形成胶体 | |
| C. | 有机玻璃是以有机物A(甲基丙烯酸甲酯)为单体,通过加聚反应得到的,合成A的一种途径是:CH3C≡CH+CO+CH3$\stackrel{pd}{OH}$→CH2≡(CH3)COOCH3,其过程符合绿色化学的原则 | |
| D. | 近期在西非国家爆发的埃博拉疫情呈加速蔓延之势,已知该病毒对化学药品敏感,双氧水、“84”消毒液均可以将病毒氧化而达到消毒的目的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 环保太阳能公厕已在多地投入使用,其顶部的太阳能电池板可将太阳能转变成电能和热能 | |
| B. | 我国已能利用3D打印技术,以钛合金粉末为原料,通过激光熔化逐层堆积,来制造飞机钛合金结构件,高温时可用金属钠还原相应的氯化物来制取金属钛 | |
| C. | 汽车尾气中的氮氧化物和碳氢化合物在大气环境中受强烈的太阳紫外线照射后产生一种新的二次污染物-光化学烟雾也会引起雾霾,汽车尾气中含有氮氧化物,原因是汽油燃烧不充分 | |
| D. | 生物炼铜法就是利用某种能耐受铜盐毒性的细菌,利用空气中的氧气把不溶性的硫化铜转化为可溶性的铜盐,从而使铜的冶炼变得成本低,污染小,反应条件十分简单 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
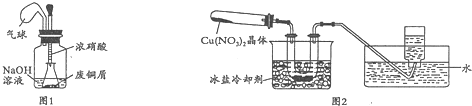
| 实验序号 | 1 | 2 | 3 | 4 |
| 温度/℃ | 35 | 50 | 70 | 95 |
| 样品颜色 | 深蓝色 | 深蓝色 | 浅绿色 | 暗蓝色 |
| 样品中碱式碳酸铜的质量分数/% | 90.9 | 92.7 | x | 92.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 萃取碘水中的碘时,将碘水倒入分液漏斗,然后再注入酒精,震荡静置后下层液体下口出,上层液体上口出 | |
| B. | 在蔗糖溶液中加入几滴稀硫酸,水浴加热5 min,加入NaOH溶液至碱性,再加入银氨溶液并水浴加热 | |
| C. | 将Fe(NO3)2固体溶于稀硫酸后,滴加KSCN溶液,溶液变红,说明已经Fe(NO3)2变质 | |
| D. | 提纯混有少量硝酸钾的氯化钠,应采用在较高温度下制得浓溶液再冷却结晶、过滤干燥 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
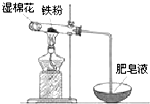 铁是日常生活中用途最广、用量最大的金属材料.
铁是日常生活中用途最广、用量最大的金属材料.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com