
| A. | 甲基的电子式: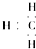 | B. | 乙炔的最简式:C2H2 | ||
| C. | 乙醛的结构简式:CH3COH | D. | 苯分子的比例模型: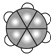 |
分析 A.甲基不带电荷,甲基中碳原子的外层有7个电子;
B.最简式为分子中各原子的最简比;
C.醛基的表示方法错误,应该为-CHO;
D.苯分子为平面结构,C的原子半径大于H原子.
解答 解:A.甲基不带电荷,甲基中碳原子的外层有7个电子,甲基的电子式: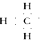 ,故A错误;
,故A错误;
B.C2H2为乙炔的分子式,其最简式为CH,故B错误;
C.乙醛中含有醛基,其正确的结构简式为:CH3CHO,故C错误;
D.碳原子的相对体积大于氢原子,则苯分子的比例模型为: ,故D正确;
,故D正确;
故选D.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及比例模型、电子式、结构简式、最简式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的分析能力及规范答题能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向0.1mol/L NaOH溶液滴加醋酸 | |
| B. | 向氢硫酸饱和溶液中通入氯气 | |
| C. | 向氯化铜溶液中加入适量氢氧化钡溶液 | |
| D. | 向硝酸银溶液通入氯化氢气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向某无色溶液中加入BaCl2,产生白色浑浊说明该溶液中一定有SO42- | |
| B. | 向淀粉碘化钾溶液中加氯水,溶液变为蓝色说明氯气的氧化性强于碘单质 | |
| C. | 硫酸能与NaCl反应生成HCl,说明硫酸的酸性比盐酸强 | |
| D. | 向某溶液中滴加稀盐酸无明显现象,再加硝酸银产生白色沉淀,说明溶液中含Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CuSO4[Cu(OH)2] | B. | NaOH[NaOH] | C. | CuCl2[CuCl2] | D. | NaCl[NaCl] |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 | B. | 13 | C. | 7 | D. | 1.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 维生素A: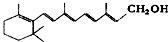 它是一种难溶于水的醇 它是一种难溶于水的醇 | |
| B. | 用灼烧并闻气味的方法区别纯棉织物和纯毛织物 | |
| C. | 某雨水样品采集后放置一段时间,pH值由4.68变为4.28,是因为水中溶解了较多的CO2 | |
| D. | 金属材料都是导体,非金属材料不都是绝缘体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com