
| ŹµŃé²½Öč | Ō¤ĘŚĻÖĻóŗĶ½įĀŪ |
| ²½Öč1£ŗȔɣĮæĖłµĆČÜŅŗÓŚŹŌ¹ÜÖŠ£¬µĪ¼Ó3mol£®L-1H2SOÖĮČÜŅŗ³ŹĖįŠŌ£¬Č»ŗó½«ĖłµĆČÜŅŗ·ÖÖĆÓŚA”¢BŹŌ¹ÜÖŠ | |
| ²½Öč2£ŗ | |
| ²½Öč3£ŗ |
·ÖĪö £Ø1£©ĒāŃõ»ÆÄĘ¹żĮ棬¶žŃõ»ÆĮņŗĶĒāŃõ»ÆÄĘ·“Ӧɜ³ÉŃĒĮņĖįÄĘŗĶĖ®£»
£Ø2£©øł¾Ż·“Ó¦ŌĄķ£ŗCl2+Na2SO3+2NaOHØT2NaCl+Na2SO4+H2O£»
£Ø3£©øł¾ŻĖłĻŽÖĘŹµŃéŹŌ¼ĮŗĶSO32-”¢ClO-µÄŠŌÖŹ£¬ĻČ¼ÓČėĮņĖįÖĮĖįŠŌ£¬Čō“ęŌŚSO32-”¢ClO-£¬·Ö±šÉś³ÉĮĖH2SO3ŗĶHClO£»ŅņĪŖHClO¾ßÓŠŃõ»ÆŠŌ£¬Ń”Ōńµķ·Ū-KIČÜŅŗ£¬Ö¤Ć÷ÓŠClO-µÄ“ęŌŚ£»H2SO3¾ßÓŠ»¹ŌŠŌ£¬Ń”Ōń¾ßÓŠĒæŃõ»ÆŠŌøßĆĢĖį¼ŲČÜŅŗ£¬Ö¤Ć÷SO32-µÄ“ęŌŚ£®
½ā“š ½ā£ŗ£Ø1£©SO2Óė¹żĮæNaOHČÜŅŗ·“Ó¦£¬ŅņNaOH¹żĮ棬¹ŹÉś³ÉµÄŹĒÕżŃĪ£¬»Æѧ·½³ĢŹ½ĪŖ£ŗSO2+2NaOH=Na2SO3+H2O£»
¹Ź“š°øĪŖ£ŗSO2+2NaOH=Na2SO3+H2O£»
£Ø2£©øł¾Ż·“Ó¦ŌĄķ£ŗCl2+Na2SO3+2NaOHØT2NaCl+Na2SO4+H2O£¬ĖłŅŌŅ»¶Ø“ęŌŚµÄŅõĄė×ÓĪŖ£ŗCl-”¢OH-£¬¹Ź“š°øĪŖ£ŗCl-”¢OH-£»
£Ø3£©ŅņĪŖĪüŹÕŅŗ³Ź¼īŠŌ£¬ĻČȔɣĮæĪüŹÕŅŗÓŚŹŌ¹ÜÖŠ£¬µĪ¼Ó3moL-L-1 H2SO4ÖĮČÜŅŗ³ŹĖįŠŌ£¬Č»ŗó½«ĖłµĆČÜŅŗ·ÖÖĆÓŚA”¢BŹŌ¹ÜÖŠĻČ¼ÓČėĮņĖįµÄŹŌ¹Ü£¬Čō“ęŌŚSO32-”¢ClO-£¬·Ö±šÉś³ÉĮĖH2SO3ŗĶHClO£»ĻņAŹŌ¹ÜÖŠµĪ¼Ó1-2µĪ0.01mol£®L-1KMnO4ČÜŅŗ£¬KMnO4Äܱ»SO32-»¹ŌĪŖĆĢĄė×Ó¶ųĶŹÉ«£¬ČÜŅŗ³ŹĒ³×ĻÉ«£¬ŌņÖ¤Ć÷²»“ęŌŚSO32-£»
ĻņBŹŌ¹ÜÖŠµĪ¼Ó1-2µĪµķ·Ū-KIČÜŅŗ£¬ClO-ÄÜÓėµāĄė×Ó·“Ӧɜ³Éµ„ÖŹµā£¬ČÜŅŗ»į±äĄ¶É«£¬ČōČÜŅŗ²»±äĄ¶É«£¬ŌņÖ¤Ć÷²»“ęŌŚClO-£®
¹Ź“š°øĪŖ£ŗ
| ŹµŃé²½Öč | Ō¤ĘŚĻÖĻóŗĶ½įĀŪ |
| ²½Öč1£ŗȔɣĮæĪüŹÕŅŗÓŚŹŌ¹ÜÖŠ£¬µĪ¼Ó3 moL•L-1 H2SO4ÖĮČÜŅŗ³ŹĖįŠŌ£¬Č»ŗó½«ĖłµĆČÜŅŗ·ÖÖĆÓŚA”¢BŹŌ¹ÜÖŠ | |
| ²½Öč2£ŗĻņAŹŌ¹ÜÖŠµĪ¼Ó1-2µĪ0.01mol£®L-1KMnO4ČÜŅŗ | ČÜŅŗ³ŹĒ³×ĻÉ«£¬ŌņÖ¤Ć÷²»“ęŌŚSO32- |
| ²½Öč3£ŗĻņBŹŌ¹ÜÖŠµĪ¼Ó1-2µĪµķ·Ū-KIČÜŅŗ | ČÜŅŗ²»±äĄ¶É«£¬ŌņÖ¤Ć÷²»“ęŌŚClO- |
µćĘĄ ±¾ĢāŹōÓŚŹµŃéĢ½¾æĢā£¬ŅŖøł¾ŻŹµŃéŌĄķĢį³ö¼ŁÉč£¬ŌŁ½įŗĻĪļÖŹµÄŠŌÖŹ¼ÓŅŌŃéÖ¤£¬²ąÖŲÓŚæ¼²éѧɜµÄŹµŃéĢ½¾æÄÜĮ¦ŗĶ¶ŌÖŖŹ¶µÄÓ¦ÓĆÄÜĮ¦£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Č«ĒņĘųŗņ±äÅÆæÉÄÜŹĒÓÉÓŚ¶žŃõ»ÆĢ¼ŗ¬ĮæµÄ¼±¾ēŌö¼Ó | |
| B£® | ĖįÓźæÉŅŌ·ÖĪŖĮņĖįŠĶĖįÓźŗĶĻõĖįŠĶĖįÓź | |
| C£® | ¾ÓŹŅÖŠµÄ×°äź²ÄĮĻ»ŗĀżŹĶ·Å³öĄ“µÄĪŪČ¾ĪļÖŠ×ī³£¼ūµÄŹĒ¼×Č©”¢±½µČÓŠ»śĪļÕōĘų | |
| D£® | ¼ģŃé¾ÓŹŅÖŠ¼×Č©ĘųĢåŹĒ·ń“ęŌŚ£¬æÉŅŌ³éČ”²¢ĶعżĘ·ŗģČÜŅŗĄ“¼ģŃé |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

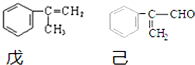
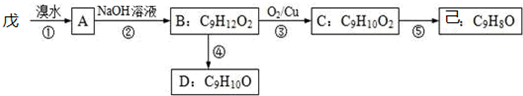
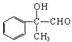
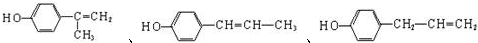 £®
£®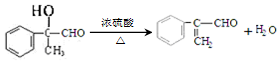 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ū¢Ü¢Ż | B£® | ¢Ś¢Ū¢Ü | C£® | ¢Ś¢Ū¢Ż | D£® | ¢Ł¢Ś¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
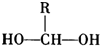 $\stackrel{-H_{2}O}{”ś}$
$\stackrel{-H_{2}O}{”ś}$ Ēėøł¾ŻĶ¼×÷“š£ŗ
Ēėøł¾ŻĶ¼×÷“š£ŗ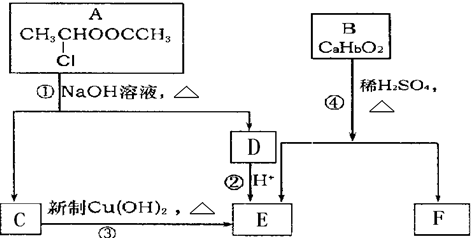

 Ӣ
Ӣ Ӣ
Ӣ Ӣ
”¢ £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ²»É÷½«Ėį½¦µ½ŃŪÖŠ£¬Ó¦Į¢¼“ÓĆøɲ¼²Į£¬ŗó±ßĻ“±ßÕ£ŃŪ¾¦ | |
| B£® | ²»É÷½«ÅؼīČÜŅŗÕ“µ½Ę¤·ōÉĻ£¬ŅŖĮ¢¼“ÓĆ“óĮæĖ®³åĻ“£¬Č»ŗóĶæÉĻÅšĖįČÜŅŗ | |
| C£® | ¾Ę¾«ŌŚŹµŃéĢØÉĻČ¼ÉÕŹ±£¬ÓĆĖ®ĘĖĆš»šŃę | |
| D£® | ÅäÖĘĮņĖįČÜŅŗŹ±£¬æÉĻČŌŚĮæĶ²ÖŠ¼ÓČėŅ»¶ØĢå»żµÄĖ®£¬ŌŁŌŚ½Į°čĻĀĀżĀż¼ÓČėÅØĮņĖį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
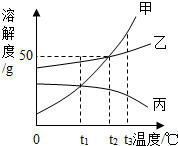
| A£® | t1”ꏱ£¬·Ö±šČ”³öĻąĶ¬ÖŹĮæµÄ¼×”¢±ūĮ½ÖÖ±„ŗĶČÜŅŗÉżĪĀµ½t2”ꏱ£¬¼×ŗĶŅŅČÜÖŹµÄÖŹĮæ·ÖŹżĻąµČ | |
| B£® | t2”ꏱ£¬½«¼×”¢ŅŅĮ½ÖÖ±„ŗĶČÜŅŗ·Ö±šŗćĪĀÕō·¢µČÖŹĮæµÄĖ®£¬Īö³ö¾§ĢåµÄÖŹĮææÉÄܲ»µČ | |
| C£® | ½«ČżÖÖ±„ŗĶČÜŅŗ·Ö±š“Ót3”ę½µµĶµ½t2”ꏱ£¬¼×ŗĶŅŅČÜÖŹµÄÖŹĮæ·ÖŹż¼õŠ”£¬±ūµÄČÜÖŹµÄÖŹĮæ·ÖŹż²»±ä | |
| D£® | µ±¼×µÄ±„ŗĶČÜŅŗÖŠŗ¬ÓŠÉŁĮæŅŅŹ±£¬æÉŅŌ²ÉČ”ĄäČ“Čȱ„ŗĶČÜŅŗµÄ°ģ·ØĢįČ”ŅŅ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | C+CO2 $\frac{\underline{\;¼ÓČČ\;}}{\;}$2CO | B£® | 2H2+O2 $\frac{\underline{\;øßĪĀ\;}}{\;}$2H2O | ||
| C£® | CaCO3 $\frac{\underline{\;µćČ¼\;}}{\;}$ CaO+CO2 | D£® | Ė®ÕōĘūÄż½į³ÉĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓƶčŠŌµē¼«µē½āČŪČŚĀČ»ÆÄĘ£ŗ2Cl-+2H2O$\frac{\underline{\;Ķصē\;}}{\;}$Cl2”ü+H2”ü+2OH- | |
| B£® | ĮņĖįĀĮČÜŅŗÖŠ¼ÓČėĘ«ĀĮĖįÄĘČÜŅŗ£ŗAl3++3AlO2-+6H2O=4Al£ØOH£©3”ż | |
| C£® | FeS¹ĢĢå·ÅČėĻ”ĻõĖįČÜŅŗÖŠ£ŗFeS+2H+=Fe2++H2S”ü | |
| D£® | ĀČ»ÆĀĮČÜŅŗÖŠ¼ÓČė¹żĮæ°±Ė®Al3++4NH3•H2O=AlO2-+4NH4++2H2O |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com