
| ×°ÖĆ | 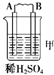 |
 |
 |
| ĻÖĻó | ¶ž¼Ū½šŹōA²»¶ĻČܽā | CµÄÖŹĮæŌö¼Ó | AÉĻÓŠĘųĢå²śÉś |


 ×÷Ņµøص¼ĻµĮŠ“š°ø
×÷Ņµøص¼ĻµĮŠ“š°ø Ķ¬²½Ń§µäŅ»æĪ¶ąĮ·ĻµĮŠ“š°ø
Ķ¬²½Ń§µäŅ»æĪ¶ąĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 ¶ĢÖÜĘŚÖ÷×åŌŖĖŲA”¢B”¢C”¢DµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬ĖüĆĒµÄŌ×ÓŗĖĶāµē×Ó²ćŹżÖ®ŗĶĪŖ7£®BµÄ»ÆŗĻĪļÖÖĄą·±¶ą£¬ŹżÄæÅÓ“ó£®AÓėDÄÜŠĪ³ÉŌ×ÓøöŹż±ČĪŖ1£ŗlŗĶ2£ŗlµÄ»ÆŗĻĪļ£®
¶ĢÖÜĘŚÖ÷×åŌŖĖŲA”¢B”¢C”¢DµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬ĖüĆĒµÄŌ×ÓŗĖĶāµē×Ó²ćŹżÖ®ŗĶĪŖ7£®BµÄ»ÆŗĻĪļÖÖĄą·±¶ą£¬ŹżÄæÅÓ“ó£®AÓėDÄÜŠĪ³ÉŌ×ÓøöŹż±ČĪŖ1£ŗlŗĶ2£ŗlµÄ»ÆŗĻĪļ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
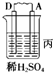
 2DB3£¬Čō3.2gDB2ĶźČ«×Ŗ»ÆĪŖDB3ĘųĢåŹ±·ÅČČakJ£»1mol DB3ĘųĢåĶźČ«×Ŗ»ÆĪŖĘäĖ®»ÆĪļ·ÅČČbkJ£¬Ōņ±źæöĻĀ33.6L DB2ĶźČ«Ķź³ÉÉĻŹöĮ½²½·“Ó¦·ÅČČ
2DB3£¬Čō3.2gDB2ĶźČ«×Ŗ»ÆĪŖDB3ĘųĢåŹ±·ÅČČakJ£»1mol DB3ĘųĢåĶźČ«×Ŗ»ÆĪŖĘäĖ®»ÆĪļ·ÅČČbkJ£¬Ōņ±źæöĻĀ33.6L DB2ĶźČ«Ķź³ÉÉĻŹöĮ½²½·“Ó¦·ÅČČ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
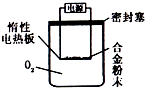
£Ø2013?·īĻĶĒų¶žÄ££©ÓÉA”¢B”¢C”¢DĖÄÖÖ½šŹō°“±ķ֊װÖĆ½ųŠŠŹµŃ飬ĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ£Ø””””£©
| |||||||||||||||
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com