TiO
2在很多领域有着广泛的应用前景.
(1)制备TiO
2的常见方法:将TiCl
4水解产物加热脱水生成TiO
2.已知常温下Ti(OH)
4的K
sp=7.94×10
-54,测得TiCl
4水解后溶液的pH=2,则此时溶液中c(Ti
4+)=
.
(2)制备纳米TiO
2的方法:以N
2为载体,用钛醇盐Ti(OR)
4和水蒸气反应生成Ti(OH)
4,再控制温度生成纳米TiO
2.温度控制不当会使产物含结晶水,测定产物aTiO
2?bH
2O组成的方法如下:
步骤一:取样品2.010g,在酸性条件下充分溶解,并用适量铝将TiO
2+还原为Ti
3+,过滤并洗涤,将所得滤液和洗涤液合并注入250mL容量瓶,并用稀硫酸定容,得待测液.
步骤二:取待测液25.00mL于锥形瓶中,加几滴KSCN溶液作指示剂,用0.1000mol?L
-1NH
4Fe(SO
4)
2标准溶液滴定,将Ti
3+氧化为TiO
2+.重复滴定2次.滴定所得的相关数据如表:
滴定
序号 |
待测液体积/mL |
NH4Fe(SO4)2标准溶液
滴定管起点读数/mL |
NH4Fe(SO4)2标准溶液
滴定管终点读数/mL |
| 1 |
25.00 |
0.02 |
24.02 |
| 2 |
25.00 |
0.08 |
24.06 |
| 3 |
25.00 |
0.12 |
24.14 |
①钛醇盐Ti(OR)
4和水蒸气反应的化学方程式为
.
②步骤一中用稀硫酸而不用水定容的原因是
.
③通过计算确定该样品的组成
(写计算过程).



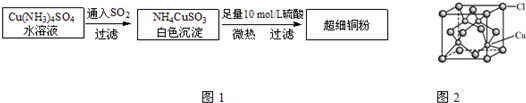
 (2009?广东)铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂.
(2009?广东)铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂.

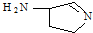 ,则分子中σ键与π键之比为
,则分子中σ键与π键之比为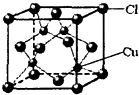 所示,该化合物的化学式为
所示,该化合物的化学式为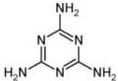 ).
).