
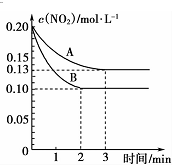
���� ��1����������A����Ӧ��ǰ3minv��NO2��=$\frac{��0.20-0.13��mol/L}{3min}$=0.035mol/��L��min����v��O2��=$\frac{1}{2}$ v��NO2����
�ڷ�Ӧ����ƽ���ʱ�����̣�˵����ѧ��Ӧ����B����A���Ҵﵽƽ��״̬ʱ��������ת����B����A��˵���ı�����ʱƽ�������ƶ��ҷ�Ӧ���ʼӿ죻
�۸÷�Ӧ������Ӧ�����ȷ�Ӧ�������¶�ƽ�������ƶ�����ѧƽ�ⳣ��ֻ���¶��йأ�
��2����ѧƽ�ⳣ��K����������Ũ����֮���뷴Ӧ��Ũ����֮���ıȣ�
����ƽ��ʱ���������c�� NO2��=0.4mol•L-1��������c��O2��Ϊ0.1mol/L��ʵ����c��O2��Ϊ1.3mol•L-1��˵�����������ֽ����c��O2��Ϊ1.2mol/L����Ӧ��c�� NO2��Ϊ2.4mol/L����������ת����=$\frac{�μӷ�Ӧ��c��N{O}_{2}��}{�����ɵ�c��N{O}_{2}��}$��
N2O5��g������ʼŨ��Ӧ����������ȫ�ֽ��Ũ�ȣ�
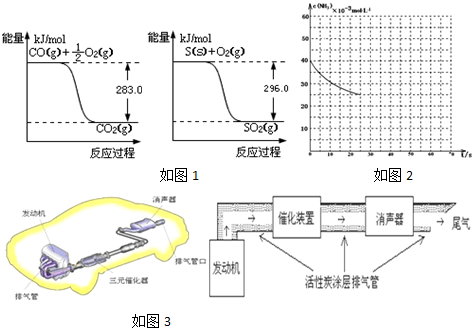
��3������������ǡ����ȫ��Ӧ�������ᣬ��Ӧ����ʽΪNO+NO2+O2+H2O=2HNO3�����ݷ���ʽ����x��
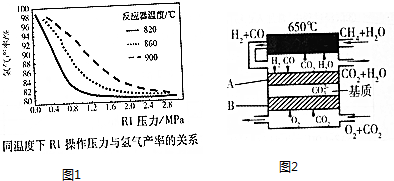
��4���ü�����һ�������¿����������������Ⱦ�����ɶ�����̼�͵�����ˮ������ת�Ƶ����غ㡢ԭ���غ���ƽ����ʽ��
��� �⣺��1����������A����Ӧ��ǰ3minv��NO2��=$\frac{��0.20-0.13��mol/L}{3min}$=0.035mol/��L��min����v��O2��=$\frac{1}{2}$ v��NO2��=$\frac{1}{2}$��0.035mol/��L��min��=0.0175mol/��L��min�����ʴ�Ϊ��0.0175mol/��L��min����
�ڷ�Ӧ����ƽ���ʱ�����̣�˵����ѧ��Ӧ����B����A���Ҵﵽƽ��״̬ʱ��������ת����B����A��˵���ı�����ʱƽ�������ƶ��ҷ�Ӧ���ʼӿ죬
����ͼ֪����Ӧ��ʼŨ�Ȳ��䣬��Ӧ�ﵽƽ��ʱ��������ת����������ʹ�ô���������ѹǿƽ�������ƶ�����������ת���ʼ�С�����Ըı������ֻ�����¶ȣ����������¶ȣ�
�ʴ�Ϊ���¶ȣ�
����A��B�ı�������������¶ȣ������¶ȶ�������ת��������˵��ƽ�������ƶ���������Ӧ�����ȷ�Ӧ�������¶�ƽ�ⳣ����������KA��KB���ʴ�Ϊ������
��2����ѧƽ�ⳣ��K����������Ũ����֮���뷴Ӧ��Ũ����֮���ıȣ���ѧƽ�ⳣ��K=$\frac{{c}^{4}��N{O}_{2}����c��{O}_{2}��}{{c}^{2}��{N}_{2}{O}_{5}��}$��
����ƽ��ʱ���������c�� NO2��=0.4mol•L-1��������c��O2��Ϊ0.1mol/L��ʵ����c��O2��Ϊ1.3mol•L-1��˵�����������ֽ����c��O2��Ϊ1.2mol/L����Ӧ��c�� NO2��Ϊ2.4mol/L����������ת����=$\frac{�μӷ�Ӧ��c��N{O}_{2}��}{�����ɵ�c��N{O}_{2}��}$=$\frac{2.4mol/L}{0.4mol/L+2.4mol/L}$=$\frac{6}{7}$��
N2O5��g������ʼŨ��Ӧ����������ȫ�ֽ��Ũ��=$\frac{2.4mol/L+0.4mol/L}{4}��2$=1.4mol/L��
�ʴ�Ϊ��K=$\frac{{c}^{4}��N{O}_{2}����c��{O}_{2}��}{{c}^{2}��{N}_{2}{O}_{5}��}$��$\frac{6}{7}$��1.4��
��3������������ǡ����ȫ��Ӧ�������ᣬ��Ӧ����ʽΪNO+NO2+O2+H2O=2HNO3�����ݷ���ʽ����x=$\frac{a+b}{2}$����ѡa��
��4���ü�����һ�������¿����������������Ⱦ�����ɶ�����̼�͵�����ˮ������ת�Ƶ����غ㡢ԭ���غ���ƽ����ʽΪ2NO2+CH4�TN2+CO2+2H2O��
�ʴ�Ϊ��2NO2+CH4�TN2+CO2+2H2O��
���� ���⿼�黯ѧƽ����㡢��������Ի�ѧƽ���ƶ�Ӱ���֪ʶ�㣬���ؿ���ѧ�������жϼ�����������ȷ�����������Ĺ�ϵˮ�Ȿ��ؼ����ѵ��ǣ�2�����������ת���ʵļ��㣬ע�����ɵ�����ΪI��II����ʽ�����������ܺͣ�Ϊ�״��㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶ȣ��棩 | 20 | 40 | 60 | 80 | 100 |
| ʯ�� | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| ���� | 32 | 44.6 | 61.8 | 83.8 | 114 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȼ�� | B�� | ���� | C�� | ʳ�� | D�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| t/s | 0 | 500s | 1 000s |
| c��H2��/��mol•L-1�� | 5.00 | 3.52 | 2.48 |
| c��CO��/��mol•L-1�� | 2.50 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
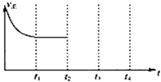 2013��9�£��й��������е������������ص������������������ӱ������ϵȵصĿ�����Ⱦ��Ϊ6��������Ⱦ�������ض���Ⱦ������β����ȼú����������ȡů�ŷŵ�CO2�ȶ��������γɵ�ԭ��
2013��9�£��й��������е������������ص������������������ӱ������ϵȵصĿ�����Ⱦ��Ϊ6��������Ⱦ�������ض���Ⱦ������β����ȼú����������ȡů�ŷŵ�CO2�ȶ��������γɵ�ԭ��| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ�������ʱ��/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ۺ͵���ø��Ϻ��� | |
| B�� | ��պ����������Ϊ75%�ľƾ������Ƥ�� | |
| C�� | �������߹�����䲡�� | |
| D�� | �ø������ֽ�����걾 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʱ�䣨min�� | 0 | 1 | 2 | 3 | 4 | 5 |
| n��CuO����mol�� | 0.080 | 0.060 | 0.040 | 0.020 | 0.020 | 0.020 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com