
| A. | 胶体和溶液都是均一、稳定的分散系,静置不易产生沉淀 | |
| B. | 胶体与纳米级微粒在直径上具有相同数量级 | |
| C. | 光线通过时,胶体产生丁达尔效应,溶液则无丁达尔效应 | |
| D. | 向Fe(OH)3胶体中逐滴加入稀硫酸无明显现象 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 研究和开发CO2和CO的创新利用是环境保护和资源利用双赢的课题.
研究和开发CO2和CO的创新利用是环境保护和资源利用双赢的课题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化钡溶液和盐酸 | B. | 硝酸银溶液和硝酸 | ||
| C. | 氯化钡溶液和硝酸银溶液 | D. | 硝酸钡溶液和硝酸银溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2[SO42-]=[NH4+]>[H+]=[OH-] | B. | [SO42-]>[NH4+]]>[H+]=[OH-] | ||
| C. | [NH4+]]>[SO42-]>c(OH-)>c(H+) | D. | [NH4+]]>[SO42-]>[H+]>[OH-] |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由X、Y、Z三种元素中的任意两种组成的具有10电子的微粒有4种 | |
| B. | X、Y、Z可以形成离子化合物 | |
| C. | Y和Z分别形成的简单离子,其离子半径为Y>Z | |
| D. | Y和Z可以组成一种Y和Z的质量比为7:20的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可能存在NaCl | B. | 可能存在Na2SO4 | C. | 一定存在FeCl3 | D. | 一定存在Ba(NO3)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
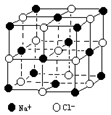 晶体具有规则的几何外形,晶体中最基本的重复单元称之为晶胞.NaCl晶体结构如图所示.
晶体具有规则的几何外形,晶体中最基本的重复单元称之为晶胞.NaCl晶体结构如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Na2O2+2H2O=4NaOH+O2↑ | B. | 2F2+2H2O=4HF+O2 | ||
| C. | 3NO2+H2O=NO+2HNO3 | D. | 3Fe+4H2O(g)$\frac{\underline{\;\;△\;\;}}{\;}$4H2+Fe3O4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com